Pytanie 1
Na przedstawionym scyntygramie ukazano duży obszar
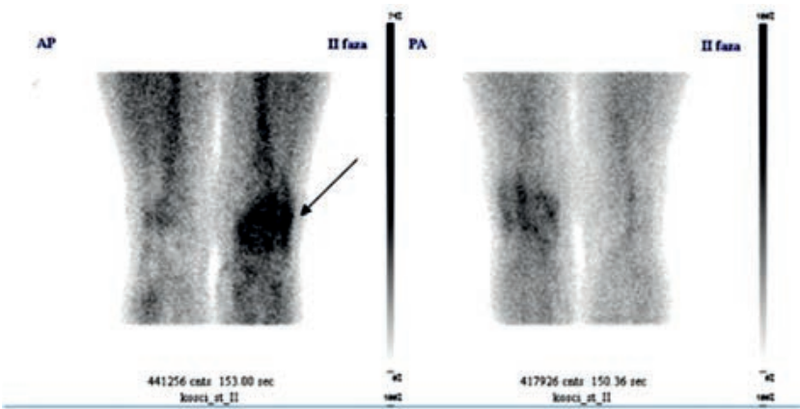
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Na przedstawionym scyntygramie ukazano duży obszar

W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
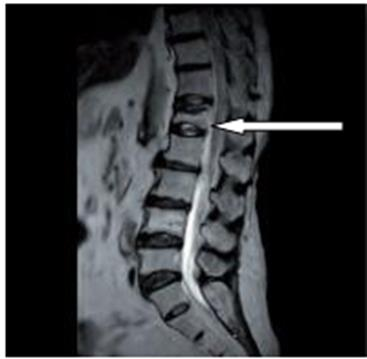
Na obrazie rezonansu magnetycznego strzałką oznaczono wyrostek kolczysty kręgu
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
Wskazaniem do wykonania badania spirometrycznego jest
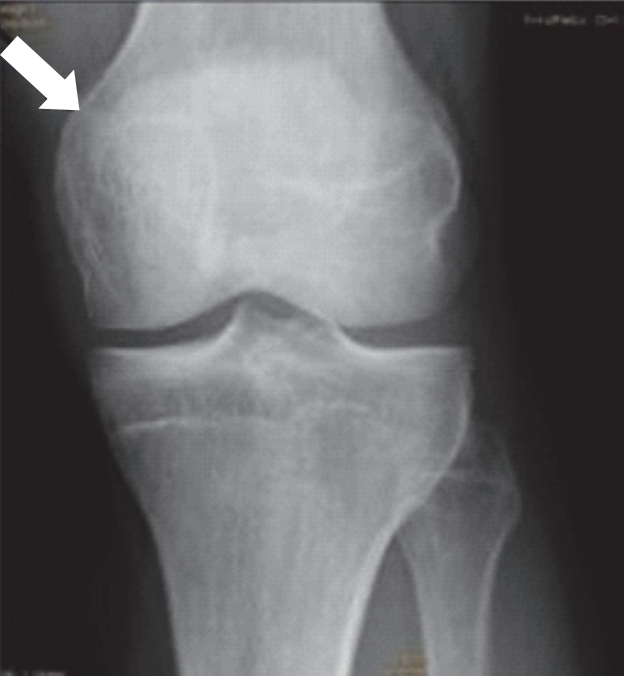
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
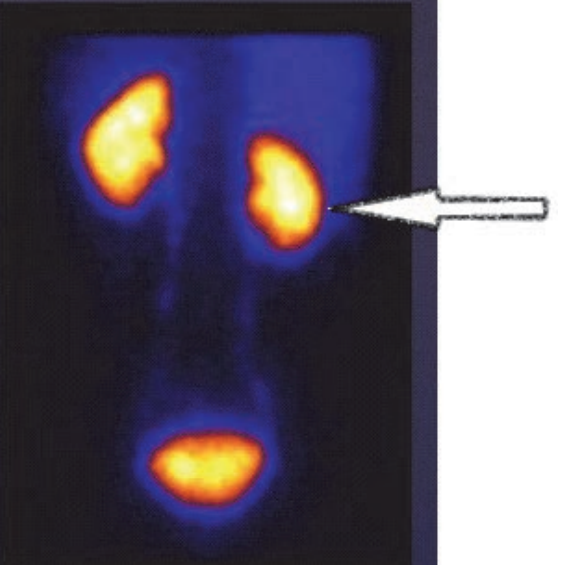
Na scyntygramie strzałką oznaczono
Który radioizotop stosuje się do badania scyntygraficznego kości?
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Nieostrość geometryczna obrazu rentgenowskiego zależy od
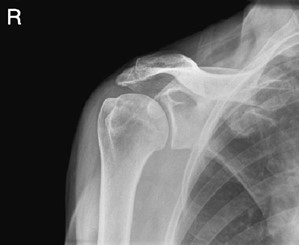
Na radiogramie uwidoczniono
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Które badanie, zgodnie z zakresem kompetencji, może samodzielnie wykonać technik elektroradiolog?
W badaniu EKG odprowadzenie I rejestruje różnicę potencjałów między
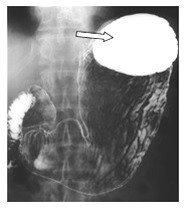
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
Do planowego badania TK klatki piersiowej z użyciem środka cieniującego pacjent powinien zgłosić się
Przy podejrzeniu ciała obcego w oczodole należy wykonać
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Na obrazie rentgenowskim strzałką zaznaczono
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
„Ognisko zimne” w obrazie scyntygraficznym oznacza
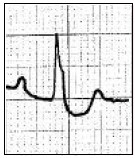
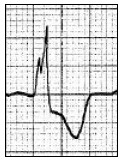
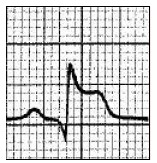
Który zapis EKG przedstawia falę Pardee'go?

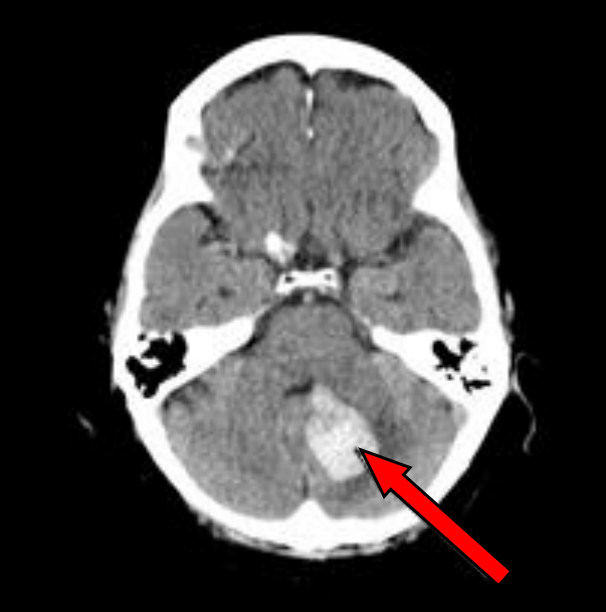
Na przekroju poprzecznym TK mózgu strzałką wskazano obszar
Celem radioterapii paliatywnej nie jest
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
Zarejestrowane na elektrokardiogramie miarowe fale f w kształcie „zębów piły” poprzedzielane prawidłowymi zespołami QRS są charakterystyczne dla
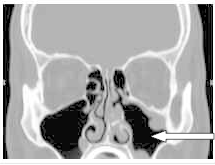
Na obrazie TK zaznaczono zatokę
Odprowadzenie II rejestruje różnicę potencjałów między
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
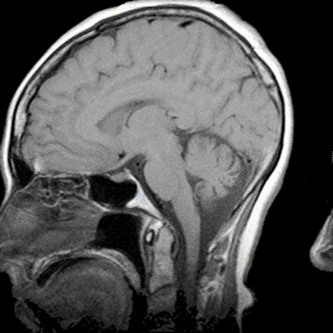
Który artefakt uwidoczniono na skanie RM głowy?
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
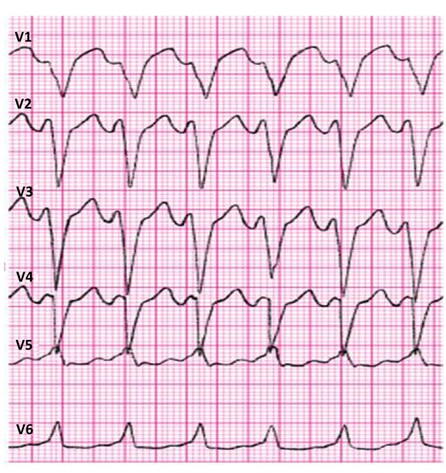
Które zaburzenie rytmu serca zarejestrowano na elektrokardiogramie?
Chorobą układu oddechowego typu obturacyjnego jest