Pytanie 1
Piktogram nie jest konieczny dla
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Piktogram nie jest konieczny dla
Zamieszczony fragment procedury opisuje sposób otrzymywania
| „W zlewce o pojemności 250 cm3 rozpuść w 50 cm3 wody destylowanej 5 g uwodnionego siarczanu(VI) miedzi(II). Do roztworu dodaj 16,7 cm3 roztworu NaOH o stężeniu 6 mol/dm3. Następnie dodaj 10 g glukozy w celu przeprowadzenia reakcji redukcji jonów miedzi(II) do miedzi(I). Ostrożnie ogrzewaj zlewkę z mieszaniną reakcyjną do otrzymania czerwonego osadu (...)Osad odsącz, przemyj alkoholem i susz na bibule na powietrzu." |
W parownicy porcelanowej, w której znajduje się 2,5 g naftalenu, umieść krążek bibuły z niewielkimi otworami oraz odwrócony lejek szklany. Zatyczkę lejka zrób z korka z waty. Parownicę umieść w płaszczu grzejnym. Po delikatnym ogrzaniu parownicy, pary substancji przechodzą przez otwory w bibule i kondensują na wewnętrznych ściankach lejka... Powyższy opis dotyczy metody oczyszczania naftalenu przez
Piktogram ukazujący czaszkę oraz skrzyżowane kości piszczelowe jest typowy dla substancji o działaniu
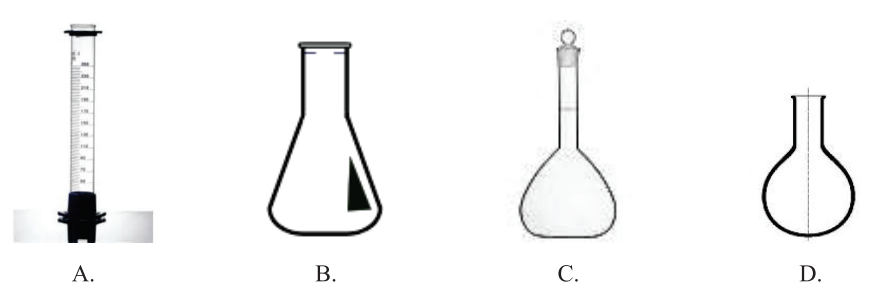
Laboratoryjny aparat szklany, który wykorzystuje kwasy do wytwarzania gazów w reakcji z metalem lub odpowiednią solą, to
Sporządzono 250 cm3 roztworu glicerolu o gęstości 1,05 g/cm3 w temperaturze 20°C. Korzystając z danych zamieszczonych w tabeli, określ stężenie procentowe sporządzonego roztworu glicerolu.
| Glicerolu [%] | 10% | 20% | 30% | 50% |
|---|---|---|---|---|
| d20 [g/dm3] | 1023,70 | 1048,40 | 1073,95 | 1127,20 |
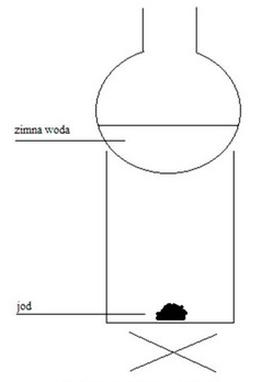
Na rysunku przedstawiono zestaw do oczyszczania jodu w procesie
Który z podanych związków chemicznych można wykorzystać do oceny całkowitego usunięcia jonów chlorkowych z osadu?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Instalacja, do której należy podłączyć palnik, powinna być pokryta farbą w kolorze
Reagenty o najwyższej czystości to reagenty
Etykiety chemikaliów zawierają zwroty H, które informują o rodzaju zagrożenia. Cyfra "3" pojawiająca się po literze "H" w oznaczeniu, definiuje rodzaj zagrożenia?
Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Kalibracja pH-metru nie jest potrzebna po
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
Jakie jest stężenie procentowe roztworu uzyskanego poprzez rozpuszczenie 25 g jodku potasu w 100 cm3 destylowanej wody (o gęstości 1 g/cm3)?
Transformacja zolu w żel to zjawisko określane jako
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
Jakim kolorem zazwyczaj oznacza się przewody w instalacji gazowej w laboratorium?
Który z procesów jest endotermiczny?
Do rozpuszczania próbek wykorzystuje się wodę królewską, która stanowi mieszaninę stężonych kwasów
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Połączono równe ilości cynku i bromu, a następnie poddano je reakcji Zn + Br2 → ZnBr2. W tych warunkach stopień reakcji cynku wynosi (masy atomowe: Zn – 65u, Br – 80u)?
Dokonano pomiaru pH dwóch roztworów, uzyskując wartości pH= 2 oraz pH= 5. Wskaźnij poprawnie sformułowany wniosek.
Jakie urządzenie laboratoryjne jest używane do realizacji procesu ekstrakcji?
Próbka, którą analizujemy, to bardzo rozcieńczony wodny roztwór soli nieorganicznych, który ma być poddany analizie. Proces, który można zastosować do zagęszczenia tego roztworu, to
Temperatura wrzenia aniliny przy normalnym ciśnieniu wynosi 457,13 K. W trakcie jej oczyszczania metodą destylacji prostej pod ciśnieniem atmosferycznym należy zebrać frakcję wrzącą w przedziale temperatur
Reagent, który reaguje wyłącznie z jednym konkretnym jonem lub związkiem, nazywamy reagente
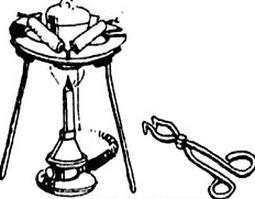
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
Czy próbkę laboratoryjną przechowuje się w lodówce, gdy występuje w niej
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Ilustracja przedstawia fragment szklanej pipety wielomiarowej

W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?
Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Działanie podejmowane po pobraniu próbki wody, mające na celu zachowanie jej składu chemicznego podczas transportu, określa się mianem
Transportuje się pobrane próbki wody do analiz fizykochemicznych
Przyrząd przedstawiony na rysunku służy do pobierania próbek substancji
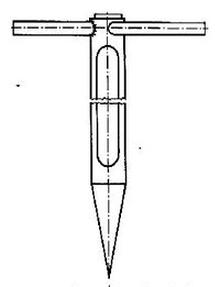
W celu przygotowania roztworu mianowanego należy użyć sprzętu przedstawionego na rysunku