Pytanie 1
Odprowadzenie II rejestruje różnicę potencjałów między
Wynik: 15/40 punktów (37,5%)
Wymagane minimum: 20 punktów (50%)
Odprowadzenie II rejestruje różnicę potencjałów między
Wskazaniem do wykonania przesiewowego badania densytometrycznego jest
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Badanie gęstości mineralnej kości metodą DXA należy wykonać
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
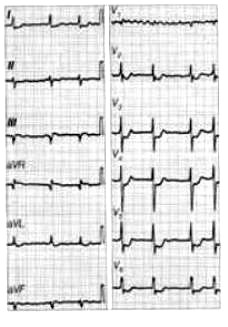
Który zapis EKG przedstawia falę Pardee'go?
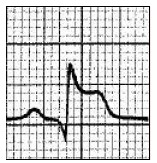
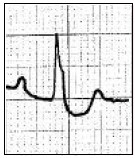
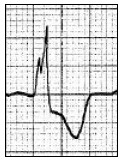

Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Badanie metodą Dopplera umożliwia
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
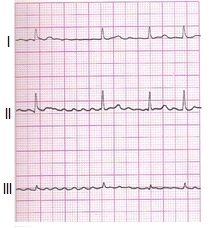
Który z nowotworów jest hormonozależny?
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Największa wartość energii promieniowania stosowanego w radioterapii jest generowana przy użyciu
W badaniu cystografii wstępującej środek kontrastowy należy podać
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
Promieniowanie rentgenowskie jest
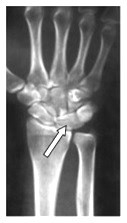
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Na elektrokardiogramie uwidoczniono
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
W ultrasonografii występuje zależność:
Warstwa półchłonna (WP) służy do obliczania
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
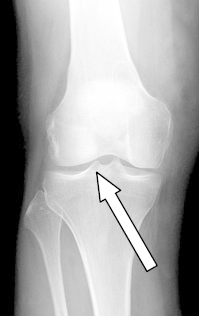
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
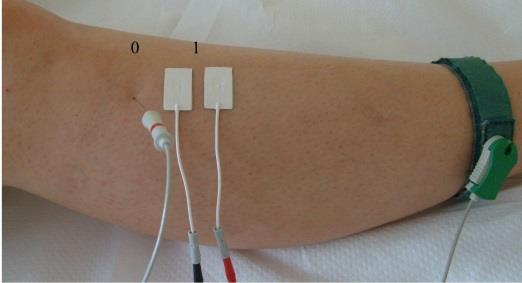
Na ilustracji przedstawiono przygotowanie pacjenta do badania
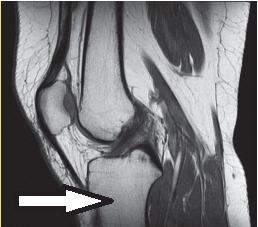
Którą kość oznaczono na obrazie rezonansu magnetycznego?
Jak przebiega promień centralny w projekcji AP czaszki?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Na zamieszczonym radiogramie strzałką oznaczono kość
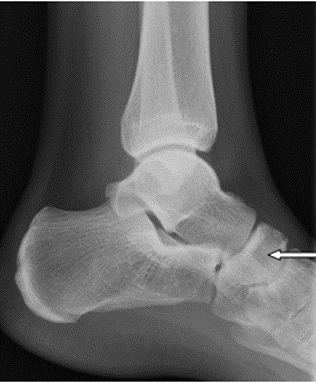
Na rentgenogramie strzałką zaznaczono
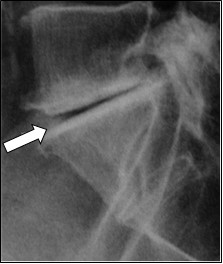
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
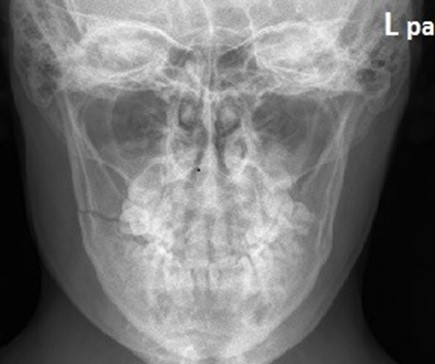
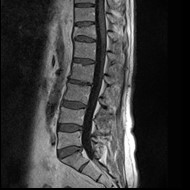
Na obrazie uwidoczniono złamanie kompresyjne kręgu
Przy podejrzeniu ciała obcego w oczodole należy wykonać
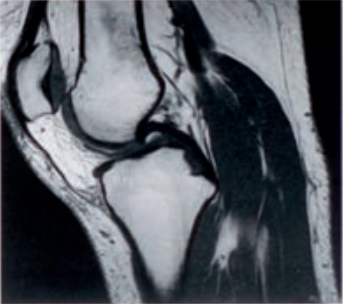
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest