Pytanie 1
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Skrótem CTV w radioterapii oznacza się
Pojawienie się w zapisie EKG patologicznego załamka Q lub QS może wskazywać na
Na ilustracji przedstawiono zjawisko
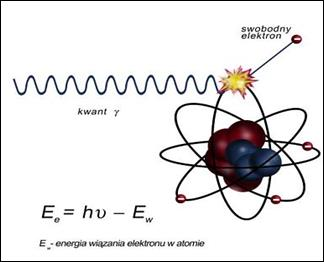
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
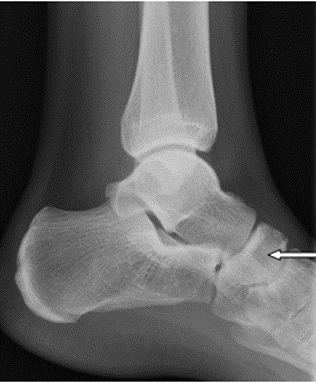
Na zamieszczonym radiogramie strzałką oznaczono kość
Na schemacie oznaczono
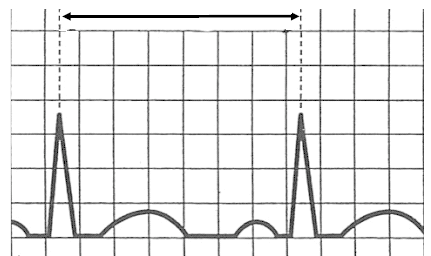
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
W badaniu EKG elektrodę przedsercową V4 należy umocować
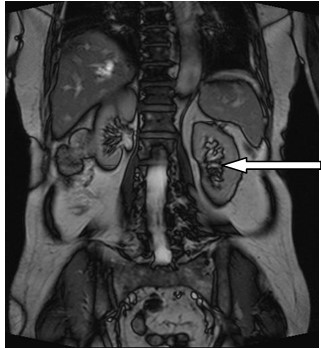
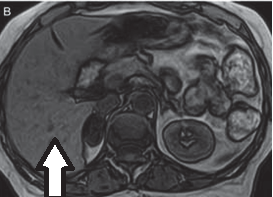
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
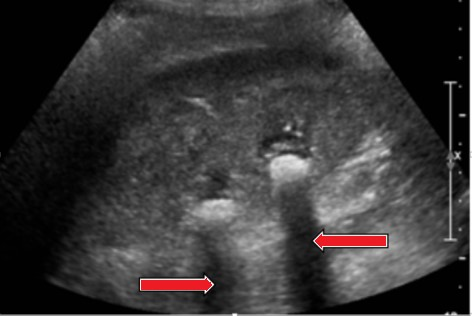
Który artefakt wskazano strzałkami na obrazie USG nerki?
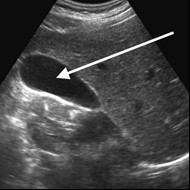
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
W jakich jednostkach mierzy się natężenie dźwięku?
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
Promieniowanie jonizujące pośrednio to
W leczeniu izotopowym tarczycy podaje się
W zapisie EKG załamek U występuje bezpośrednio po załamku
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Wskazaniem do wykonania badania spirometrycznego jest
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
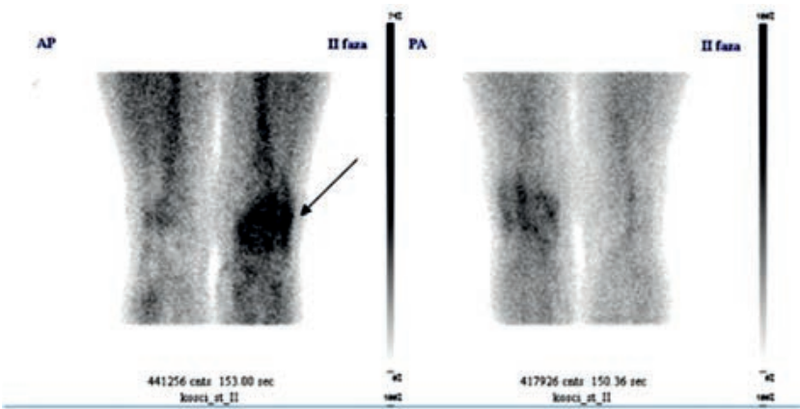
Na przedstawionym scyntygramie ukazano duży obszar
Diagnozowanie metodą PET oparte jest na zjawisku
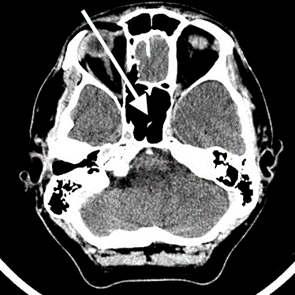
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
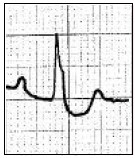
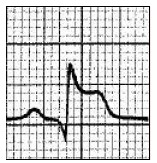
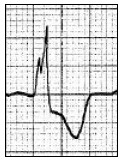
Który zapis EKG przedstawia falę Pardee'go?

Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
Zdjęcie zatok przynosowych wykonuje się w pozycji
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
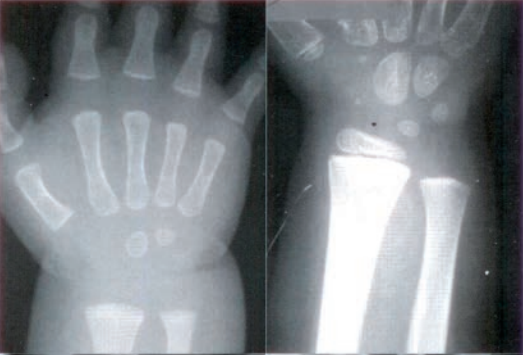
Zestaw rentgenogramów przedstawia
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Wskazaniem do wykonania badania spirometrycznego jest
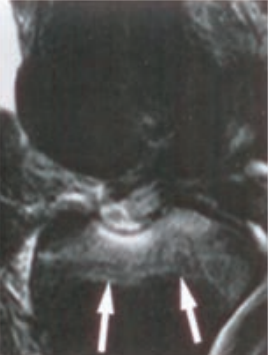
Obraz stawu kolanowego otrzymano metodą
Który obszar napromieniania wskazano na ilustracji strzałką?