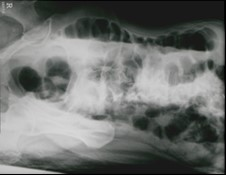
Pytanie 1
Radiogram przedstawia
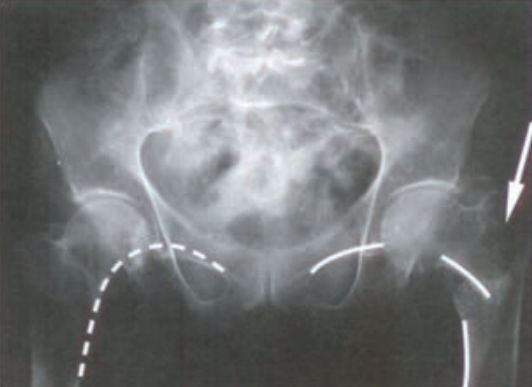
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Radiogram przedstawia

Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
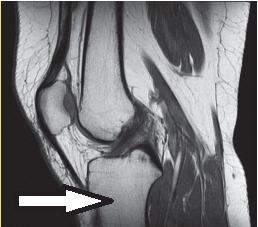
Na zamieszczonym radiogramie strzałką oznaczono kość
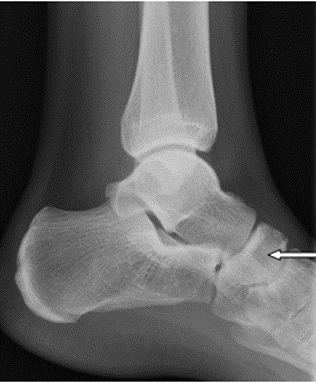
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
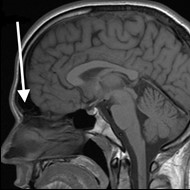
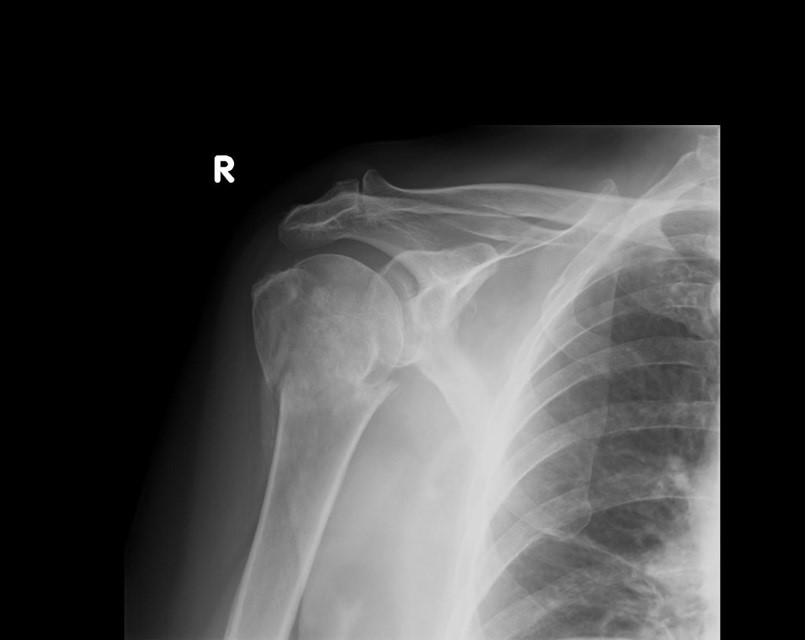
Na radiogramie uwidoczniono
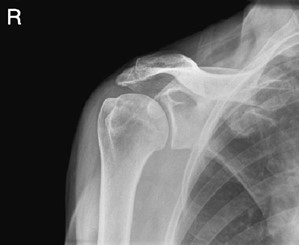
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
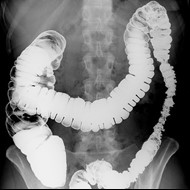
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
W obrazowaniu MR wykorzystuje się moment magnetyczny
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Na radiogramie uwidoczniono
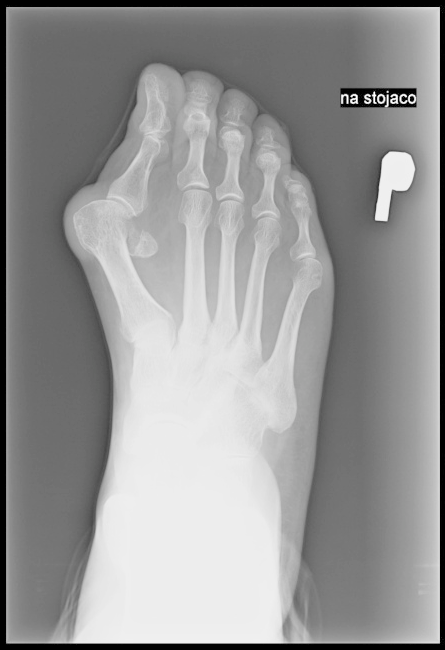
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
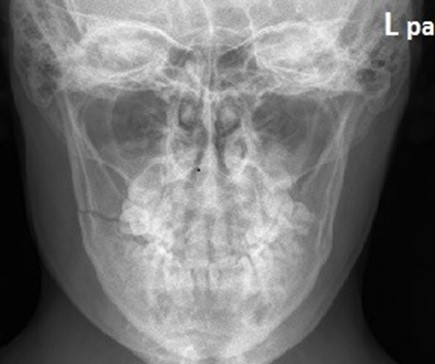
Którą kość oznaczono na obrazie rezonansu magnetycznego?
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
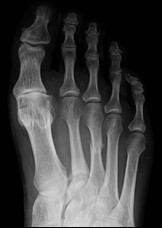
Na radiogramie stopy uwidocznione jest złamanie trzonu
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
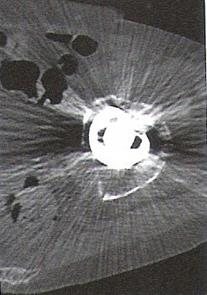
Zarejestrowany na obrazie TK artefakt jest spowodowany
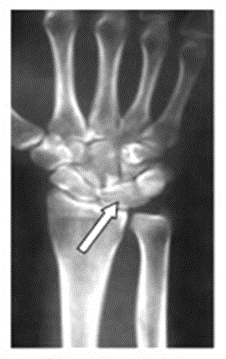
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
Fistulografia to badanie kontrastowe
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
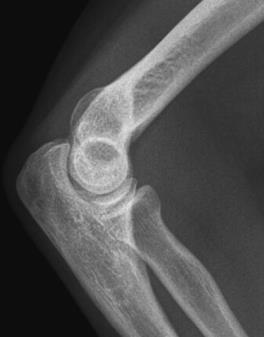
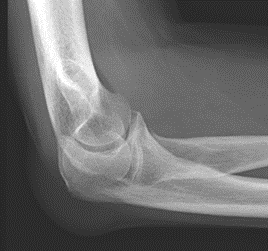
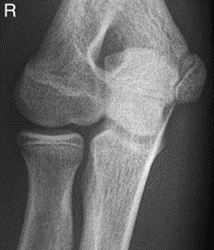
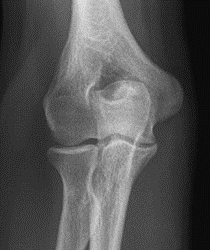
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Ligand stosuje się
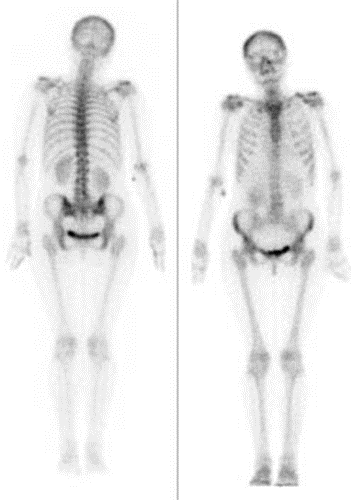
Przedstawiony obraz został zarejestrowany podczas wykonania
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
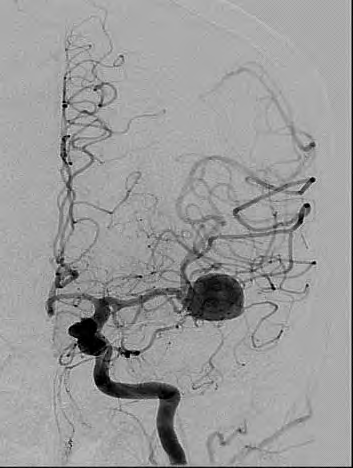
Którą patologię uwidoczniono w badaniu angiograficznym?
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Na radiogramie uwidoczniono złamanie
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
W radiografii mianem SID określa się
Które badanie zostało zarejestrowane na przedstawionym radiogramie?