Pytanie 1
Substancje chemiczne, które zazwyczaj wykorzystuje się w eksperymentach preparatywnych oraz w jakościowych analizach, charakteryzujące się czystością w przedziale 99-99,9%, nazywa się
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Substancje chemiczne, które zazwyczaj wykorzystuje się w eksperymentach preparatywnych oraz w jakościowych analizach, charakteryzujące się czystością w przedziale 99-99,9%, nazywa się
Korzystając z wykresu określ, w jakiej temperaturze należy rozpuszczać azotan(V) potasu, aby całkowicie rozpuścić 110 g soli w 100 g wody.
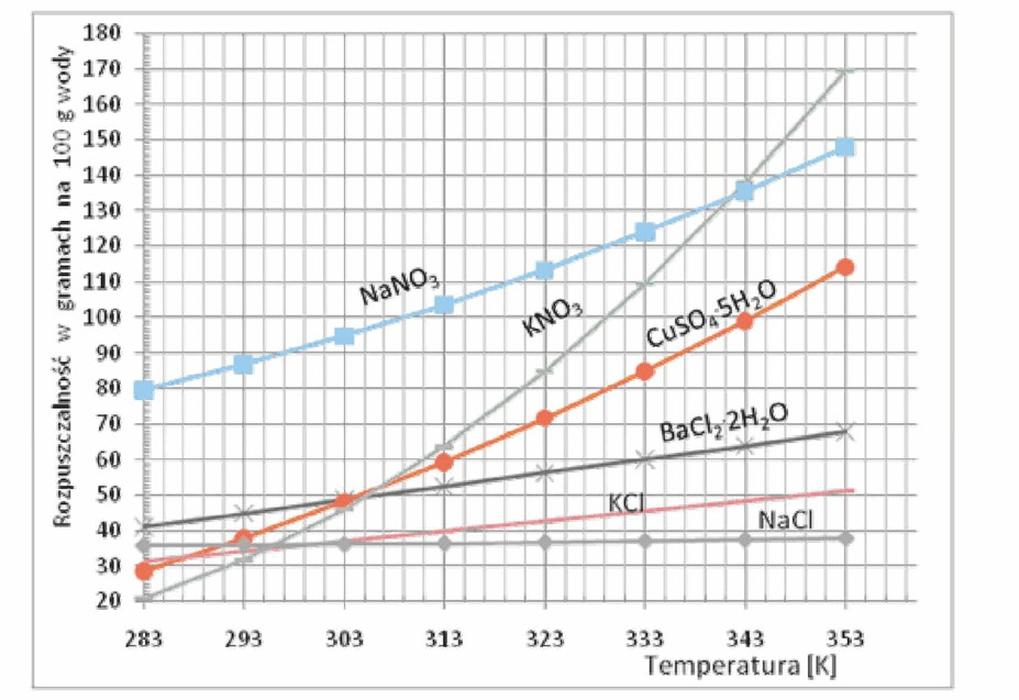
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Laboratoryjna apteczka powinna zawierać m.in.
Osoba pracująca z lotnym rozpuszczalnikiem straciła przytomność. Jakie działania należy podjąć, aby udzielić pierwszej pomocy?
Mając wagę laboratoryjną z dokładnością pomiaru 10 mg, nie da się wykonać odważki o masie
Przedstawiono wyciąg z karty charakterystyki substancji chemicznej. Na podstawie informacji zawartej w zamieszczonym fragmencie karty wskaż wzór chemiczny substancji, której można użyć jako materiału neutralizującego lodowaty kwas octowy.
Kwas octowy lodowaty 99,5% Materiały zapobiegające rozprzestrzenianiu się skażenia i służące do usuwania skażenia Jeżeli to możliwe i bezpieczne, zlikwidować lub ograniczyć wyciek (uszczelnić, zamknąć dopływ cieczy, uszkodzone opakowanie umieścić w opakowaniu awaryjnym). Ograniczyć rozprzestrzenianie się rozlewiska przez obwałowanie terenu; zebrane duże ilości cieczy odpompować. Małe ilości rozlanej cieczy przysypać niepalnym materiałem chłonnym (ziemia, piasek oraz materiałami neutralizującymi kwasy, np. węglanem wapnia lub sodu, zmielonym wapieniem, dolomitem), zebrać do zamykanego pojemnika i przekazać do zniszczenia. Zanieczyszczoną powierzchnię spłukać wodą. Popłuczyny zebrać i usunąć jako odpad niebezpieczny. |
Którego odczynnika należy użyć do przygotowania roztworu wzorcowego, zawierającego jony \( \text{Fe}^{3+} \)?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Dekantacja to metoda
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jaką substancję należy koniecznie oddać do utylizacji?
W jakim celu używa się kamyczków wrzenne w trakcie długotrwałego podgrzewania cieczy?
Próbka, której celem jest ustalenie poziomu składników, dla których oznaczenia przygotowane przez różne laboratoria są niezgodne, to próbka
Elementami brakującymi w zestawie przedstawionym na rysunku są
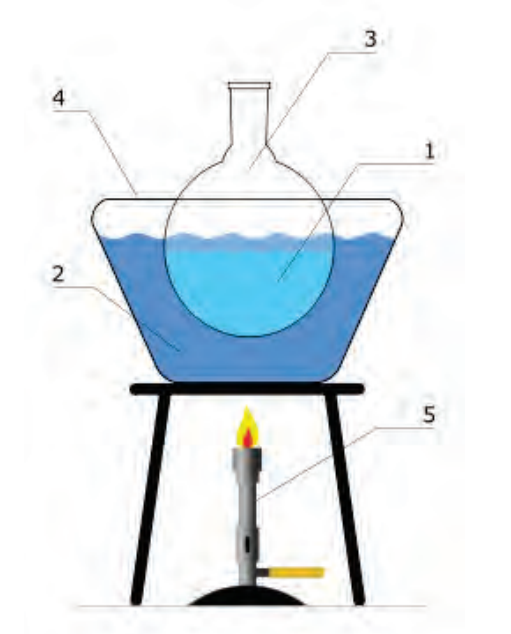
W celu przygotowania 100 cm3 roztworu mianowanego, jaką kolbę należy zastosować?
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie substancje są potrzebne do uzyskania nierozpuszczalnego wodorotlenku cynku?
Które równanie przedstawia reakcję otrzymywania mydła?
| CH3COOH + NaOH →CH3COONa + H2O | 2 CH3COOH + Na2O →2 CH3COONa + H2O | 2 C2H5COOH + 2 Na →2 C2H5COONa + H2↑ | C17H35COOH + NaOH →C17H35COONa + H2O |
W wyniku analizy sitowej próbki stałej otrzymano frakcję o średnicy ziaren 12 – 30 mm. Jaką masę powinna mieć prawidłowo pobrana próbka pierwotna?
| Tabela. Wielkość próbki pierwotnej w zależności od wielkości ziarna | ||||
|---|---|---|---|---|
| Średnica ziaren lub kawałków [mm] | do 1 | 1 - 10 | 11 - 50 | ponad 50 |
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Podczas pomiaru masy substancji w naczyniu wagowym na wadze technicznej, dla zrównoważenia masy na szalce zastosowano odważniki: 10 g, 5 g, 500 mg, 200 mg, 200 mg, 50 mg, 20 mg, 10 mg oraz 10 mg. Masa substancji razem z naczynkiem wyniosła
Skrót "cz." na etykiecie odczynnika chemicznego wskazuje, że
Który z procesów jest endotermiczny?
Proces oddzielania składników jednorodnej mieszaniny, polegający na eliminacji jednego lub większej ilości składników z roztworu lub substancji stałej przy użyciu odpowiednio wybranego rozpuszczalnika, to
Na podstawie informacji zawartych w tabeli, wskaż liczbę próbek pierwotnych, które należy pobrać z partii materiału o objętości \( 100 \, \text{m}^3 \).
Wzór: \( n = 0{,}5 \cdot \sqrt{V} \)
\( V \) – objętość jednostki pobierania \( \text{m}^3 \)
\( n \) – liczba miejsc pobieranych próbek pierwotnych
Wartość \( n \) zaokrągla się do liczby całkowitej.
Minimalna liczba miejsc poboru \( n = 12 \), maksymalna \( n = 30 \)
Aby oszacować czystość MgCO3, poddano prażeniu próbkę o wadze 5 g tej soli aż do osiągnięcia stałej masy. W trakcie prażenia zachodzi reakcja:
MgCO3 → MgO + CO2 Całkowity ubytek masy wyniósł 2,38 g.
(Masy molowe reagentów to: MgCO3 – 84 g/mol, MgO – 40 g/mol, CO2 – 44 g/mol) Jaką czystość miała próbka węglanu magnezu?
Roztwór zawierający 16,00 g siarczanu(VI) miedzi(II) nasycono siarkowodorem. Masa wytrąconego siarczku miedzi(II), po odsączeniu i wysuszeniu, wynosiła 8,64 g. Oblicz procentową wydajność tej reakcji.
Równanie reakcji:
\( \text{CuSO}_4 + \text{H}_2\text{S} \rightarrow \text{CuS} + \text{H}_2\text{SO}_4 \)
\( \text{M CuSO}_4 = 160 \, \text{g/mol} \)
\( \text{M CuS} = 96 \, \text{g/mol} \)
Jaką objętość powinna mieć kolba miarowa, aby przygotować mianowany roztwór NaOH o stężeniu 0,050 M z analitycznej odważki, która zawiera 0,1 mola NaOH?
Próbki wody, które mają być badane pod kątem zawartości krzemu, powinny być przechowywane w pojemnikach
Zgłębniki o konstrukcji przypominającej świder są wykorzystywane do pobierania próbek różnych materiałów
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na podstawie danych zawartych w tabeli wskaż, które opakowania zawierają produkt zgodny ze specyfikacją.
| WŁAŚCIWOŚCI | NORMA KLASY A wg specyfikacji produktu | OPAKOWANIE | ||
|---|---|---|---|---|
| 1 | 2 | 3 | ||
| POSTAĆ | Bezbarwna ciecz, bez zanieczyszczeń. Dopuszcza się niebieskawе zabаrwienie i obecność skrystalizowanego osadu | Bezbarwna ciecz | ||
| Zawartość ługu sodowego (NaOH), min, % masy | 46,0 | 46,5 | 46,8 | 48,0 |
| Węglan sodu (Na₂CO₃), nie więcej niż, % masy | 0,4 | 0,3 | 0,3 | 0,2 |
| Chlorek sodu (NaCl), nie więcej niż, % masy | 0,020 | 0,015 | 0,014 | 0,011 |
| Chloran sodu (NaClO₃), nie więcej niż, % masy | 0,007 | 0,006 | 0,005 | 0,002 |
| Siarczan sodu (Na₂SO₄), nie więcej niż, % masy | 0,040 | 0,038 | 0,035 | 0,029 |
| Zawartość żelaza (Fe₂O₃), max, WT. PPM | 15 | 15 | 15 | 10 |
Przedstawiony sprzęt szklany to
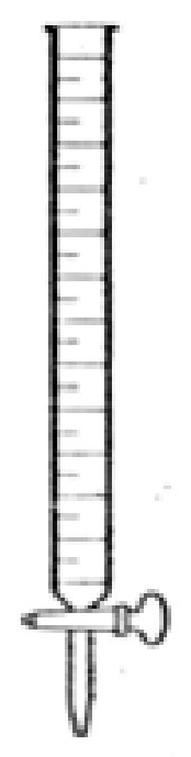
Którą substancję można bezpośrednio wyrzucić do odpadów komunalnych?
Jak definiuje się próbkę wzorcową?
Jakie jest przeznaczenie pieca muflowego?
Aparat przedstawiony na ilustracji służy do
