Pytanie 1
W radiografii mianem SID określa się
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
W radiografii mianem SID określa się
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
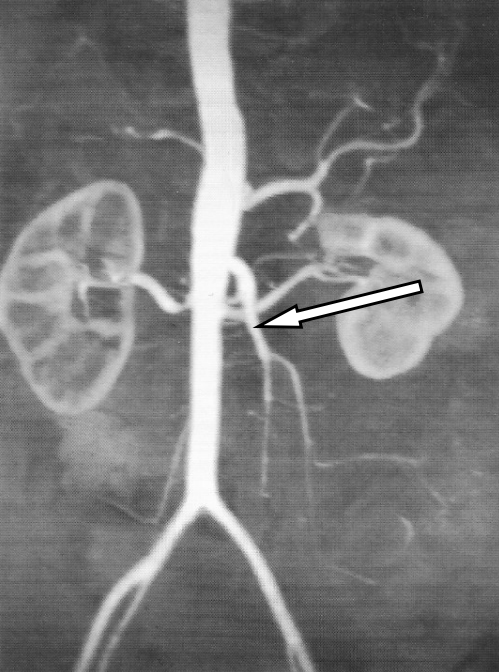
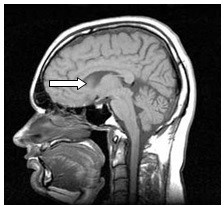
Którą tętnicę zaznaczono strzałką na obrazie MR?
Największa wartość energii promieniowania stosowanego w radioterapii jest generowana przy użyciu
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Promieniowanie rentgenowskie jest
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
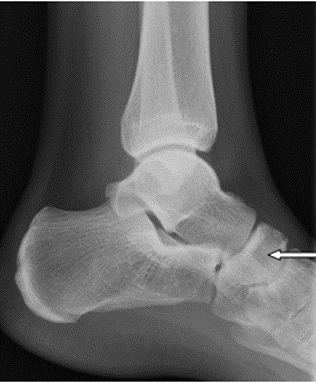
Na zamieszczonym radiogramie strzałką oznaczono kość
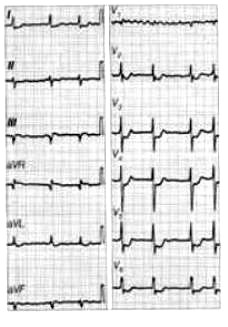
Na elektrokardiogramie uwidoczniono
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
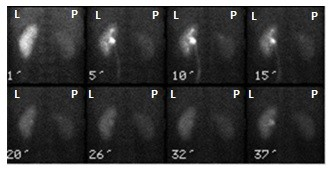
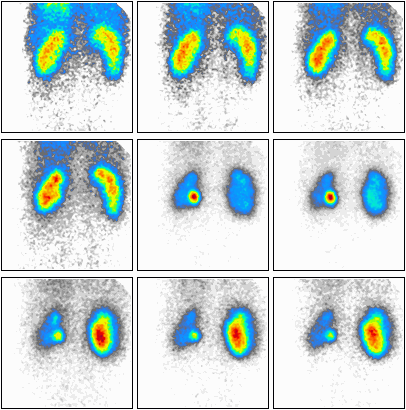
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Jednostką indukcji magnetycznej jest
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
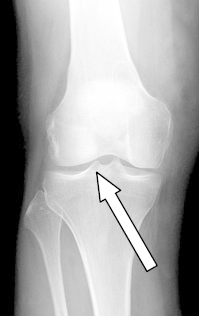
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W radioterapii konwencjonalnej pacjent jest leczony promieniowaniem pochodzącym
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
W medycynie nuklearnej wykorzystuje się:
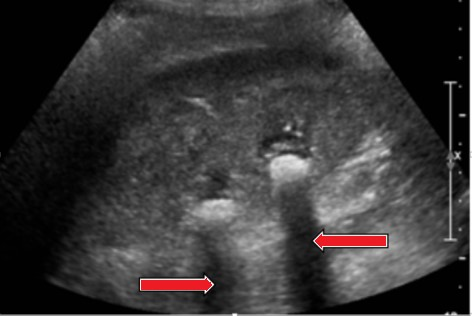
Który artefakt wskazano strzałkami na obrazie USG nerki?
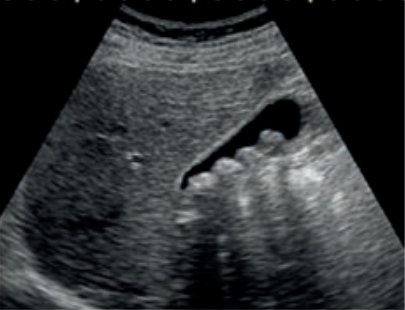
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Pojawienie się w zapisie EKG patologicznego załamka Q lub QS może wskazywać na
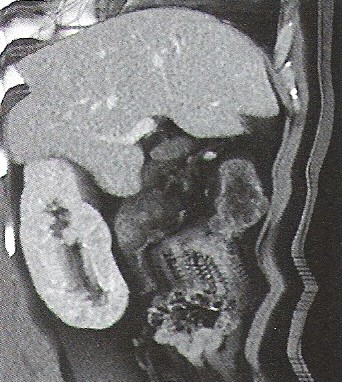
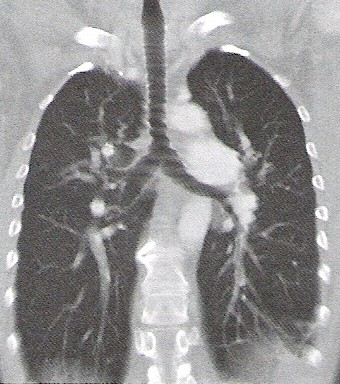
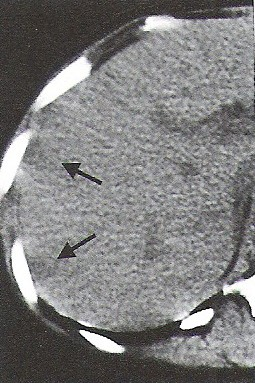
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

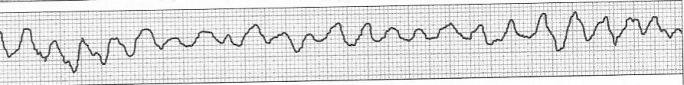
Zamieszczony elektrokardiogram przedstawia
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Badanie gęstości mineralnej kości metodą DXA należy wykonać
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
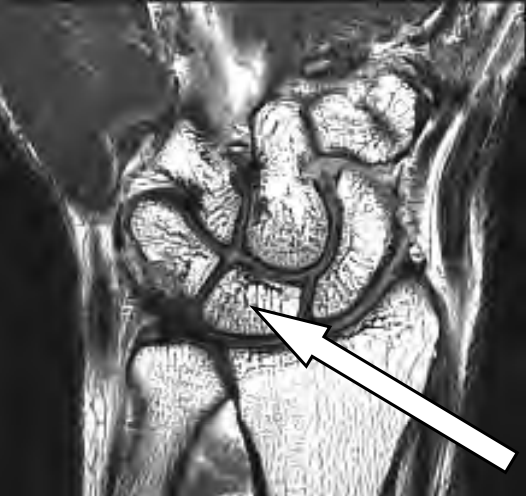
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
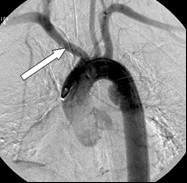
Na obrazie cyfrowej angiografii subtrakcyjnej strzałką zaznaczono
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to