Pytanie 1
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Wynik: 20/40 punktów (50,0%)
Wymagane minimum: 20 punktów (50%)
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
W badaniu cystografii wstępującej środek kontrastowy należy podać
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Do wczesnych odczynów popromiennych po radioterapii zalicza się
Cholangiografia to badanie radiologiczne
Na wykresie EKG zaznaczono
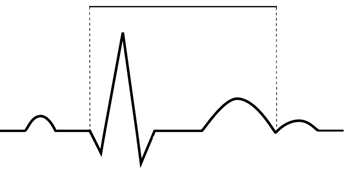
Na schemacie oznaczono
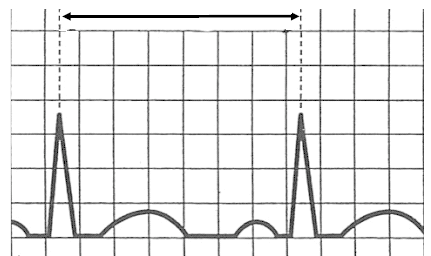
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
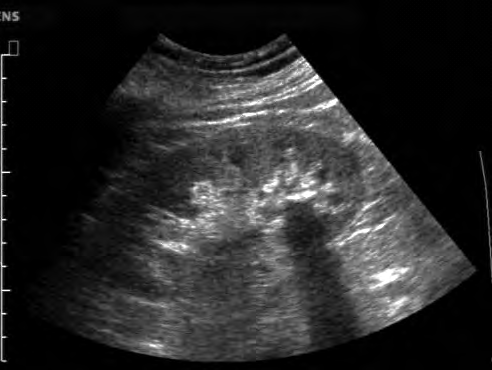
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
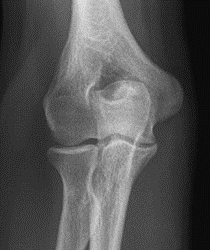
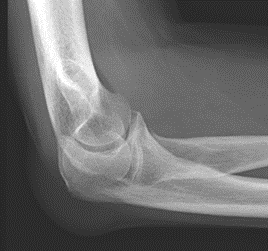
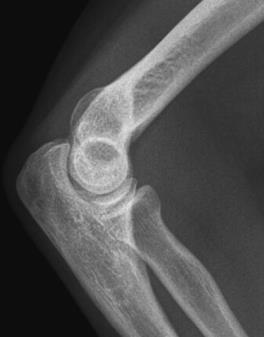
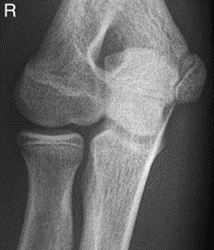
Celem radioterapii paliatywnej nie jest
Więzka promieniowania X to
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
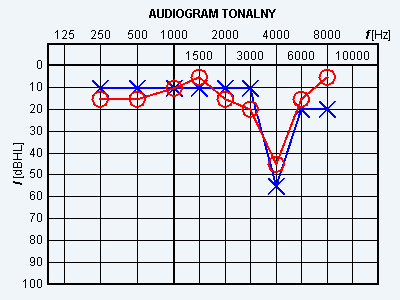
Przyczyną zaniku kostnego jest
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Do wykonania stomatologicznego zdjęcia rentgenowskiego techniką kąta prostego promień centralny należy ustawić prostopadle do
Na radiogramie uwidoczniono złamanie
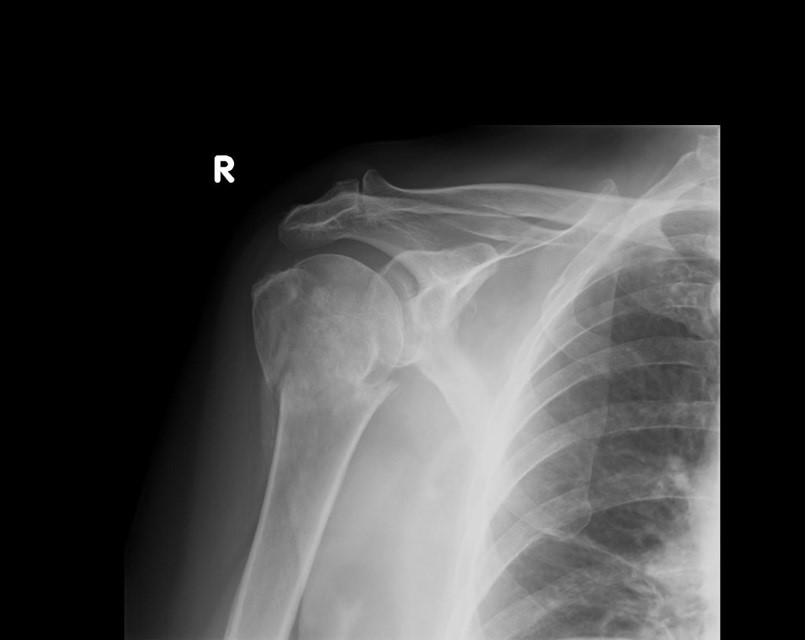
Radiogram przedstawia
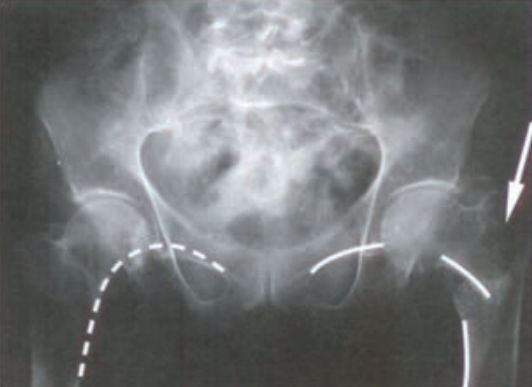
Limfografia to badanie kontrastowe
Audiometria impedancyjna polega na pomiarze
Czas połowicznego zaniku jest wykorzystywany
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
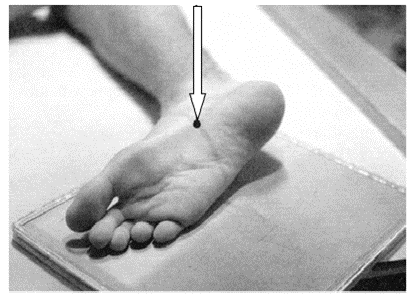
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Pielografia zstępująca umożliwia diagnostykę
Chorobą układu oddechowego typu obturacyjnego jest
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
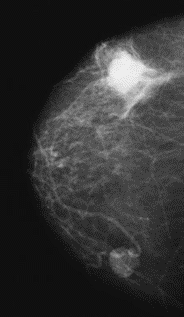
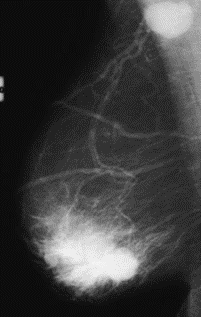
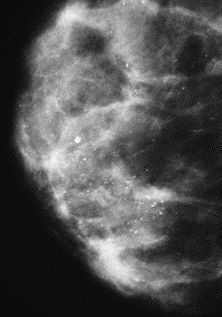
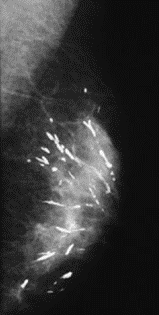
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem