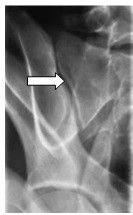
Pytanie 1
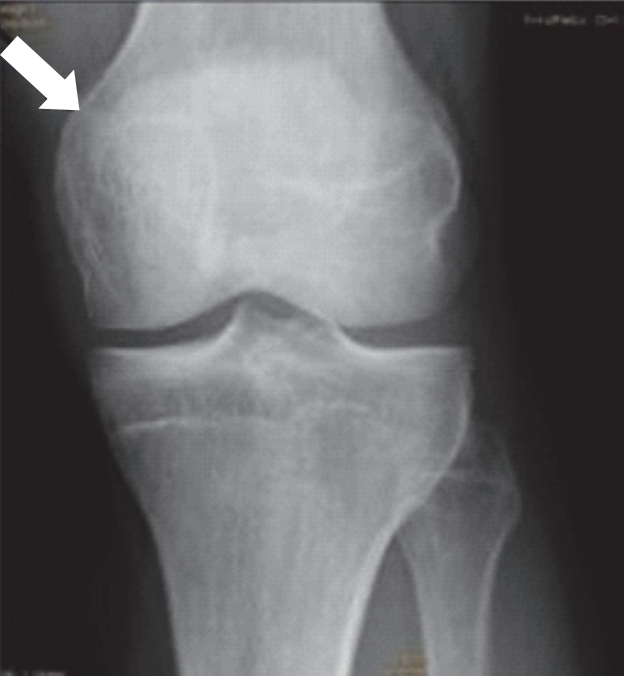
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?

Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
Wskazaniem do wykonania badania spirometrycznego jest
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
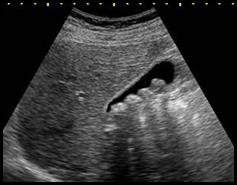
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
Przy podejrzeniu ciała obcego w oczodole należy wykonać
Chorobą układu oddechowego typu obturacyjnego jest
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
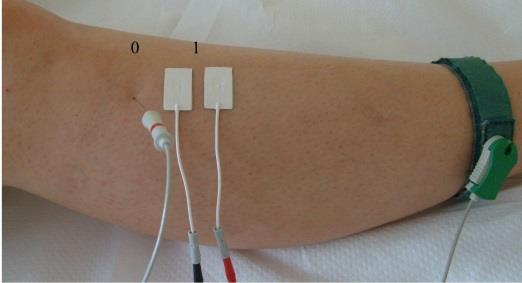
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
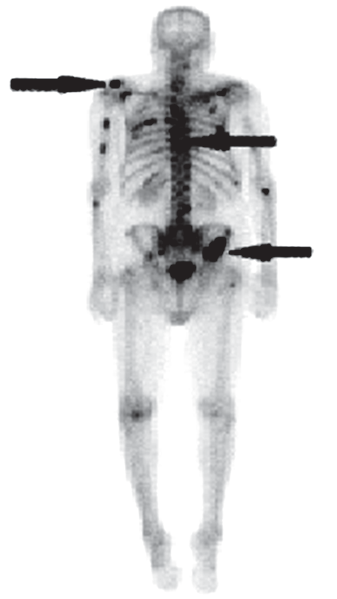
Na scyntygramie kości strzałkami oznaczono ogniska
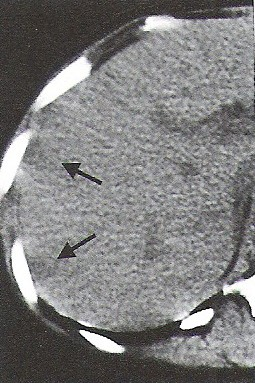
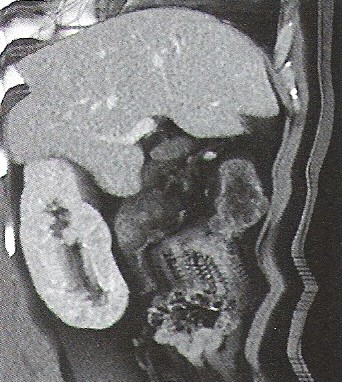
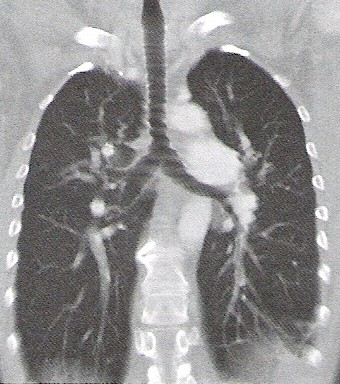
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

Do środków kontrastujących negatywnych należą
Na zamieszczonej rycinie przedstawiono
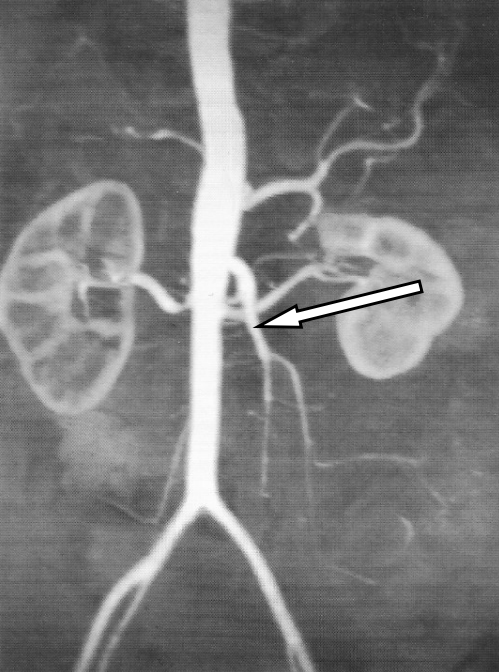
Którą tętnicę zaznaczono strzałką na obrazie MR?
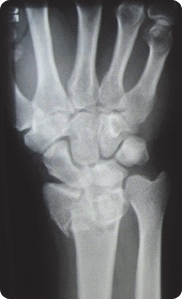
Na radiogramie uwidoczniono złamanie nasady
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
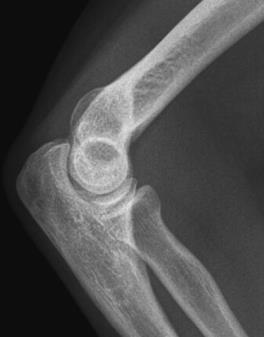
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
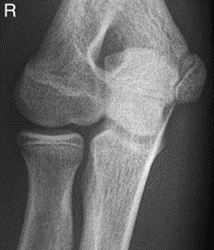
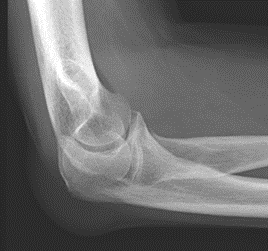
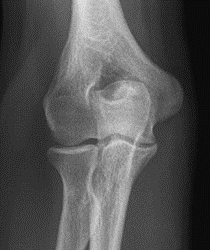
W brachyterapii MDR stosowane są dawki promieniowania
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Zdjęcie zatok przynosowych wykonuje się w pozycji
Badanie gęstości mineralnej kości metodą DXA należy wykonać
W badaniu audiometrycznym do oceny przewodnictwa kostnego wybranego ucha słuchawkę kostną należy przyłożyć do
Na radiogramie TK głowy strzałką wskazano
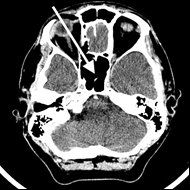
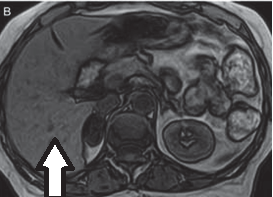
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
Wyniosłość międzykłykciowa znajduje się na nasadzie
Szczytowy przepływ wydechowy zarejestrowany w trakcie badania maksymalnie natężonego wydechu jest oznaczany skrótem
Które czynności wykonuje technik elektroradiolog w pracowni „gorącej”?
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?