Pytanie 1
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
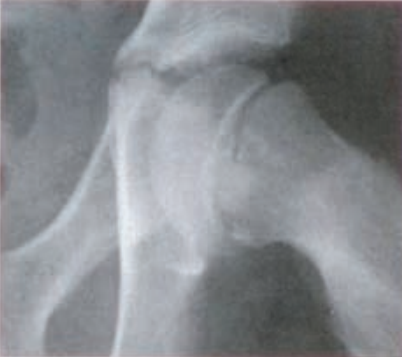
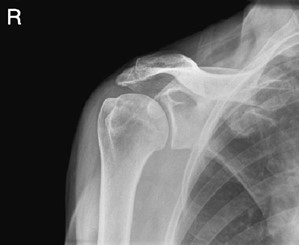
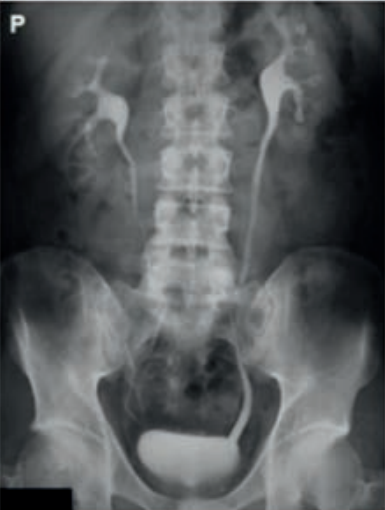
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
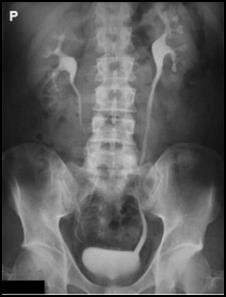
Przedstawiony obraz został zarejestrowany podczas wykonania
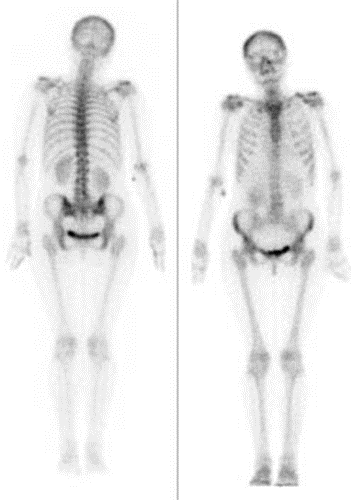
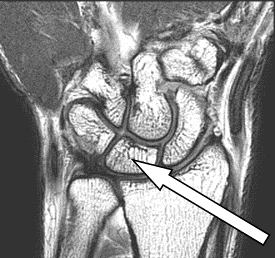
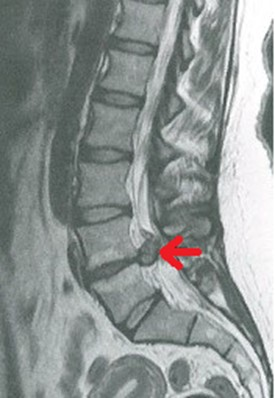
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
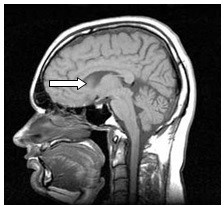
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
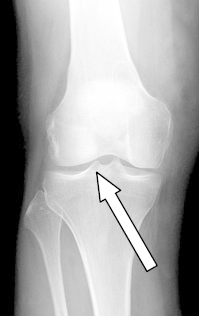
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
Jednostką indukcji magnetycznej jest
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
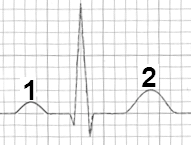
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Na radiogramie uwidoczniono
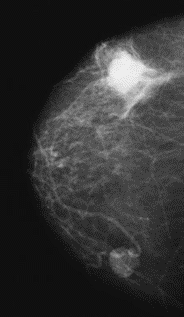
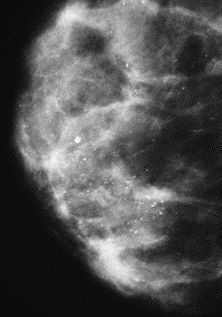
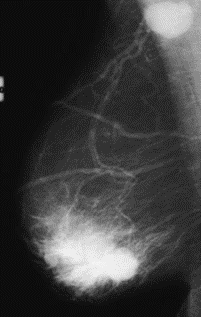
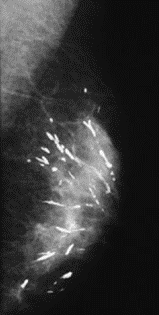
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
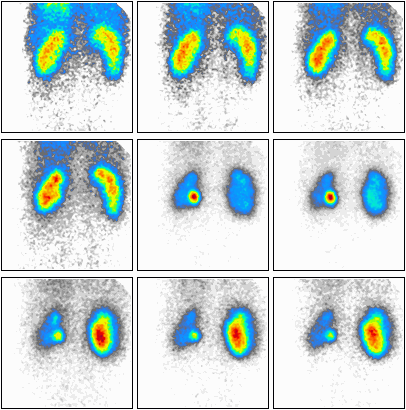
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
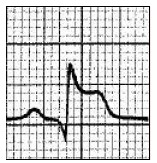
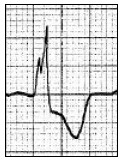
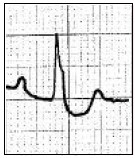
Który zapis EKG przedstawia falę Pardee'go?

Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Fotostymulacja wykonywana jest podczas badania
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Na rentgenogramie uwidoczniono badanie
W zapisie EKG zespół QRS odzwierciedla
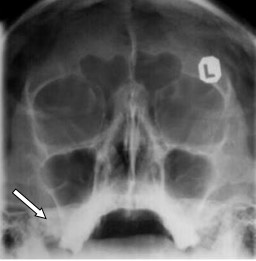
Zdjęcie zatok przynosowych wykonuje się w pozycji
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
Na schemacie oznaczono
Cholangiografia to badanie radiologiczne
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
Szczytowy przepływ wydechowy zarejestrowany w trakcie badania maksymalnie natężonego wydechu jest oznaczany skrótem
Na radiogramie czaszki strzałką zaznaczono
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Do środków kontrastujących negatywnych należą
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy