Pytanie 1
Przedstawiony obraz został zarejestrowany podczas wykonania
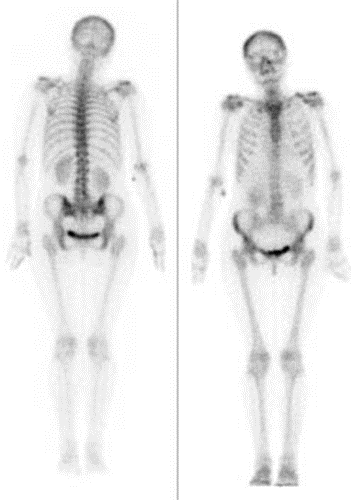
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Przedstawiony obraz został zarejestrowany podczas wykonania

Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
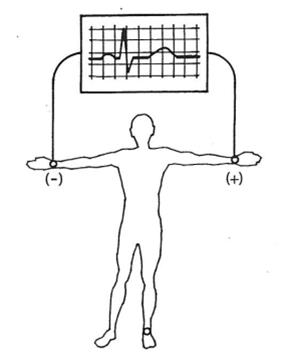
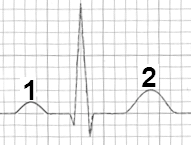
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
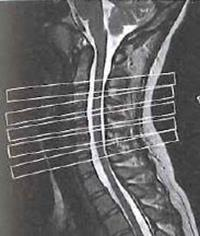
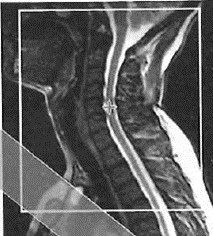
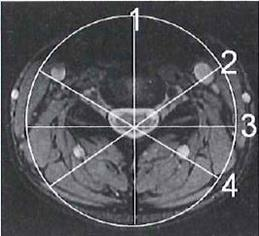
Na którym obrazie MR jest widoczne pasmo saturacji?

Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
W medycynie nuklearnej wykorzystuje się:
Technika stereotaktyczna polega na napromienianiu nowotworu
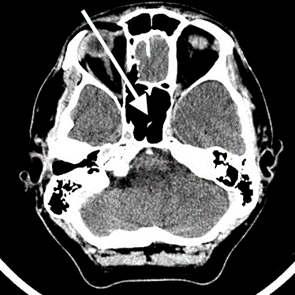
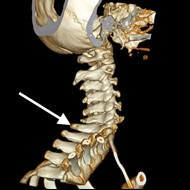
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Teleterapia polega na napromienowaniu
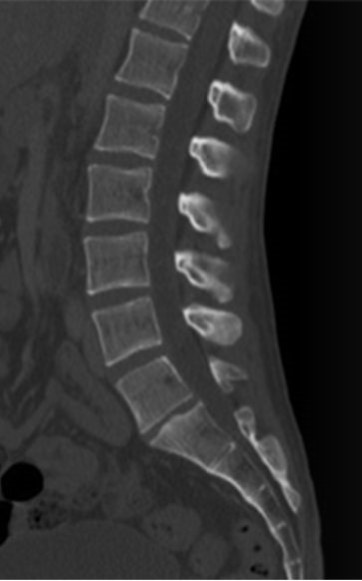
Którą metodą zostało wykonane badanie kręgosłupa zobrazowane na zdjęciu?
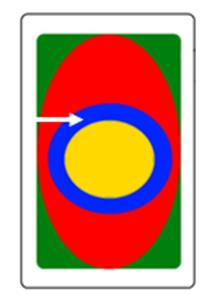
Który obszar napromieniania wskazano na ilustracji strzałką?
Technik elektroradiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta:
Cholangiografia to badanie radiologiczne
Na schemacie oznaczono
Czym charakteryzuje się późny odczyn popromienny?
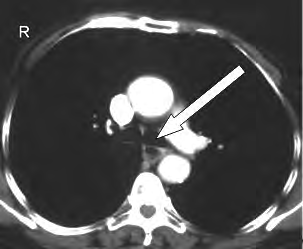
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
DSA to cyfrowa
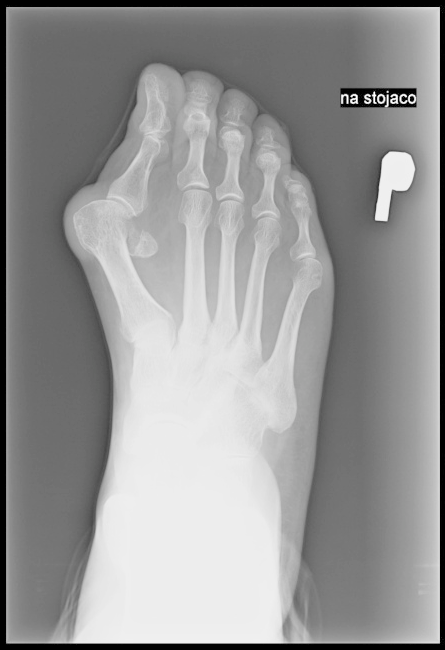
Na radiogramie uwidoczniono
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
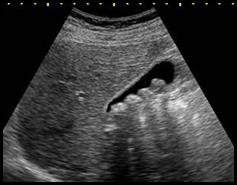
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
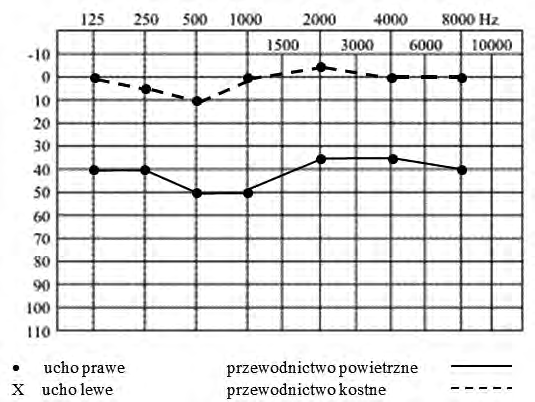
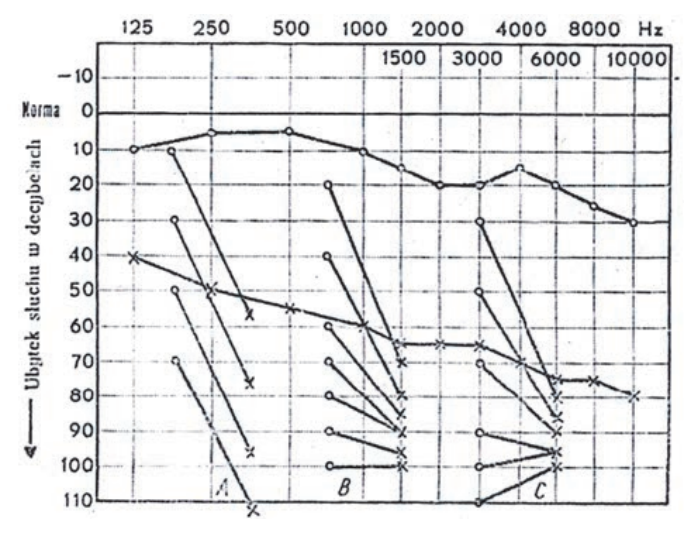
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
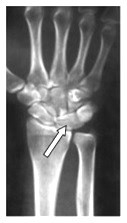
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Jakie wymagania techniczne muszą spełniać aparaty terapeutyczne stosowane w zakładach brachyterapii, służące bezpośrednio do napromieniania pacjenta metodą zdalnego wprowadzania źródeł promieniotwórczych?
W radioterapii konwencjonalnej pacjent jest leczony promieniowaniem pochodzącym
Fala głosowa rozchodzi się
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Audiogram przedstawia próbę
Więzka promieniowania X to
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
Ligand stosuje się