Pytanie 1
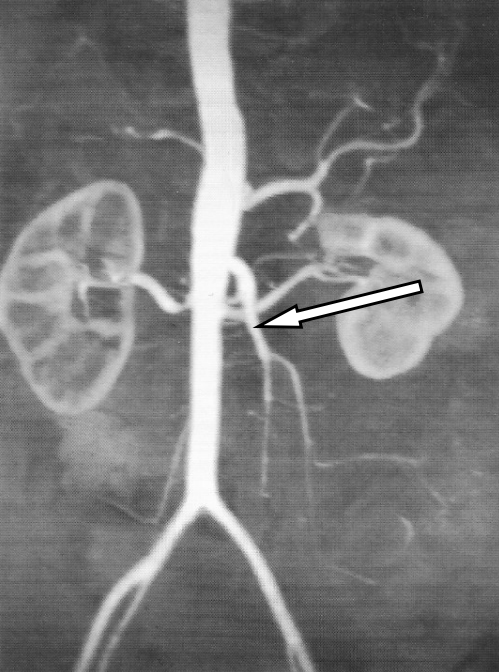
Którą tętnicę zaznaczono strzałką na obrazie MR?
Wynik: 39/40 punktów (97,5%)
Wymagane minimum: 20 punktów (50%)
Którą tętnicę zaznaczono strzałką na obrazie MR?

Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
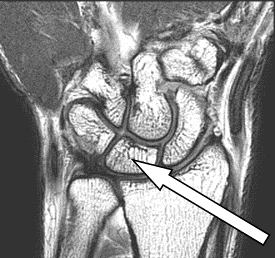
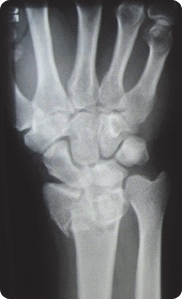
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
Objawem późnego odczynu popromiennego po teleradioterapii jest
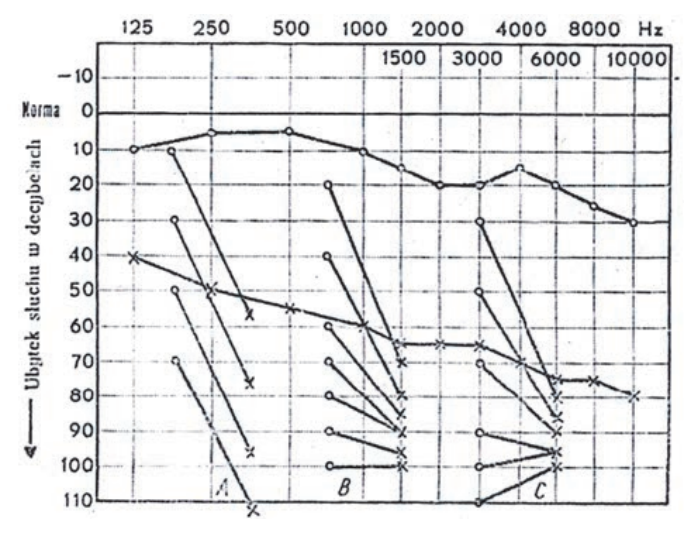
Audiogram przedstawia próbę
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu
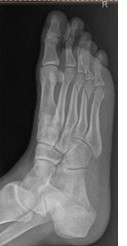
Na rentgenogramie stopy uwidocznione jest złamanie
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
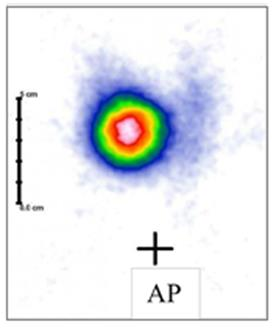
Na scyntygramie tarczycy uwidoczniono guzek
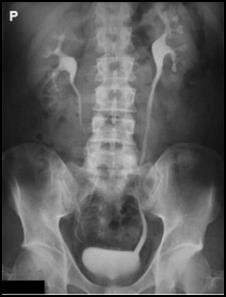
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Proces chemicznego wywoływania radiogramów polega na
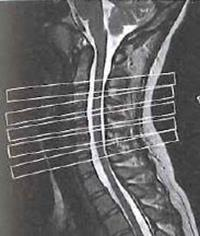
Na którym obrazie MR jest widoczne pasmo saturacji?
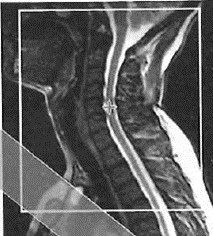

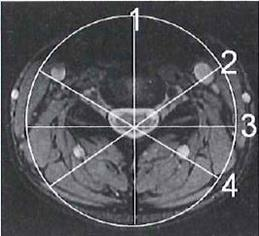
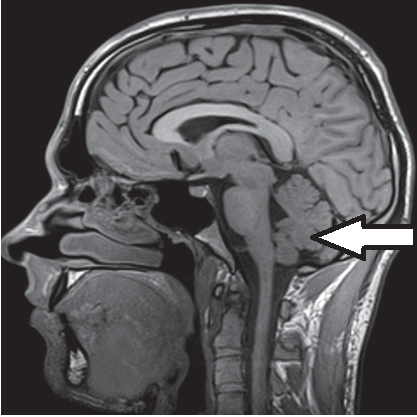
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
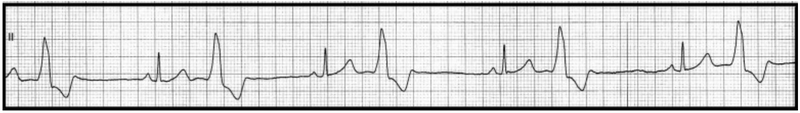
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
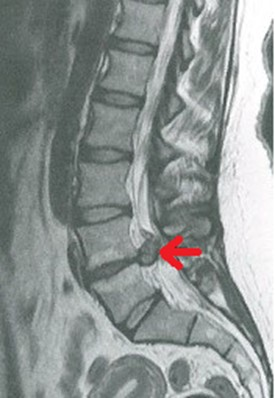
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
W zapisie EKG zespół QRS odzwierciedla
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
Ligand stosuje się
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
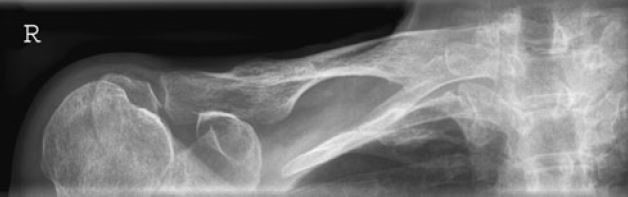
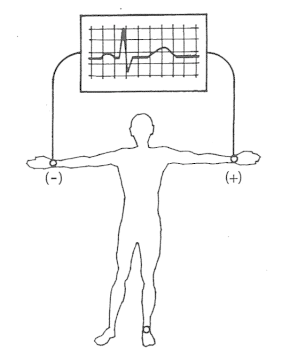
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
W której pozycji wykonuje się zdjęcie jamy brzusznej u pacjenta z podejrzeniem perforacji żołądka?
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Celem radioterapii paliatywnej nie jest
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
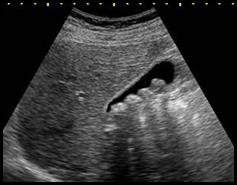
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
Do wczesnych odczynów popromiennych po radioterapii zalicza się
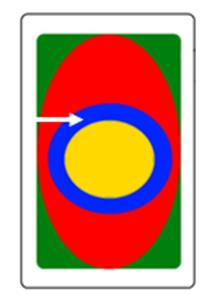
Który obszar napromieniania wskazano na ilustracji strzałką?
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
Czym charakteryzuje się późny odczyn popromienny?
Na radiogramie uwidoczniono złamanie nasady
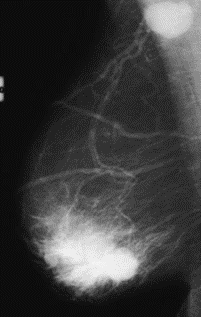
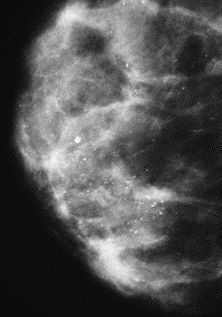
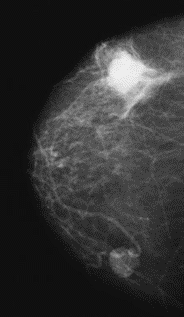
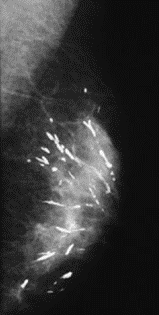
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?