Pytanie 1
Celem radioterapii paliatywnej nie jest
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Celem radioterapii paliatywnej nie jest
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
W radioterapii konwencjonalnej pacjent jest leczony promieniowaniem pochodzącym
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
Jaki jest cel stosowania bolusa w radioterapii?
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
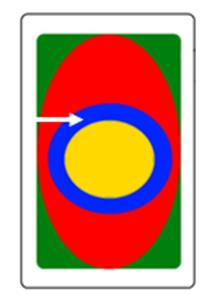
Który obszar napromieniania wskazano na ilustracji strzałką?
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
Warstwa półchłonna (WP) służy do obliczania
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Czym charakteryzuje się późny odczyn popromienny?
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Teleterapia polega na napromienowaniu
Do wczesnych odczynów popromiennych po radioterapii zalicza się
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Obrazowanie portalowe w radioterapii służy do
Promieniowanie jonizujące pośrednio to
Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
W brachyterapii MDR stosowane są dawki promieniowania
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie