Pytanie 1
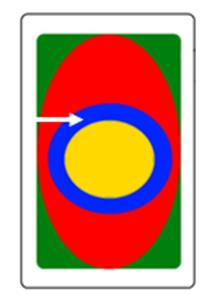
Który obszar napromieniania wskazano na ilustracji strzałką?
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Który obszar napromieniania wskazano na ilustracji strzałką?

Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
W brachyterapii MDR stosowane są dawki promieniowania
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Jakie źródła promieniowania stosowane są w brachyterapii?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Brachyterapia wewnątrzprzewodowa jest stosowana w leczeniu
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Celem radioterapii paliatywnej nie jest
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Rumień skóry pojawiający się podczas radioterapii jest objawem
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Skrótem CTV w radioterapii oznacza się
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Objawem późnego odczynu popromiennego po teleradioterapii jest
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Elementem pomocniczym w radioterapii, zapewniającym powtarzalność ułożenia w pozycji terapeutycznej, a także unieruchomienie pacjenta, jest
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
Planowany obszar napromieniania PTV obejmuje
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Teleterapia polega na napromienowaniu
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Czym charakteryzuje się późny odczyn popromienny?
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
Obrazowanie portalowe w radioterapii służy do
Promieniowanie jonizujące pośrednio to
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę