Pytanie 1
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
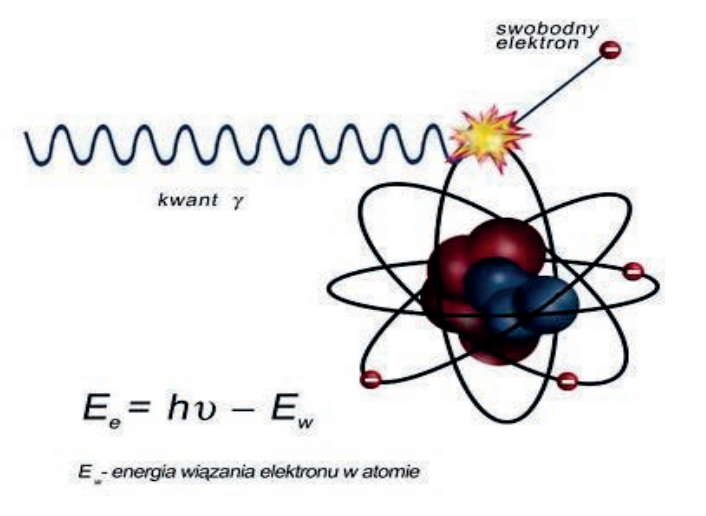
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
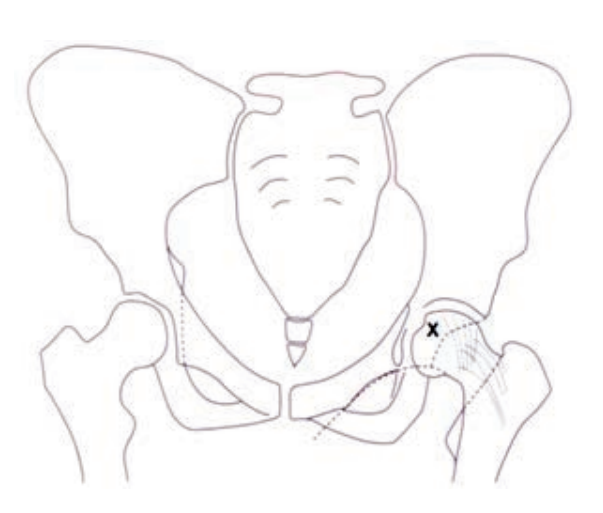
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
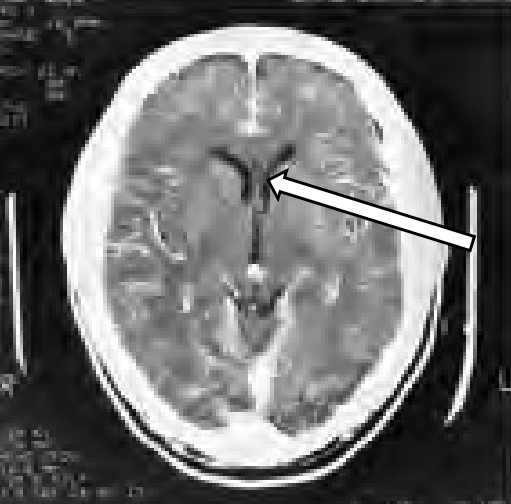
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Który artefakt uwidoczniono na skanie RM głowy?
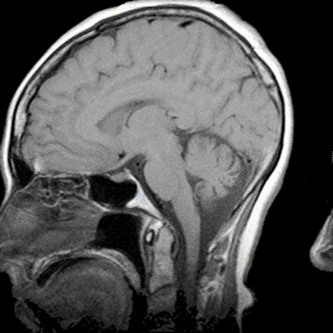
Którą kość oznaczono na obrazie rezonansu magnetycznego?
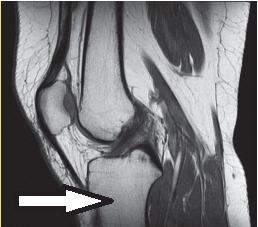
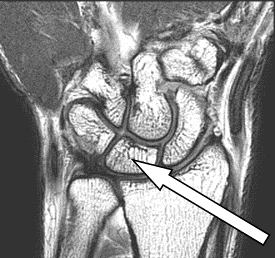
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Na zamieszczonej rycinie przedstawiono
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
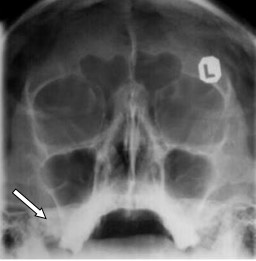
Na radiogramie czaszki strzałką zaznaczono
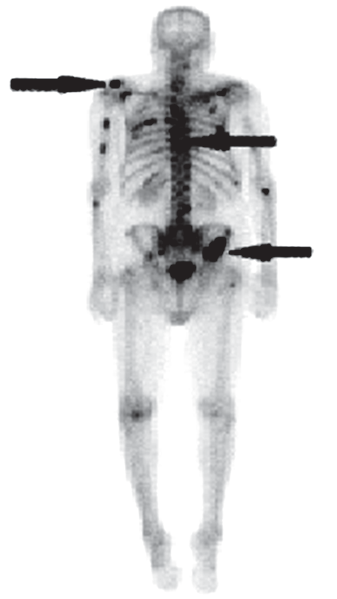
Na scyntygramie kości strzałkami oznaczono ogniska
Promieniowanie jonizujące pośrednio to
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
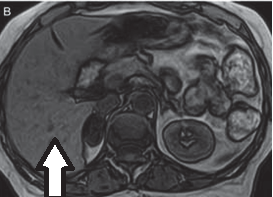
Podczas teleradioterapii piersi lewej narządem krytycznym jest
W obrazowaniu MR wykorzystuje się moment magnetyczny
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
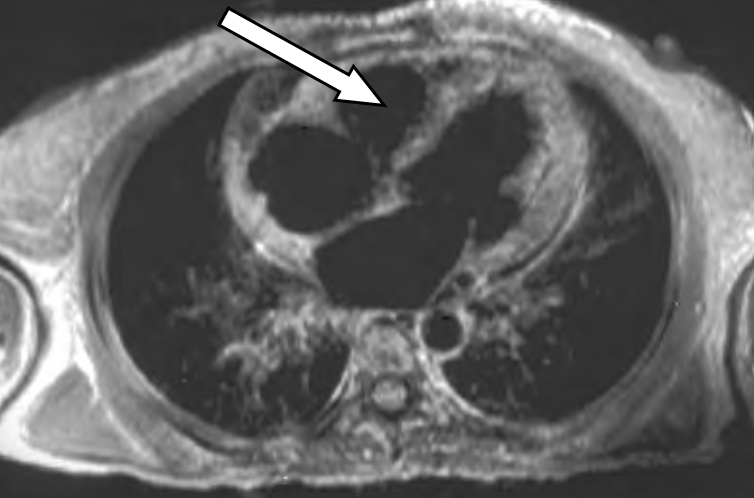
Na skanie rezonansu magnetycznego serca oznaczono
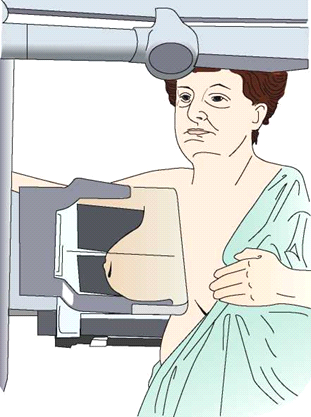
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Odprowadzenie II rejestruje różnicę potencjałów między
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Ligand stosuje się
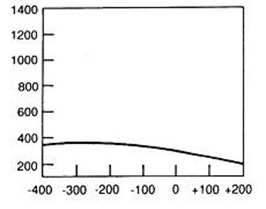
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
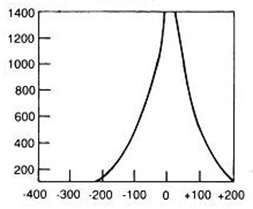
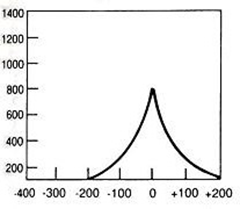
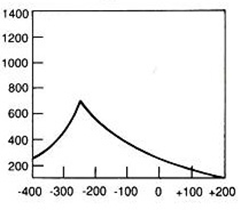
Na scyntygramie strzałką oznaczono
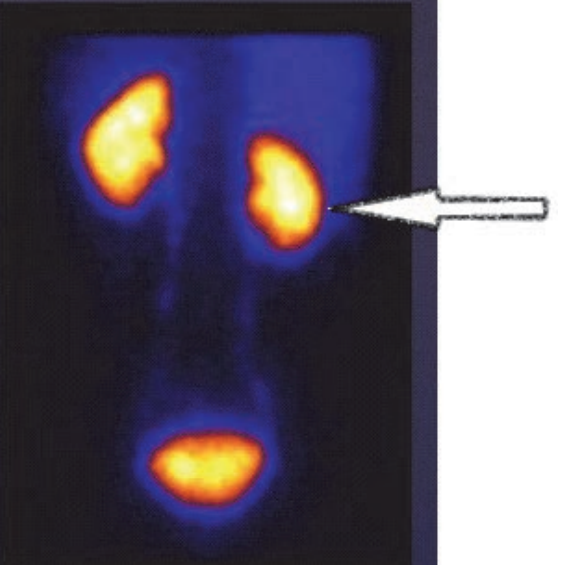
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Czym charakteryzuje się późny odczyn popromienny?
Rytm alfa i beta rejestruje się podczas badania
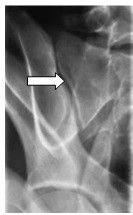
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
W przypadku migotania komór w zapisie EKG występuje
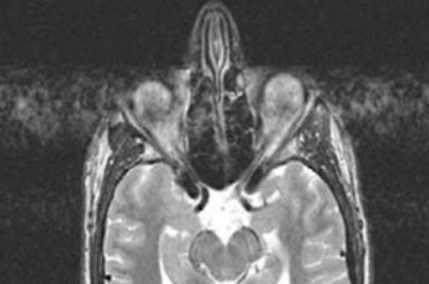
Co jest przyczyną artefaktu widocznego na obrazie MR?
W badaniu PETCT radioizotop ulega