Pytanie 1
Na zamieszczonej rycinie przedstawiono
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Na zamieszczonej rycinie przedstawiono

Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
Limfografia to badanie kontrastowe
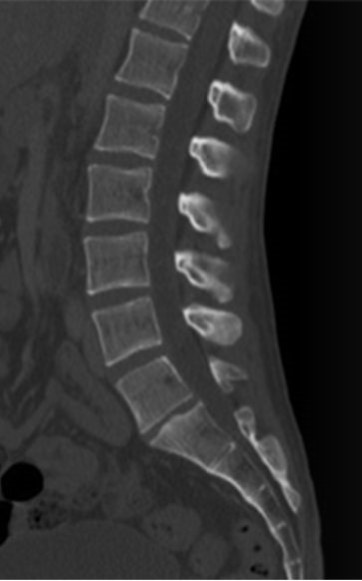
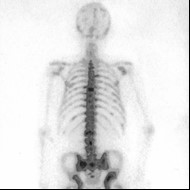
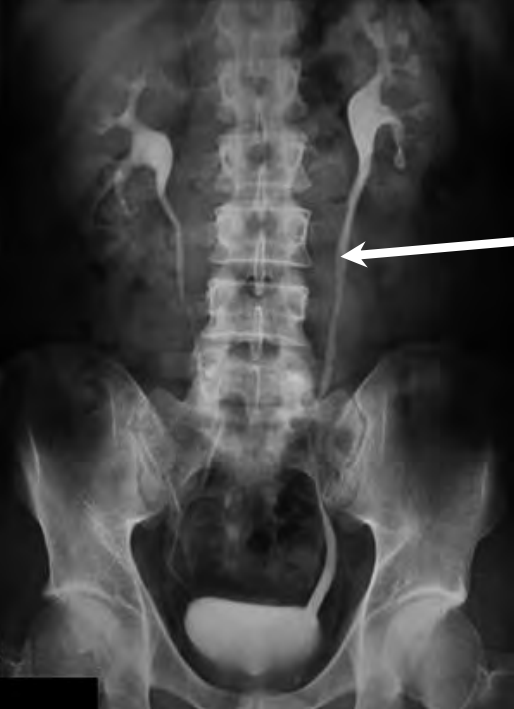
Którą metodą zostało wykonane badanie kręgosłupa zobrazowane na zdjęciu?
Urografia polega na
Pielografia zstępująca umożliwia diagnostykę
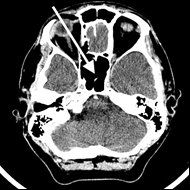
Na radiogramie TK głowy strzałką wskazano
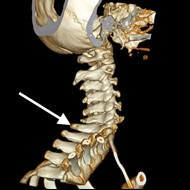
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Przedstawiony obraz został zarejestrowany podczas wykonywania
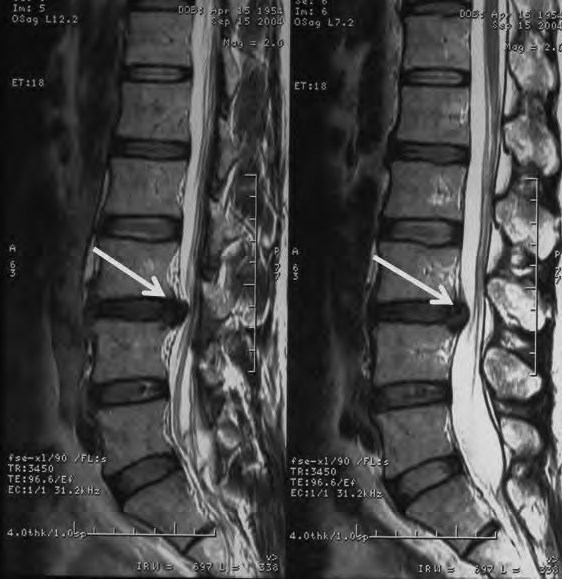
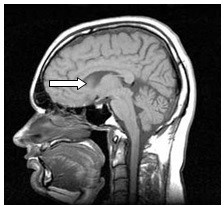
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
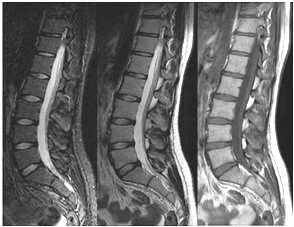
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
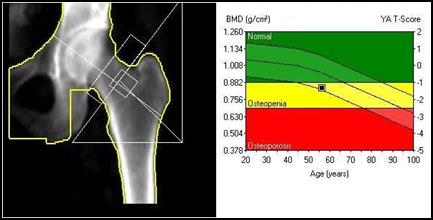
Zamieszczone na ilustracji obrazy dotyczą badania
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
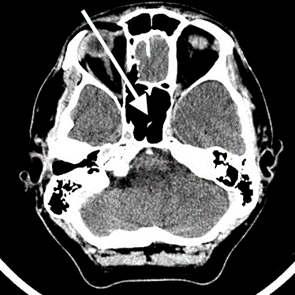
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
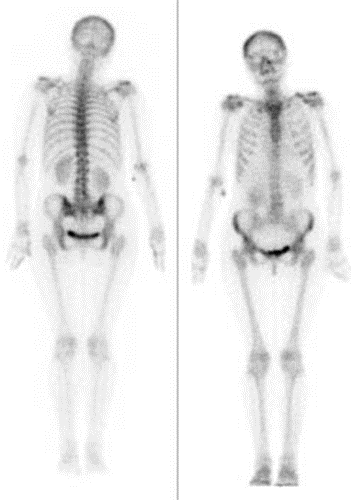
Przedstawiony obraz został zarejestrowany podczas wykonania
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
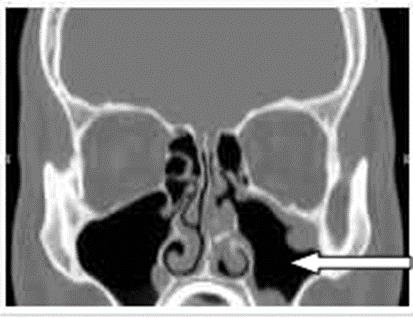
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
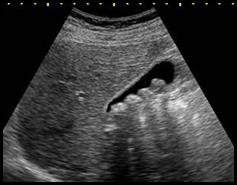
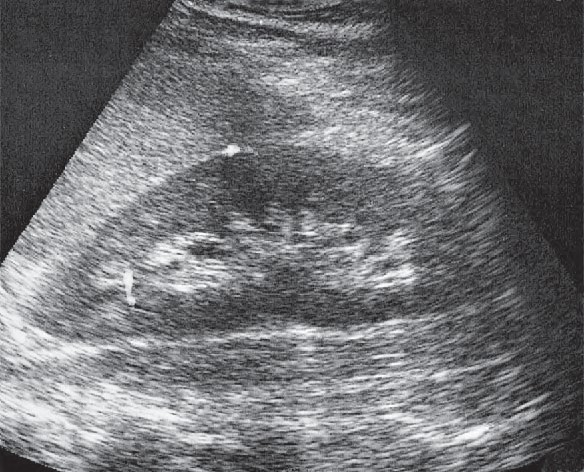
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
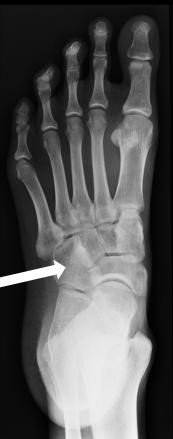
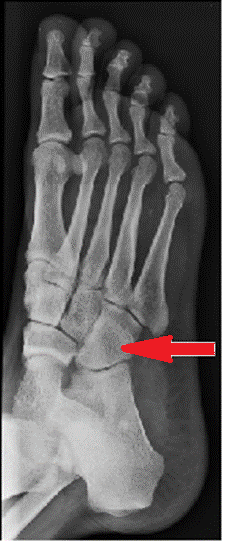
Którą kość zaznaczono strzałką na radiogramie stopy?
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

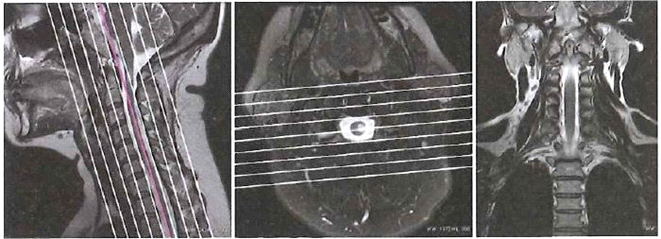
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
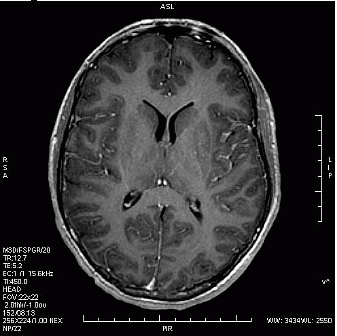
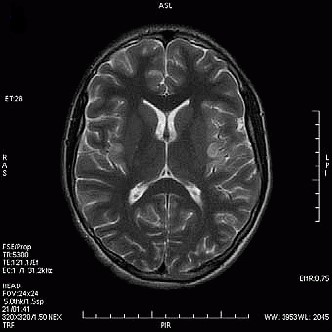
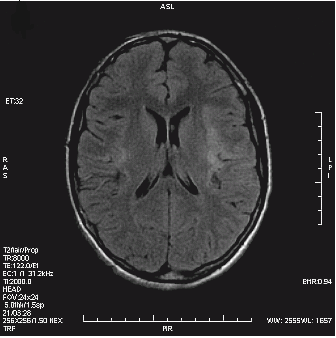
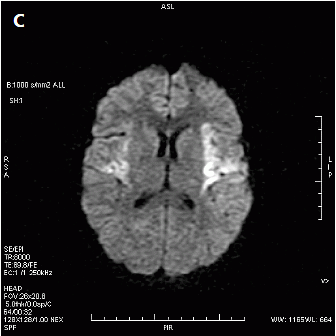
Który obraz MR mózgu został wykonany w sekwencji DWI?
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
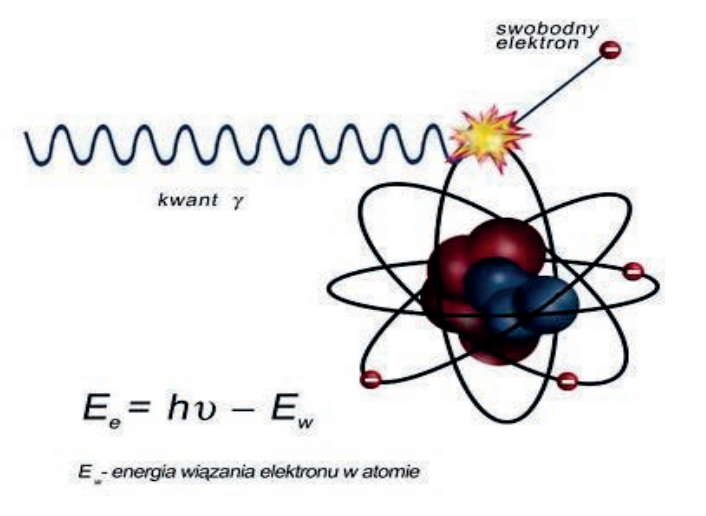
Promieniowanie rentgenowskie powstaje w wyniku hamowania
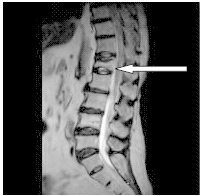
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
Na radiogramie stopy strzałką wskazano kość
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
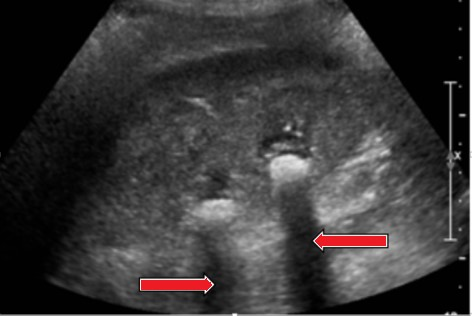
Który artefakt wskazano strzałkami na obrazie USG nerki?
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
Na obrazie RM uwidoczniono odcinek kręgosłupa