Pytanie 1
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
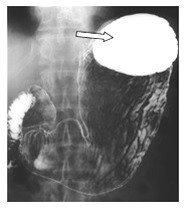
Wynik: 39/40 punktów (97,5%)
Wymagane minimum: 20 punktów (50%)
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?

W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
Na zamieszczonym radiogramie strzałką oznaczono kość
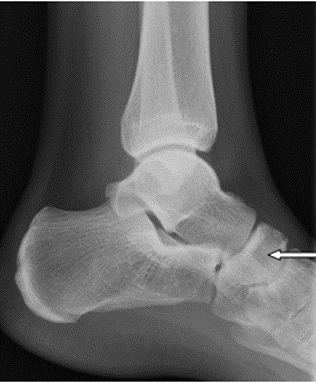
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Na radiogramie uwidoczniono
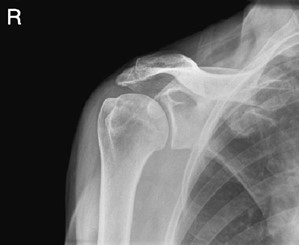
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Podczas teleradioterapii piersi lewej narządem krytycznym jest
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Czym charakteryzuje się późny odczyn popromienny?
Które urządzenia pomocnicze służą do unieruchomienia pacjenta do zabiegu radioterapii?
Nieostrość geometryczna obrazu rentgenowskiego zależy od
W badaniu cystografii wstępującej środek kontrastowy należy podać
Cholangiografia to badanie radiologiczne
Podczas badania gammakamerą źródłem promieniowania jest
Który artefakt uwidoczniono na skanie RM głowy?
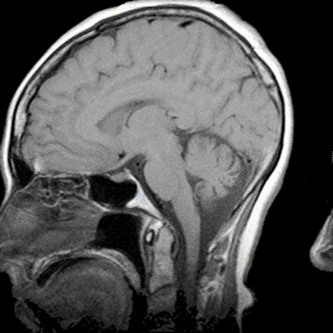
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
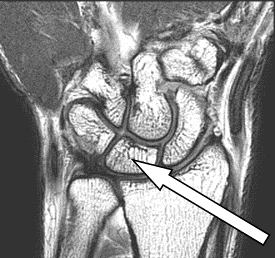
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
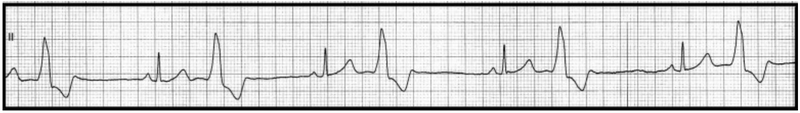
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
Odprowadzenie II rejestruje różnicę potencjałów między
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
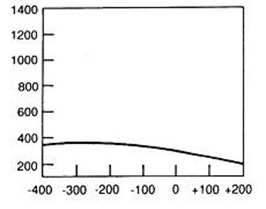
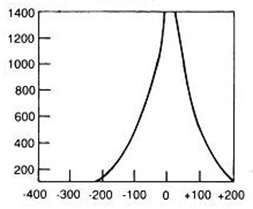
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
Fala głosowa rozchodzi się
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
W radiografii mianem SID określa się
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Na obrazie uwidoczniono
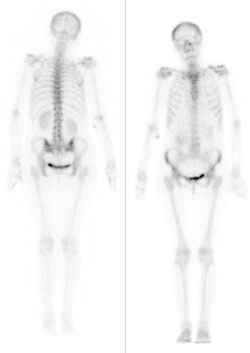
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Celiakografia jest badaniem kontrastowym
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Jednostką indukcji magnetycznej jest