Pytanie 1
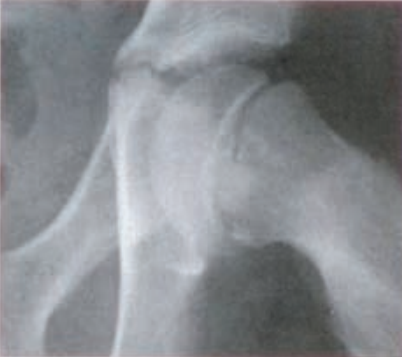
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu

SPECT to
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
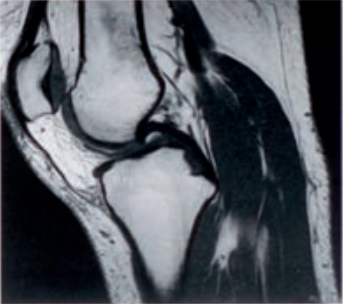
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
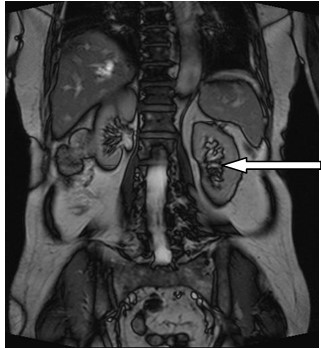
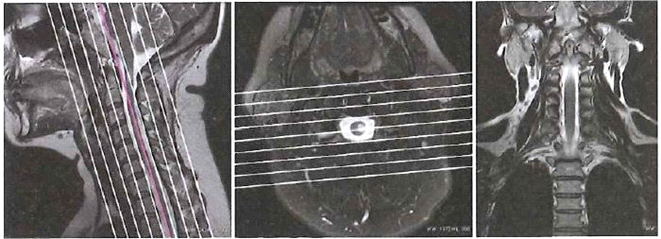
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
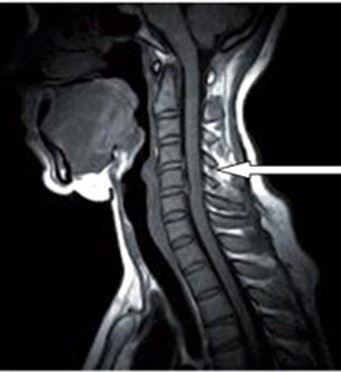
Na obrazie rezonansu magnetycznego strzałką oznaczono wyrostek kolczysty kręgu
Wskazaniem do wykonania badania spirometrycznego jest
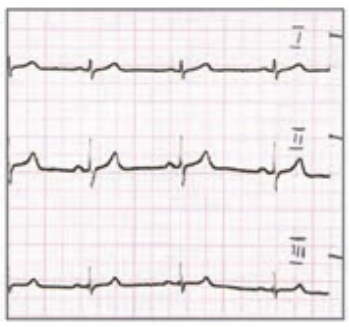
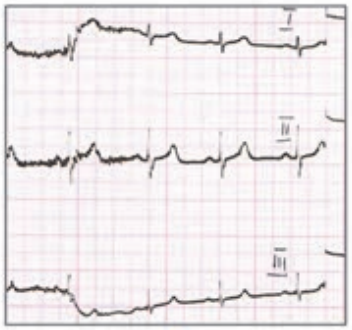
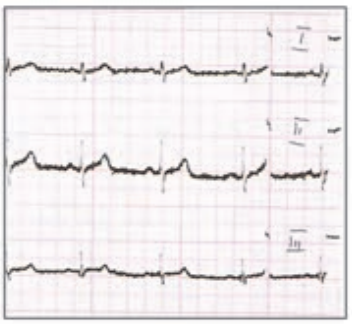
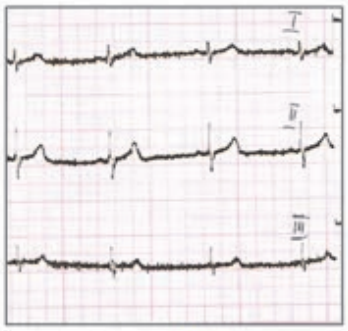
Który elektrokardiogram jest poprawny technicznie?
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Nieostrość geometryczna obrazu rentgenowskiego zależy od
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
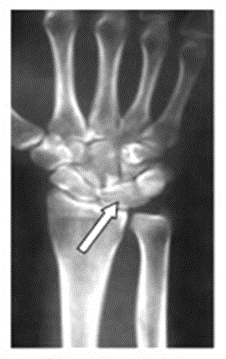
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
Jednostką indukcji magnetycznej jest
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
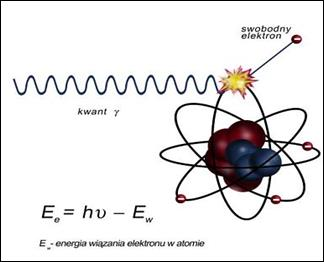
Promieniowanie rentgenowskie jest
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Na ilustracji przedstawiono zjawisko
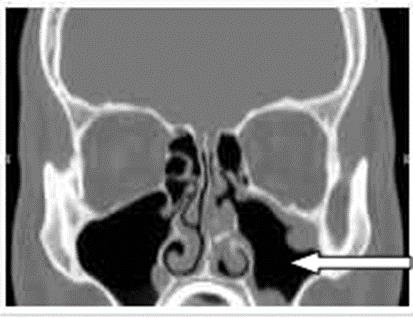
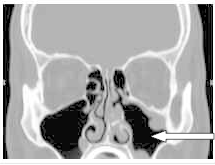
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
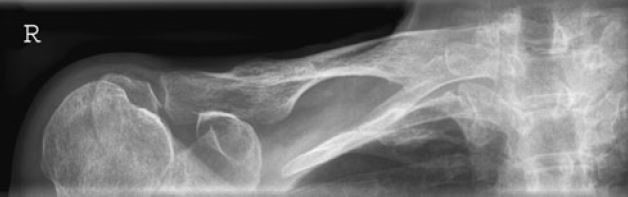
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
Na obrazie TK zaznaczono zatokę
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm × 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Jakie źródła promieniowania stosowane są w brachyterapii?
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
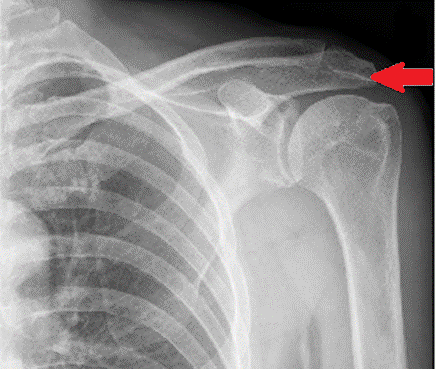
Na radiogramie stawu barkowego strzałką wskazano
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?