Pytanie 1
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Który radioizotop jest emiterem promieniowania alfa?
Technika stereotaktyczna polega na napromienianiu nowotworu
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Teleterapia polega na napromienowaniu
W ultrasonografii występuje zależność:
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Zarejestrowany na obrazie TK artefakt jest spowodowany
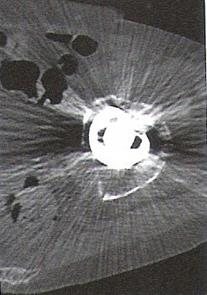
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
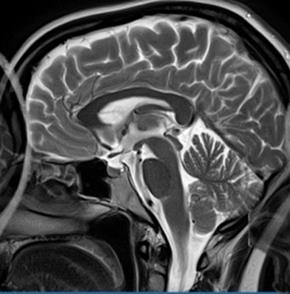
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Skrótem CTV w radioterapii oznacza się
W radioterapii hadronowej leczenie odbywa się przy użyciu
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Czas połowicznego zaniku jest wykorzystywany
Promieniowanie jonizujące pośrednio to
Który radioizotop jest emiterem promieniowania alfa?
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
W diagnostyce metodą rezonansu magnetycznego biorą udział
Obrazowanie portalowe w radioterapii służy do
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
Planowany obszar napromieniania PTV obejmuje
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Fala głosowa rozchodzi się
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Promieniowanie rentgenowskie jest
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym