Pytanie 1
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W badaniu EKG elektrodę przedsercową V4 należy umocować
W badaniu mammograficznym jedną z podstawowych projekcji jest projekcja
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
Pielografia to badanie układu
W obrazowaniu MR wykorzystuje się moment magnetyczny
Celem radioterapii paliatywnej nie jest
Zamieszczone obrazy związane są z badaniem
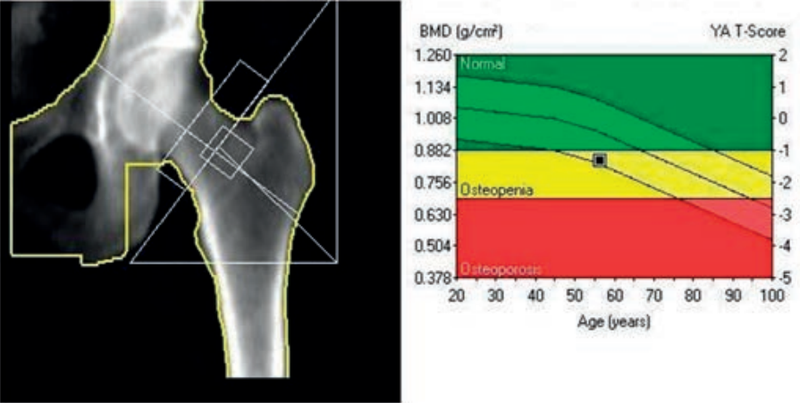
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
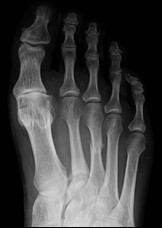
Na radiogramie stopy uwidocznione jest złamanie trzonu
Podczas wykonywania zdjęcia rentgenowskiego klatki piersiowej w celu ochrony radiologicznej pacjenta należy zastosować
Które czynności wykonuje technik elektroradiolog w pracowni „gorącej”?
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Ligand stosuje się
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
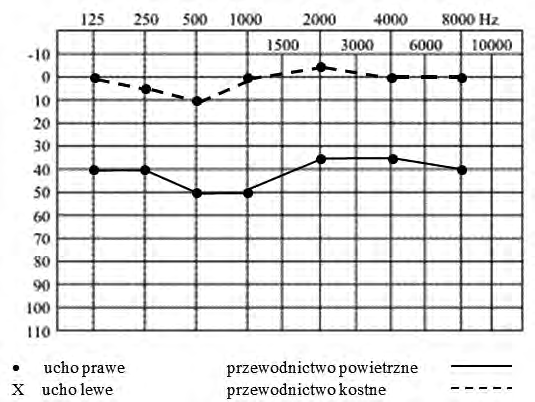
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
W badaniu EKG odprowadzenie I rejestruje różnicę potencjałów między
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
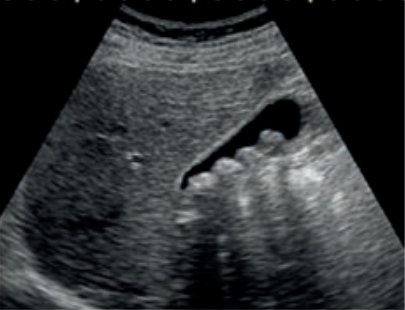
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
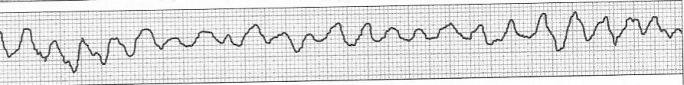
Które zaburzenie rytmu serca zarejestrowano na elektrokardiogramie?
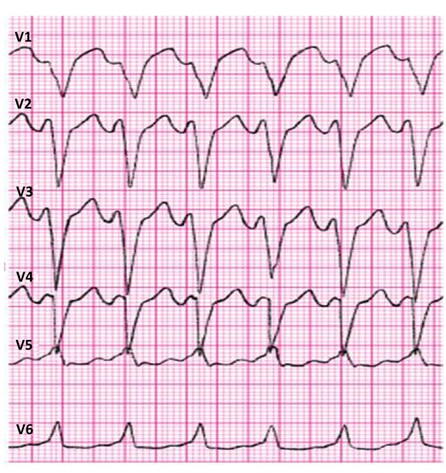
Zamieszczony elektrokardiogram przedstawia
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
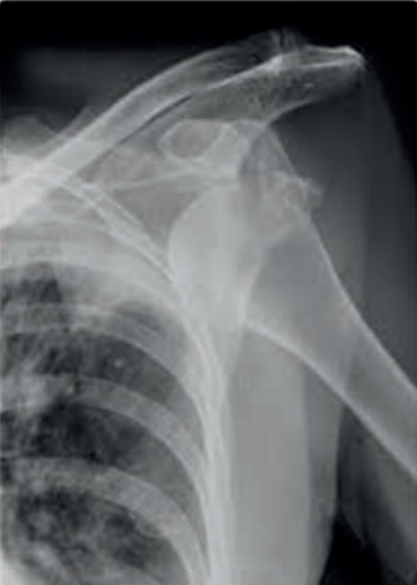
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
W badaniu audiometrycznym do oceny przewodnictwa kostnego wybranego ucha słuchawkę kostną należy przyłożyć do
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?
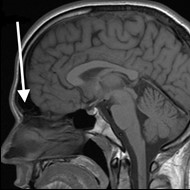
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Rumień skóry pojawiający się podczas radioterapii jest objawem
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody