Pytanie 1
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm × 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Cholangiografia to badanie radiologiczne
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Do wczesnych odczynów popromiennych po radioterapii zalicza się
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
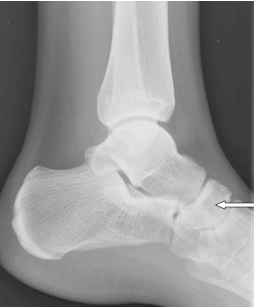
Na radiogramie uwidoczniono złamanie
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
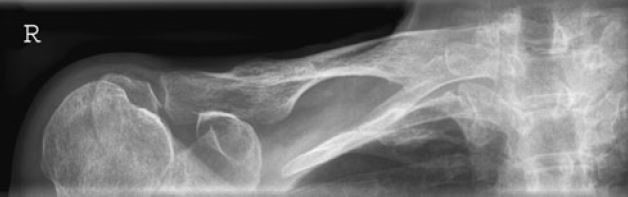
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Odprowadzenie II rejestruje różnicę potencjałów między
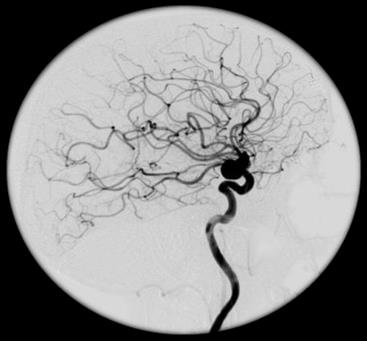
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
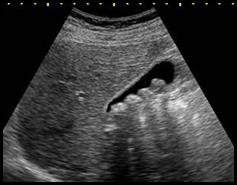
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
W medycynie nuklearnej wykorzystuje się:
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Który z nowotworów jest hormonozależny?
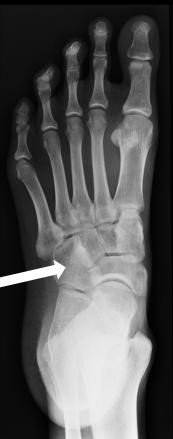
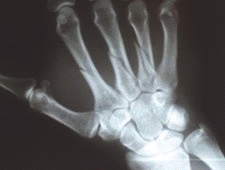
Którą kość zaznaczono strzałką na radiogramie stopy?
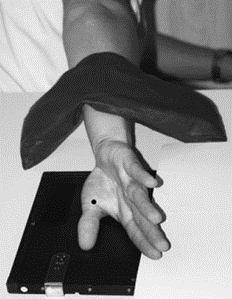
Na ilustracji przedstawiono ułożenie pacjenta do zdjęcia rentgenowskiego
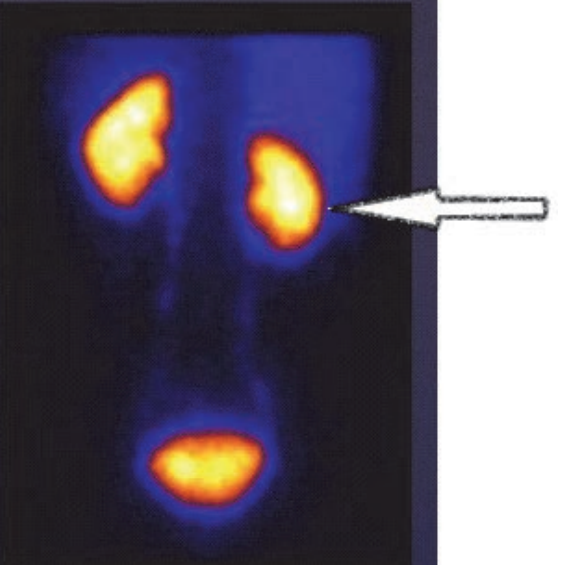
Na scyntygramie strzałką oznaczono
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
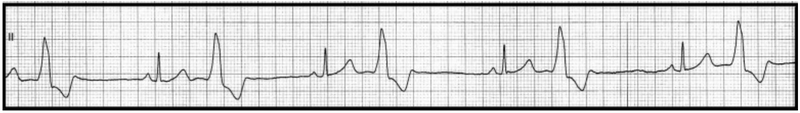
Przedstawiony obraz został zarejestrowany podczas wykonywania
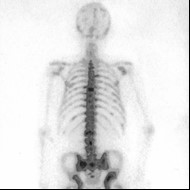
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Czas połowicznego zaniku jest wykorzystywany
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
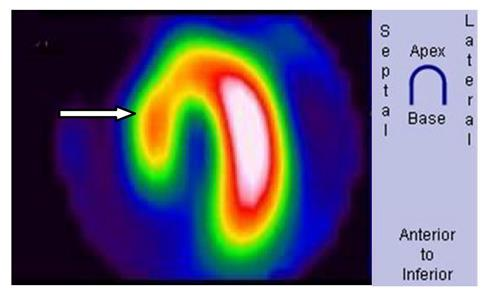
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Jednostką indukcji magnetycznej jest
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Na skanie rezonansu magnetycznego serca oznaczono
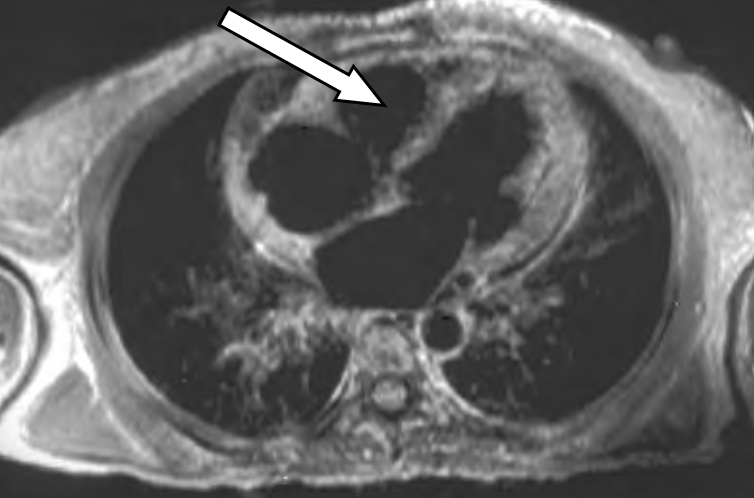
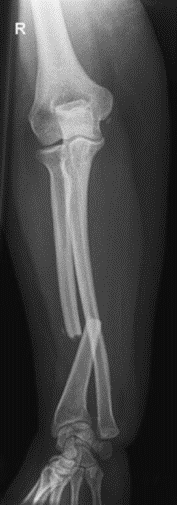
Na radiogramie uwidoczniono złamanie
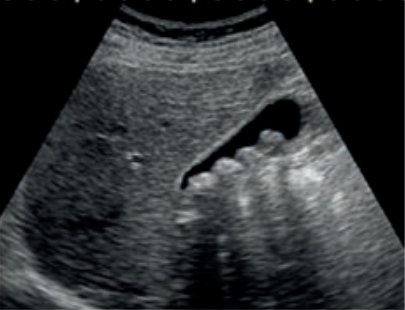
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
Na radiogramie strzałką oznaczono