Pytanie 1
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Która część małej partii materiału jest najczęściej pobierana w celu przygotowania próbki ogólnej?
Czy odpady laboratoryjne zawierające jony metali ciężkich powinny zostać poddane obróbce przed umieszczeniem ich w odpowiednio oznaczonej pojemności?
Który symbol literowy umieszczany na naczyniach miarowych wskazuje na kalibrację do "wlewu"?
Intensywna reakcja z FeCl3 jest wykorzystywana do identyfikacji
Jakie środki stosuje się do czyszczenia szkła miarowego, które zostało zanieczyszczone substancjami tłustymi?
Użycie płuczek jest konieczne w trakcie procesu
Ogólna próbka, jednostkowa lub pierwotna powinna
Co oznacza skrót AKT?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Opis w ramce przedstawia sposób oczyszczania substancji poprzez
| Próbke substancji stałej należy umieścić w kolbie kulistej, zaopatrzonej w chłodnicę zwrotną, dodać rozpuszczalnika - etanolu i delikatnie ogrzewać do wrzenia. Po lekkim ostudzeniu dodać do roztworu niewielką ilość węgla aktywnego, zagotować i przesączyć na gorąco. Przesącz pozostawić do ostygnięcia, a wydzielony osad odsączyć pod zmniejszonym ciśnieniem, przemyć niewielką ilością rozpuszczalnika, przenieść na szalkę, pozostawić do wyschnięcia, a następnie zważyć. |
W parownicy porcelanowej, w której znajduje się 2,5 g naftalenu, umieść krążek bibuły z niewielkimi otworami oraz odwrócony lejek szklany. Zatyczkę lejka zrób z korka z waty. Parownicę umieść w płaszczu grzejnym. Po delikatnym ogrzaniu parownicy, pary substancji przechodzą przez otwory w bibule i kondensują na wewnętrznych ściankach lejka... Powyższy opis dotyczy metody oczyszczania naftalenu przez
Podczas analizowania zmienności składu wód płynących w skali rocznej, próbki wody powinny być zbierane i badane przynajmniej raz na
Procedura przygotowania roztworu Zimmermana-Reinharda
70 g MnSO4·10H2O rozpuścić w 500 cm3 wody destylowanej, dodając ostrożnie 125 cm3 stężonego H2SO4 i 125 cm3 85% H3PO4, ciągle mieszając. Uzupełnić wodą destylowaną do objętości 1dm3.
Który zestaw ilości odczynników jest niezbędny do otrzymania 0,5 dm3 roztworu Zimmermana-Reinharda, zgodnie z podaną procedurą?
| MnSO4·10H2O [g] | Stężony H2SO4 [cm3] | 85% H3PO4 [cm3] | Woda destylowana [cm3] | |
|---|---|---|---|---|
| A. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 370 cm3 |
| B. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 420 cm3 |
| C. | 70 g | 125 cm3 | 125 cm3 | ok. 500 cm3 |
| D. | 70 g | 125 cm3 | 125 cm3 | ok. 800 cm3 |
Aby pobrać dokładnie 20 cm3 próbkę wody do przeprowadzenia analiz, należy zastosować
W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jaką masę chlorku sodu można znaleźć w 150 g roztworu soli o stężeniu 5% (m/m)?
W wypadku oblania skóry kwasem mrówkowym należy
| Wyciąg z karty charakterystyki Skład: kwas mrówkowy 80%, woda 11-20% Pierwsza pomoc. Po narażeniu przez drogi oddechowe. Natychmiast wezwać lekarza. Po kontakcie ze skórą. Zanieczyszczoną skórę natychmiast przemyć dużą ilością wody. |
Zestaw do filtracji nie zawiera
Przebieg: Po zważeniu dwóch suchych zlewek, odważ kolejno: do jednej 3,63 g Co(NO3)2·6H2O, a do drugiej 3,75 g Na2CO3·10H2O. Następnie do obu zlewek wlej 25 cm3 gorącej wody i mieszając za pomocą bagietki doprowadź do całkowitego rozpuszczenia soli. Do roztworu Co(NO3)2 dodaj gorący roztwór Na2CO3 podczas mieszania. Otrzymany roztwór schłodź w łaźni wodnej z 3 kostkami lodu do temperatury pokojowej. Schłodzony roztwór przefiltruj przy użyciu zestawu do sączenia pod próżnią. Osad na lejku przepłucz wodą destylowaną, aż osiągnie obojętny odczyn przesączu. Przesączony osad osusz z sączkiem międzyposiadającym złożone arkusze bibuły w temperaturze pokojowej. Po wyschnięciu osad zważ i oblicz wydajność. Określ, jaki czynnik wpływa na skład jakościowy uzyskanego węglanu kobaltu(II)?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wykorzystując pipetę gazową, pobrano próbkę azotu (Mn2 = 28 g/mol) o objętości 250 cm3 w standardowych warunkach. Jaką masę ma zmierzony azot?
Woda, która została poddana dwukrotnej destylacji, to woda
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Do kolby destylacyjnej wprowadzono 200 cm3 zanieczyszczonego acetonu o gęstości d = 0,9604 g/cm3 oraz czystości 90% masowych. W celu oczyszczenia przeprowadzono proces destylacji, w wyniku czego uzyskano 113,74 g czystego acetonu. Jakie były straty acetonu podczas destylacji?
Oddzielanie płynnej mieszaniny wieloskładnikowej poprzez odparowanie, a następnie skraplanie jej komponentów, to proces
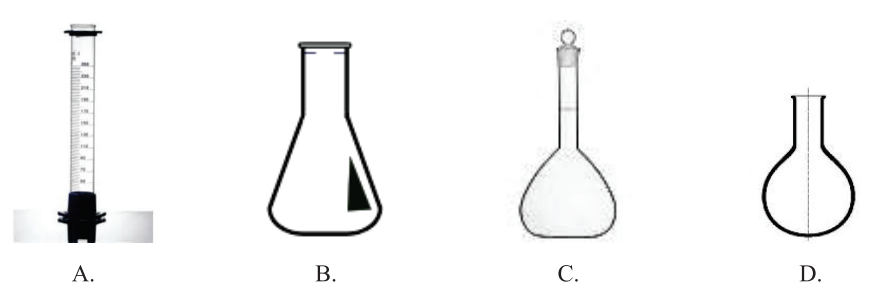
W celu przygotowania roztworu mianowanego należy użyć sprzętu przedstawionego na rysunku
Ze względu na czystość, substancja oznakowana zamieszczoną etykietą powinna być wykorzystywana głównie do

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
Laboratoryjna apteczka powinna zawierać m.in.
Chemikalia, dla których upłynął okres przydatności,
Temperatura wrzenia aniliny przy normalnym ciśnieniu wynosi 457,13 K. W trakcie jej oczyszczania metodą destylacji prostej pod ciśnieniem atmosferycznym należy zebrać frakcję wrzącą w przedziale temperatur
Do grupy reagentów o szczególnym zastosowaniu nie wlicza się
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Analiza technicznego kwasu solnego dała następujące wyniki: 30% HCl, 0,008% H2SO4, 0,04% Fe.
Korzystając z zamieszczonej tabeli wymagań, określ gatunek kwasu, pamiętając, że decyduje o nim najgorszy wskaźnik.
| Wymagania chemiczne dotyczące kwasu siarkowego | ||||
| Wymagania | Gatunki | |||
| I | II | III | IV | |
| Chlorowodór, % | > 33 | > 29 | > 28 | > 27 |
| Kwas siarkowy(VI) w przel. na SO42-, % | < 0,009 | < 0,5 | < 1,6 | < 1,8 |
| Żelazo (Fe3+), % | < 0,005 | < 0,03 | < 0,03 | < 0,05 |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.