Pytanie 1
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
Wynik: 1/40 punktów (2,5%)
Wymagane minimum: 20 punktów (50%)
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
Rozpuszczalność siarczanu(VI) potasu przy temperaturze 30oC wynosi 13 g na 100 g wody. Jaką masę tego związku należy dodać do wody, aby uzyskać 500 g roztworu nasyconego?
Proces oddzielania mieszaniny niejednorodnej, który zachodzi w wyniku opadania cząstek pod działaniem grawitacji, nazywamy
Brak odpowiedzi na to pytanie.
Na podstawie danych zawartych w tabeli określ, do oznaczania którego parametru próbka musi być utrwalona w niskim pH.
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
Brak odpowiedzi na to pytanie.
Na rysunku przedstawiono proces
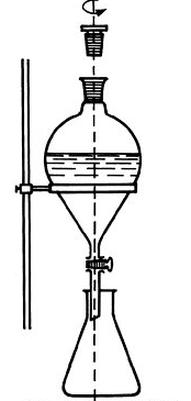
Brak odpowiedzi na to pytanie.
Jednym z sposobów oddzielania jednorodnych mieszanin jest
Brak odpowiedzi na to pytanie.
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

Brak odpowiedzi na to pytanie.
Na opakowaniu którego odczynnika powinien znaleźć się piktogram przedstawiony na ilustracji?
Brak odpowiedzi na to pytanie.
Podczas pobierania skoncentrowanego roztworu kwasu solnego konieczne jest pracowanie w włączonym dygestorium oraz zastosowanie
Brak odpowiedzi na to pytanie.
W trakcie korzystania z odczynnika opisanego na etykiecie, należy szczególnie zwrócić uwagę na zagrożenia związane
Brak odpowiedzi na to pytanie.
Wybór lokalizacji do poboru próbek wody z rzeki nie jest uzależniony od
Brak odpowiedzi na to pytanie.
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
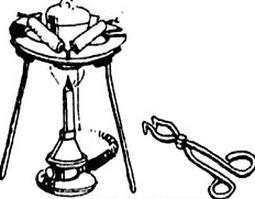
Brak odpowiedzi na to pytanie.
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
Brak odpowiedzi na to pytanie.
Metodą, która nie umożliwia przeniesienia składników próbki do roztworu, jest
Brak odpowiedzi na to pytanie.
Na rysunku przedstawiono przyrząd do pobierania próbek

Brak odpowiedzi na to pytanie.
Waga przedstawiona na rysunku umożliwia ważenie substancji z dokładnością do

Brak odpowiedzi na to pytanie.
Jakie urządzenie wykorzystuje się do pobierania próbek gazów?
Brak odpowiedzi na to pytanie.
Który z poniższych zestawów obejmuje jedynie sprzęt do pomiarów?
Brak odpowiedzi na to pytanie.
W wyniku analizy sitowej próbki stałej otrzymano frakcję o średnicy ziaren 12 – 30 mm. Jaką masę powinna mieć prawidłowo pobrana próbka pierwotna?
| Tabela. Wielkość próbki pierwotnej w zależności od wielkości ziarna | ||||
|---|---|---|---|---|
| Średnica ziaren lub kawałków [mm] | do 1 | 1 - 10 | 11 - 50 | ponad 50 |
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Brak odpowiedzi na to pytanie.
W trakcie destylacji cieczy wykorzystuje się tzw. kamienie wrzenne, ponieważ
Brak odpowiedzi na to pytanie.
Przedstawiony na rysunku zagłębnik stosuje się do pobierania próbek
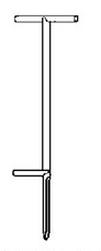
Brak odpowiedzi na to pytanie.
Aby poprawić efektywność reakcji opisanej równaniem: HCOOH + C2H5OH ⇄ HCOOC2H5 + H2O, należy
Brak odpowiedzi na to pytanie.
Kalibracja pH-metru nie jest potrzebna po
Brak odpowiedzi na to pytanie.
Fragment procedury analitycznej
(...) Przenieś badany roztwór całkowicie do rozdzielacza gruszkowego o pojemności od 50 do 100 cm3, dodaj 5 cm3 roztworu tiocyjanianu potasu oraz 10 cm3 alkoholu izopentylowego, a następnie wstrząsaj zawartością przez 30 sekund.
Po rozdzieleniu faz przenieś roztwór wodny do drugiego rozdzielacza, natomiast fazę organiczną do suchej kolbki miarowej o pojemności 50 cm3(...) Który rodzaj ekstrakcji jest opisany w powyższym fragmencie?
Brak odpowiedzi na to pytanie.
Oblicz masę wapienia, który został rozłożony, jeśli w trakcie reakcji uzyskano 44,8 dm3 CO2 (w warunkach standardowych).
MC = 12 g/mol, MCa = 40 g/mol, MO = 16 g/mol
Brak odpowiedzi na to pytanie.
W wyniku rozkładu 100 g węglanu wapnia, otrzymano 25 g tlenku wapnia. Wydajność procentowa reakcji wynosi
| MCaCO3 = 100g / mol | MCaO = 56g / mol |
Brak odpowiedzi na to pytanie.
Który z wymienionych roztworów NaOH, o określonych stężeniach, nie jest roztworem mianowanym?
Brak odpowiedzi na to pytanie.
Z 250 g benzenu (M = 78 g/mol) uzyskano 350 g nitrobenzenu (M = 123 g/mol). Jaka jest wydajność reakcji nitrowania?
Brak odpowiedzi na to pytanie.
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
Brak odpowiedzi na to pytanie.
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
Brak odpowiedzi na to pytanie.
Na rysunku numerami rzymskimi oznaczono
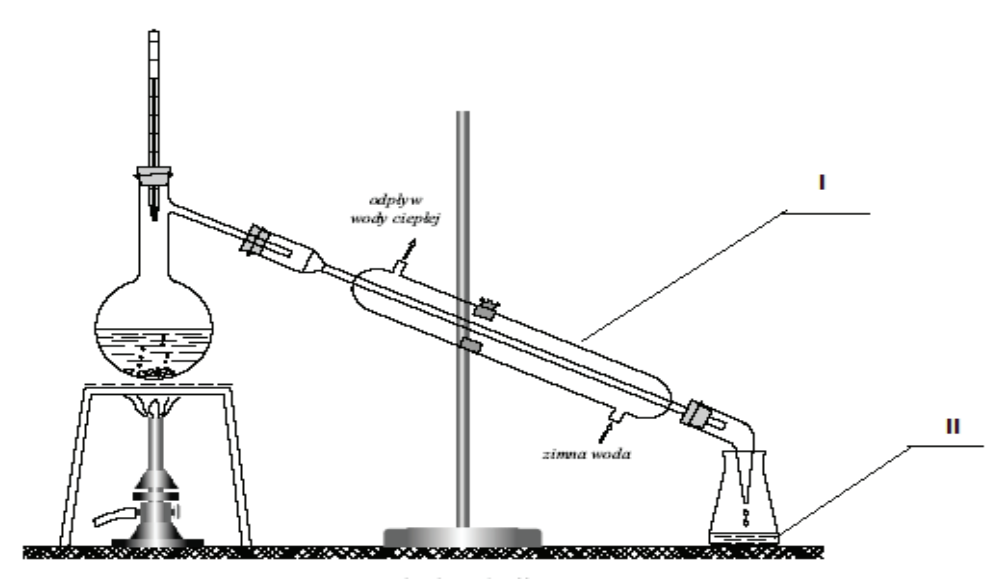
Brak odpowiedzi na to pytanie.
Zamieszczony piktogram przedstawia substancję o klasie i kategorii zagrożenia:

Brak odpowiedzi na to pytanie.
Stosunek masowy miedzi do siarki w siarczku miedzi(I) wynosi
| 16S Siarka 32 | 29Cu Miedź 63,55 |
Brak odpowiedzi na to pytanie.
W przypadku odczynnika, w którym nawet najczulsze techniki analizy chemicznej nie są w stanie wykryć zanieczyszczeń, a jego badanie wymaga zastosowania metod opartych na zjawiskach fizycznych, zalicza się on do kategorii czystości
Brak odpowiedzi na to pytanie.
Zestaw do filtracji pod obniżonym ciśnieniem powinien obejmować między innymi
Brak odpowiedzi na to pytanie.
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
Brak odpowiedzi na to pytanie.
Aby przygotować 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3, jaką kolbę miarową o pojemności należy wykorzystać?
Brak odpowiedzi na to pytanie.
Zastosowanie łaźni wodnej nie jest zalecane w trakcie prac, w których stosuje się
Brak odpowiedzi na to pytanie.
Oddzielanie płynnej mieszaniny wieloskładnikowej poprzez odparowanie, a następnie skraplanie jej komponentów, to proces
Brak odpowiedzi na to pytanie.
Aby przygotować miano kwasu solnego, konieczne jest odważenie węglanu sodu o masie wynoszącej około 400 mg. Jaką precyzję powinna mieć waga używana do odważenia węglanu sodu?
Brak odpowiedzi na to pytanie.