Pytanie 1
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

W badaniu PET stosuje się tylko radioizotopy emitujące
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Rytm alfa i beta rejestruje się podczas badania
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem jest
Brachyterapia wewnątrzprzewodowa jest stosowana w leczeniu
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
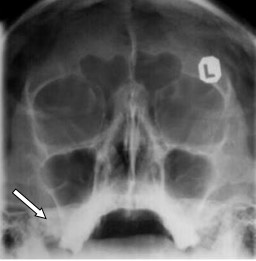
Na radiogramie czaszki strzałką zaznaczono
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
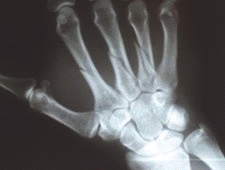
Na radiogramie uwidoczniono złamanie
W których projekcjach wykonuje się standardowe badanie mammograficzne?
Pielografia to badanie układu
Rytm alfa i beta rejestruje się podczas badania
Skrótem CTV w radioterapii oznacza się
Który radioizotop stosuje się do badania scyntygraficznego kości?
W leczeniu izotopowym tarczycy podaje się
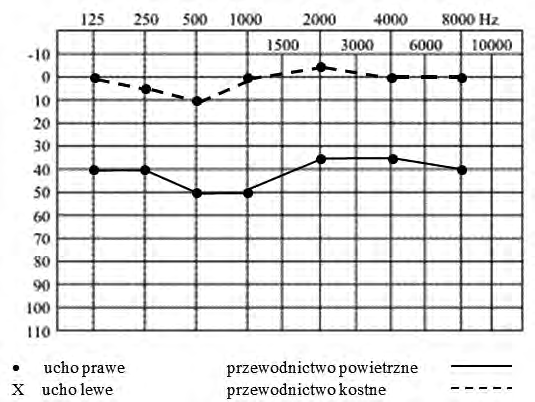
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Który radioizotop jest emiterem promieniowania alfa?
Radiogram przedstawia
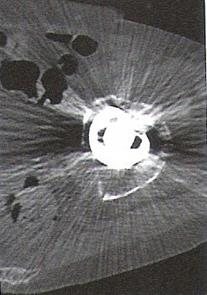
Zarejestrowany na obrazie TK artefakt jest spowodowany
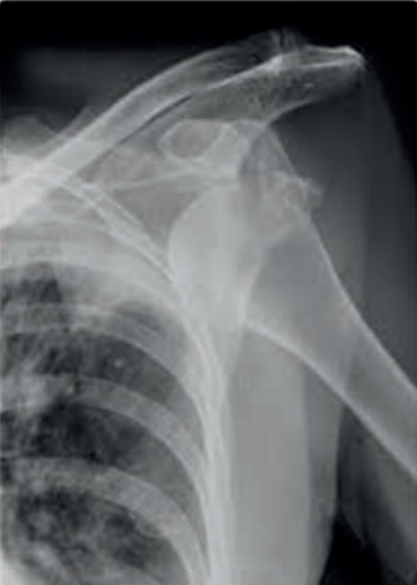
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Diagnozowanie metodą PET oparte jest na zjawisku
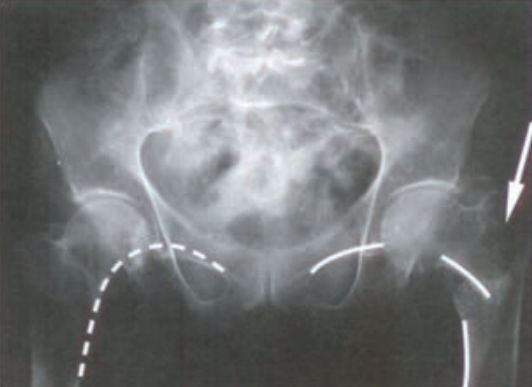
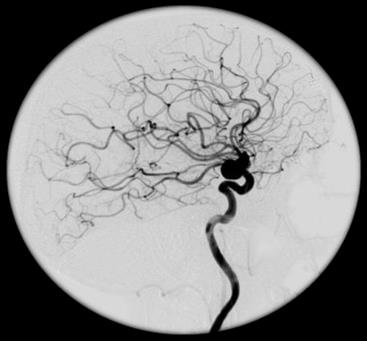
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
Fala głosowa rozchodzi się
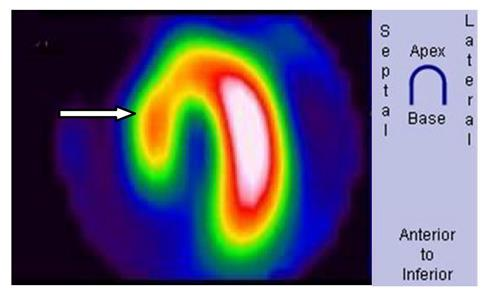
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
W ultrasonografii występuje zależność:
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




W leczeniu izotopowym tarczycy należy podać
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |