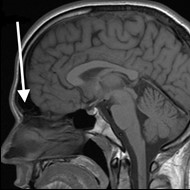
Pytanie 1
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
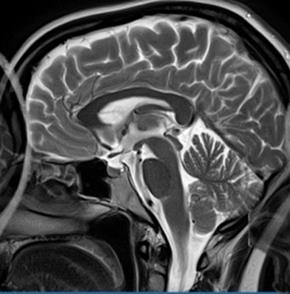
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.

Na radiogramie uwidoczniono złamanie
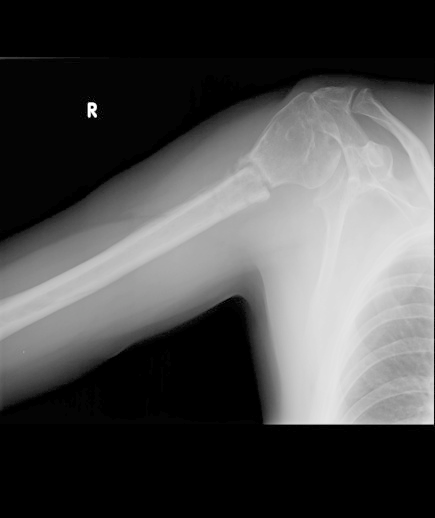
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
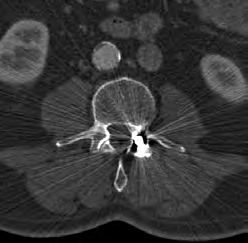
Który artefakt jest widoczny na skanie tomografii komputerowej?
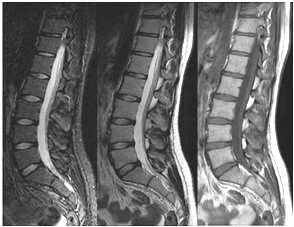
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
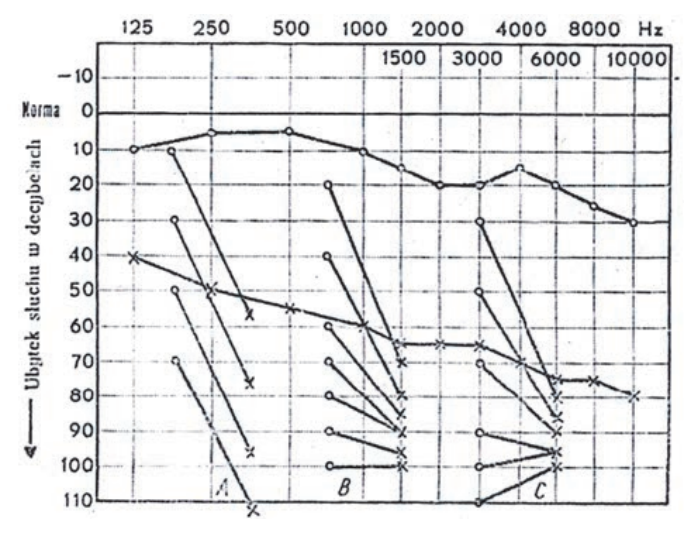
Audiogram przedstawia próbę
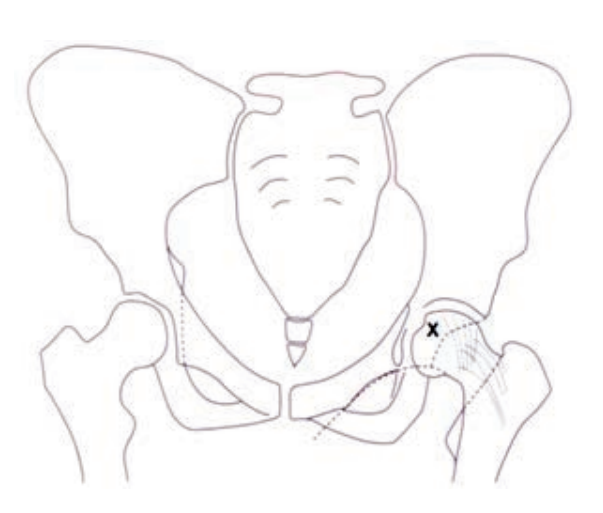
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
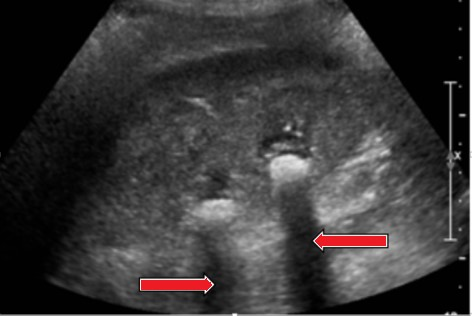
Który artefakt wskazano strzałkami na obrazie USG nerki?
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
Do planowego badania TK klatki piersiowej z użyciem środka cieniującego pacjent powinien zgłosić się
Jaki jest cel stosowania bolusa w radioterapii?
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Co jest przyczyną artefaktu widocznego na obrazie MR?
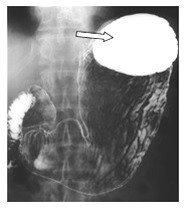
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
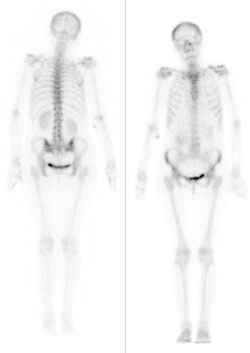
Na obrazie uwidoczniono
W badaniu cystografii wstępującej środek kontrastowy należy podać
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
W standardowym badaniu elektrokardiologicznym elektrodę C4 należy umocować
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
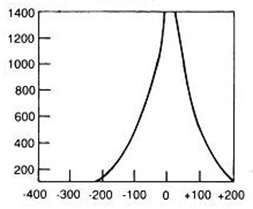
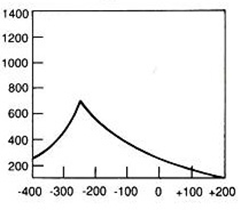
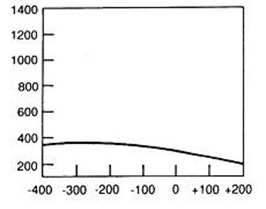
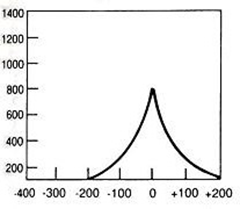
W badaniu PETCT radioizotop ulega
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
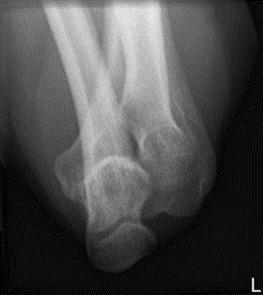
Technik elektroradiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta:
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?
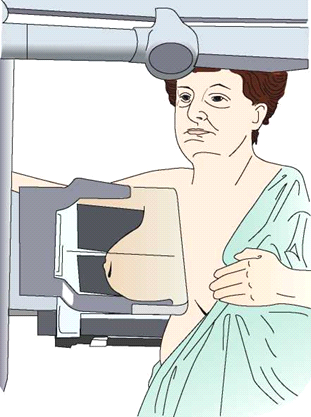
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Jak przebiega promień centralny w projekcji AP czaszki?
Do środków kontrastujących negatywnych należą
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
W ultrasonografii występuje zależność:
Czym charakteryzuje się późny odczyn popromienny?
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę