Pytanie 1
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
Wynik: 15/40 punktów (37,5%)
Wymagane minimum: 20 punktów (50%)
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
W badaniu EKG odprowadzenie I rejestruje różnicę potencjałów między
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
W których projekcjach wykonuje się standardowe badanie mammograficzne?
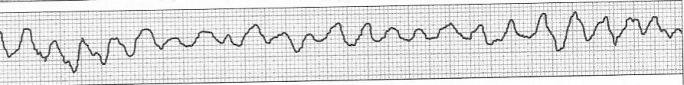
Zamieszczony elektrokardiogram przedstawia
W badaniu cystografii wstępującej środek kontrastowy należy podać
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
W obrazowaniu MR wykorzystuje się moment magnetyczny
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
Planowany obszar napromieniania PTV obejmuje
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
Limfografia to badanie kontrastowe
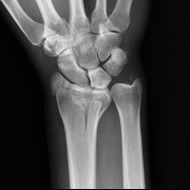
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
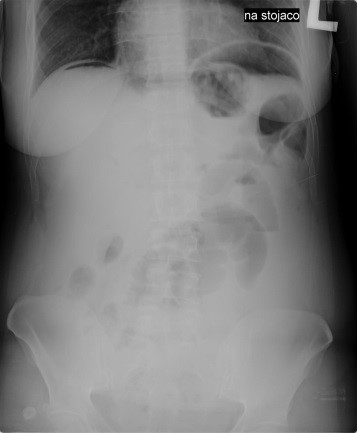
Radiogram jamy brzusznej uwidacznia
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
Brak odpowiedzi na to pytanie.
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
Brak odpowiedzi na to pytanie.
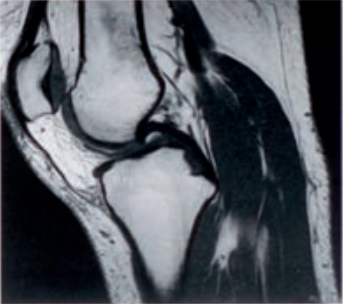
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
Brak odpowiedzi na to pytanie.
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Brak odpowiedzi na to pytanie.
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Brak odpowiedzi na to pytanie.
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Brak odpowiedzi na to pytanie.
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Brak odpowiedzi na to pytanie.
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
Brak odpowiedzi na to pytanie.
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Brak odpowiedzi na to pytanie.
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
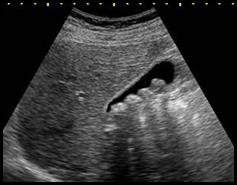
Brak odpowiedzi na to pytanie.
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
Brak odpowiedzi na to pytanie.
Zamieszczone obrazy związane są z badaniem
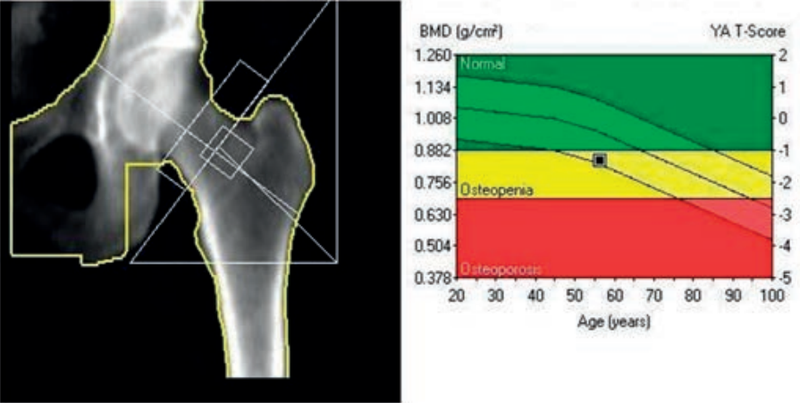
Brak odpowiedzi na to pytanie.
Na skanie rezonansu magnetycznego serca oznaczono
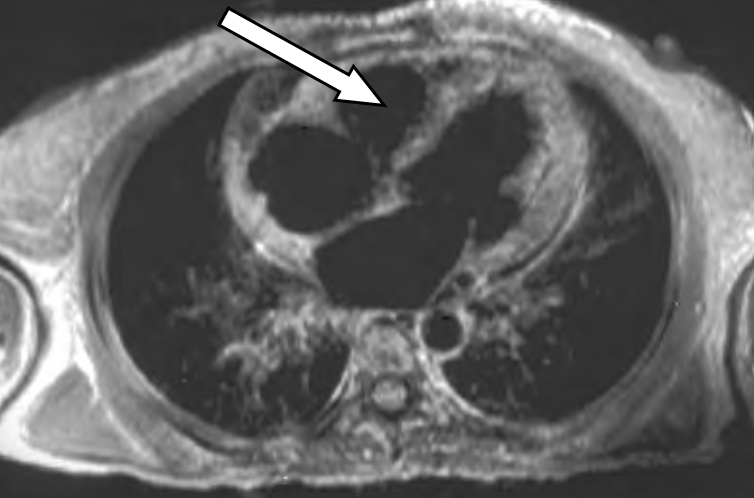
Brak odpowiedzi na to pytanie.
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Brak odpowiedzi na to pytanie.
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Brak odpowiedzi na to pytanie.
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
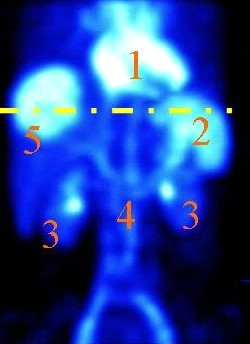
Brak odpowiedzi na to pytanie.
Na ilustracji przedstawiono przygotowanie pacjenta do badania
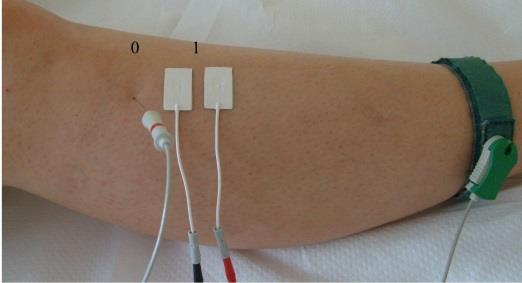
Brak odpowiedzi na to pytanie.
Na zamieszczonym radiogramie strzałką oznaczono kość
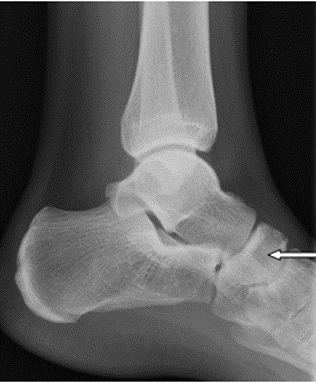
Brak odpowiedzi na to pytanie.
W badaniu EKG elektrodę przedsercową V4 należy umocować
Brak odpowiedzi na to pytanie.
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
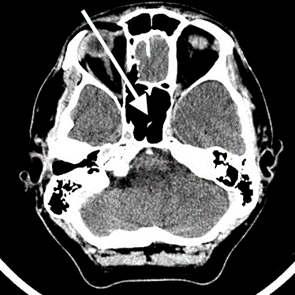
Brak odpowiedzi na to pytanie.