Pytanie 1
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
Wynik: 2/40 punktów (5,0%)
Wymagane minimum: 20 punktów (50%)
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
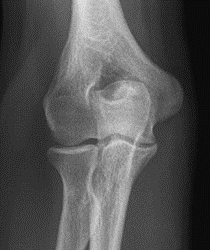
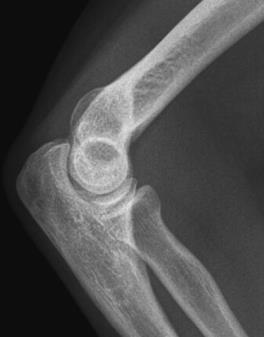
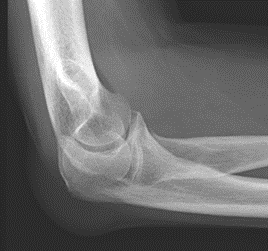
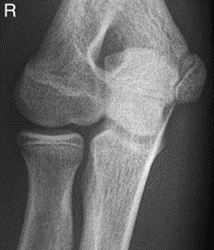
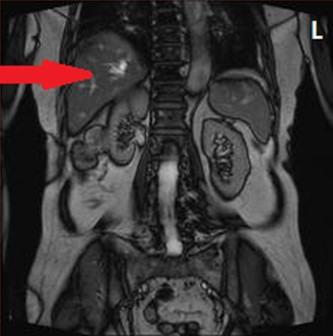
Na obrazie MR jamy brzusznej strzałką wskazano
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
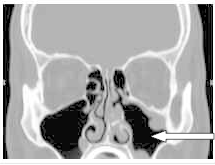
Na obrazie TK zaznaczono zatokę
W badaniu cystografii wstępującej środek kontrastowy należy podać
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Brak odpowiedzi na to pytanie.
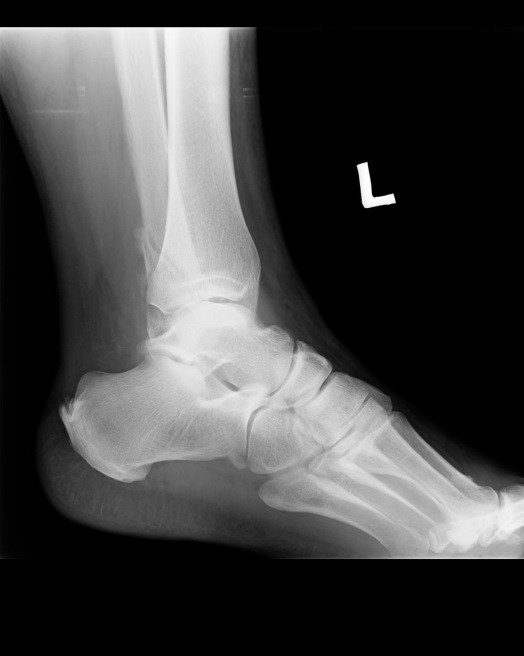
Na obrazie radiologicznym uwidoczniono złamanie kości
Fotostymulacja wykonywana jest podczas badania
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Brak odpowiedzi na to pytanie.
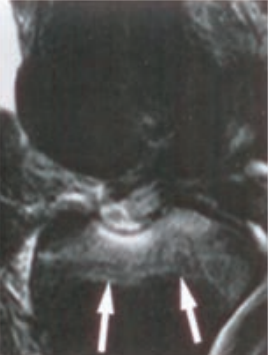
Obraz stawu kolanowego otrzymano metodą
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Obrazy DDR są tworzone w trakcie
Brak odpowiedzi na to pytanie.
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Brak odpowiedzi na to pytanie.
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Brak odpowiedzi na to pytanie.
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Brak odpowiedzi na to pytanie.
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
Brak odpowiedzi na to pytanie.
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
Brak odpowiedzi na to pytanie.
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Brak odpowiedzi na to pytanie.
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
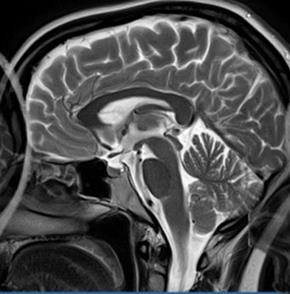
Brak odpowiedzi na to pytanie.
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
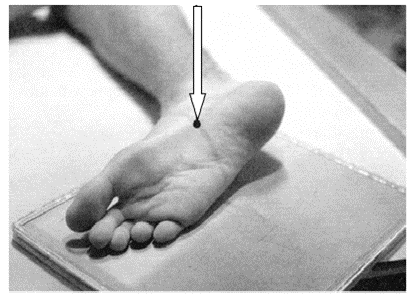
Brak odpowiedzi na to pytanie.
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
Brak odpowiedzi na to pytanie.
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Brak odpowiedzi na to pytanie.
Na obrazie rentgenowskim strzałką zaznaczono
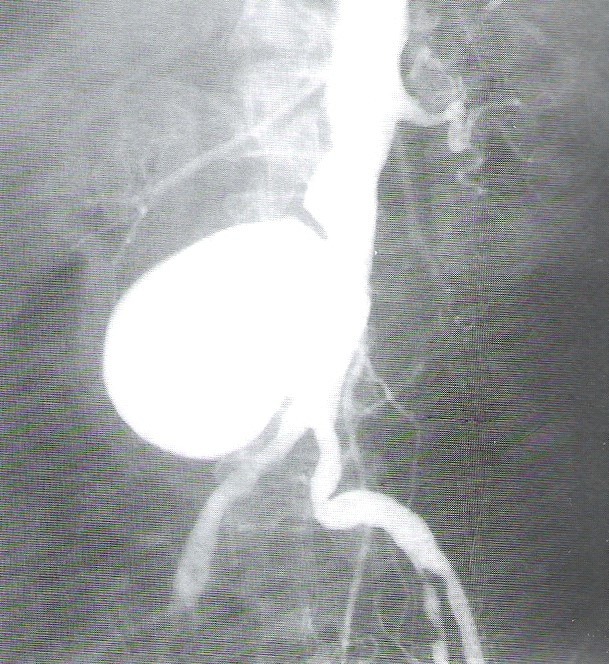
Brak odpowiedzi na to pytanie.
Na obrazie rezonansu magnetycznego strzałką oznaczono wyrostek kolczysty kręgu
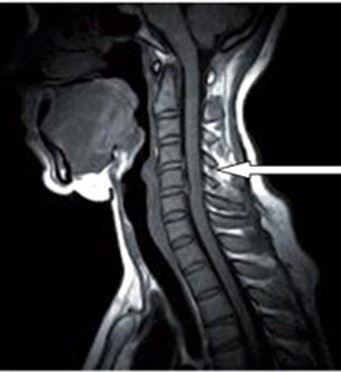
Brak odpowiedzi na to pytanie.
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
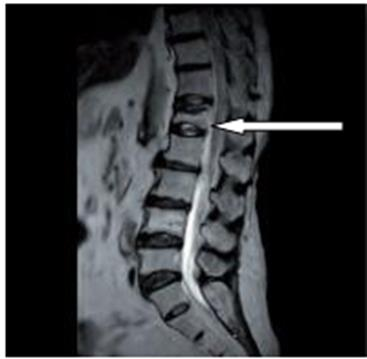
Brak odpowiedzi na to pytanie.
Na zamieszczonej rycinie przedstawiono
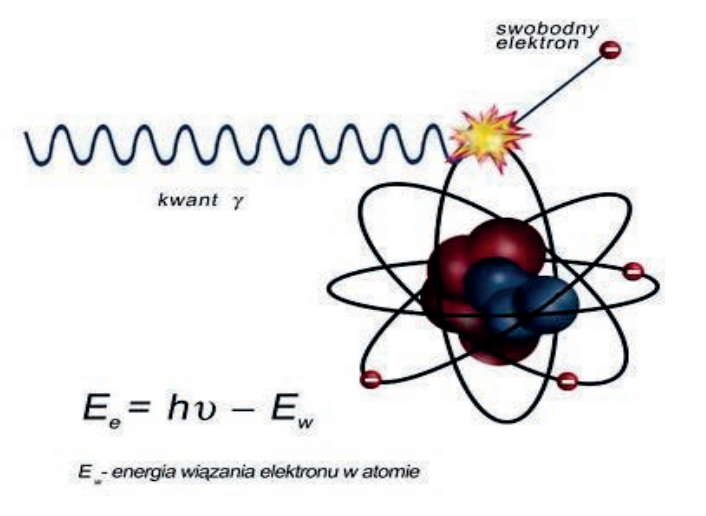
Brak odpowiedzi na to pytanie.
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Brak odpowiedzi na to pytanie.
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Brak odpowiedzi na to pytanie.
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
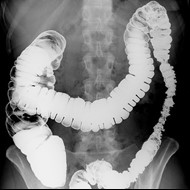
Brak odpowiedzi na to pytanie.
Na radiogramie uwidoczniono złamanie
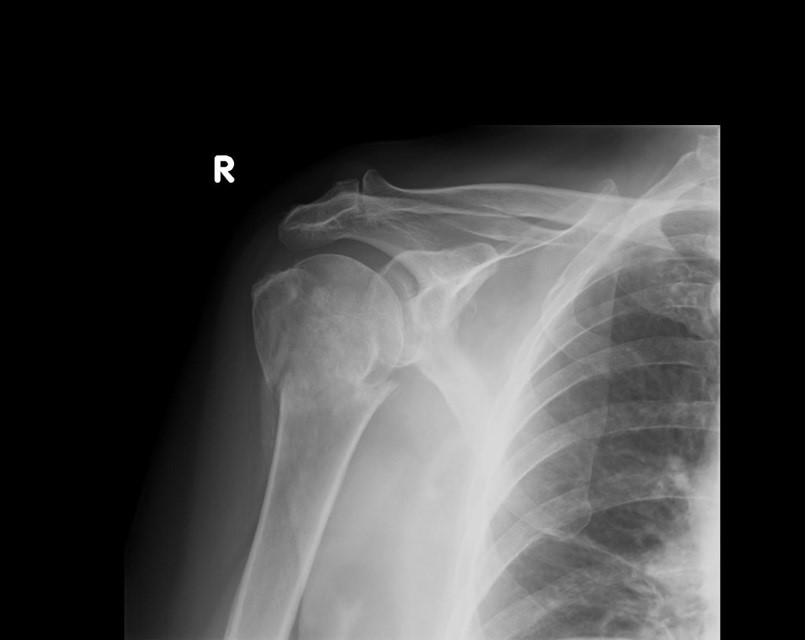
Brak odpowiedzi na to pytanie.
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Brak odpowiedzi na to pytanie.
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Brak odpowiedzi na to pytanie.
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Brak odpowiedzi na to pytanie.
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Brak odpowiedzi na to pytanie.
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
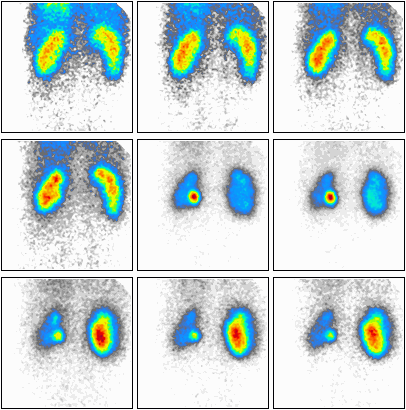
Brak odpowiedzi na to pytanie.
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Brak odpowiedzi na to pytanie.
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
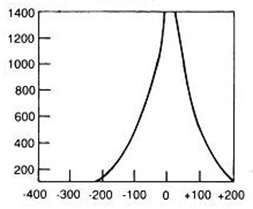
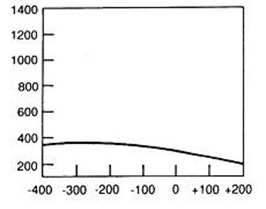
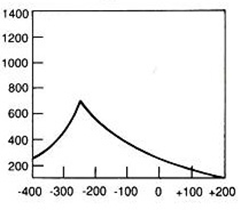
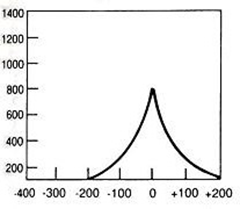
Brak odpowiedzi na to pytanie.
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Brak odpowiedzi na to pytanie.