Pytanie 1
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
Wynik: 16/40 punktów (40,0%)
Wymagane minimum: 20 punktów (50%)
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
50 cm3 alkoholu etylowego zmieszano w kolbie miarowej z 50 cm3 wody. W wyniku zjawiska kontrakcji objętość otrzymanego roztworu wyniosła 97,5 cm3. Ile wynosi stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu i stężenie procentowe roztworu alkoholu (v/v) po uzupełnieniu kolby wodą do 100 cm3?
| Stężenie procentowe (v/v) roztworu alkoholu w wodzie po zmieszaniu | Stężenie procentowe (v/v) roztworu alkoholu po uzupełnieniu kolby wodą do 100 cm3 | |
|---|---|---|
| A. | 49,2% | 48,0% |
| B. | 50,0% | 49,7% |
| C. | 51,3%, | 50,0% |
| D. | 53,3% | 50,2% |
Brak odpowiedzi na to pytanie.
Czego się używa w produkcji z porcelany?
Jakie pH ma roztwór buforowy otrzymany w wyniku zmieszania 0,2 M roztworu kwasu octowego i 0,2 M roztworu octanu sodu, w stosunku objętościowym 3 : 2?
| Bufor octanowy według Walpole'a | ||
|---|---|---|
| 0,2 M kwas octowy [ml] | 0,2 M octan sodu [ml] | pH |
| 7,0 | 3,0 | 4,39 |
| 6,0 | 4,0 | 4,58 |
| 5,0 | 5,0 | 4,75 |
| 4,0 | 6,0 | 4,94 |
| 3,0 | 7,0 | 5,13 |
Brak odpowiedzi na to pytanie.
Aby przygotować 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3, jaką kolbę miarową o pojemności należy wykorzystać?
W tabeli zamieszczono temperatury wrzenia niektórych składników powietrza. Na podstawie tych danych podaj, który ze składników oddestyluje jako ostatni.
| Temperatura wrzenia °C | Składniki |
|---|---|
| -245,9 | Neon |
| -182,96 | Tlen |
| -195,8 | Azot |
| -185,7 | Argon |
Jaką masę NaCl uzyskuje się poprzez odparowanie do sucha 250 g roztworu 10%?
Którą z poniższych czynności należy wykonać, aby zapewnić wysoką dokładność pomiaru masy substancji podczas przygotowywania próbki do analizy chemicznej?
Jakie jest stężenie procentowe roztworu uzyskanego poprzez rozpuszczenie 25 g jodku potasu w 100 cm3 destylowanej wody (o gęstości 1 g/cm3)?
Przy przygotowywaniu 100 cm3 roztworu o określonym stężeniu procentowym (m/V) konieczne jest odważenie wyliczonej ilości substancji, a następnie przeniesienie jej do
Ile gramów chlorku baru powinno się rozpuścić w wodzie, aby uzyskać 200 cm3 roztworu o stężeniu 10% i gęstości 1,203 g/cm3?
Jakim kolorem oznacza się instalację gazową w laboratorium analitycznym?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Podstawowy zestaw do filtracji, oprócz statywu i sączka, obejmuje
Aby uzyskać roztwór 25 gramów CuSO4 w 50 gramach wody, konieczne jest podgrzanie mieszanki do temperatury w przybliżeniu
W tabeli przedstawiono wymiary, jakie powinny mieć oznaczenia opakowań substancji niebezpiecznych.
Korzystając z informacji w tabeli, określ minimalne wymiary, jakie powinno mieć oznaczenie dla cysterny o pojemności 32840 dm3.
| Pojemność opakowania | Wymiary (w centymetrach) |
|---|---|
| Nieprzekraczająca 3 litrów | co najmniej 5,2 x 7,4 |
| Ponad 3 litry, ale nieprzekraczająca 50 litrów | co najmniej 7,4 x 10,5 |
| Ponad 50 litrów, ale nieprzekraczająca 500 litrów | co najmniej 10,5 x 14,8 |
| Ponad 500 litrów | co najmniej 14,8 x 21,0 |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Podczas łączenia bezwodnego etanolu z wodą występuje zjawisko kontrakcji. Gdy zmieszamy 1000 cm3 wody oraz 1000 cm3 etanolu, otrzymujemy roztwór o objętości
Sposoby utrwalania i przechowywania próbek wody przeznaczonych do badań fizykochemicznych.
Próbkę wody przeznaczoną do oznaczenia zawartości metali poddaje się utrwalaniu za pomocą
| Oznaczenie | Sposób utrwalania i przechowywania |
|---|---|
| Barwa | Przechowywać w ciemności |
| Mętność | Przechowywać w ciemności |
| Twardość | pH = 3 z użyciem HNO3 |
| OWO | 0,7 ml HCl/30 ml próbki |
| ChZT | pH 1- 2 z użyciem H2SO4 |
| Fosfor | Przechowywać w temperaturze 1-5°C |
| Glin | pH 1-2 z użyciem HNO3 |
| Żelazo | pH 1-2 z użyciem HNO3 |
| Utlenialność | pH1-2 z użyciem H2SO4, Przechowywać w ciemności |
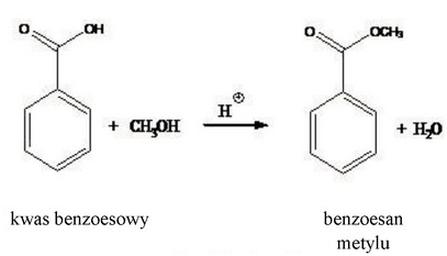
Do reakcji estryfikacji użyto 150 g kwasu benzoesowego (M = 122,12 g/mol), w wyniku której otrzymano czysty preparat benzoesanu metylu (M = 136,2 g/mol). Ile gramów benzoesanu metylu otrzymano, jeżeli reakcja przebiegała z wydajnością 92%?
Metoda przygotowania próbki do badania, która nie jest
Z podanego wykazu wybierz sprzęt potrzebny do zmontowania zestawu do sączenia pod próżnią.
| 1 | 2 | 3 | 4 | 5 | 6 |
| pompka wodna | lejek z długą nóżką | kolba okrągłodenna | kolba ssawkowa | lejek sitowy | chłodnica powietrzna |
Aby uzyskać roztwór CuSO4 o stężeniu 15%, w jakim stosunku należy połączyć roztwory 10% oraz 20%?
Fragment procedury analitycznej
(...) Przenieś badany roztwór całkowicie do rozdzielacza gruszkowego o pojemności od 50 do 100 cm3, dodaj 5 cm3 roztworu tiocyjanianu potasu oraz 10 cm3 alkoholu izopentylowego, a następnie wstrząsaj zawartością przez 30 sekund.
Po rozdzieleniu faz przenieś roztwór wodny do drugiego rozdzielacza, natomiast fazę organiczną do suchej kolbki miarowej o pojemności 50 cm3(...) Który rodzaj ekstrakcji jest opisany w powyższym fragmencie?
Odpady, które w przeważającej mierze składają się z osadów siarczków metali ciężkich, nazywa się
Na rysunku numerami rzymskimi oznaczono
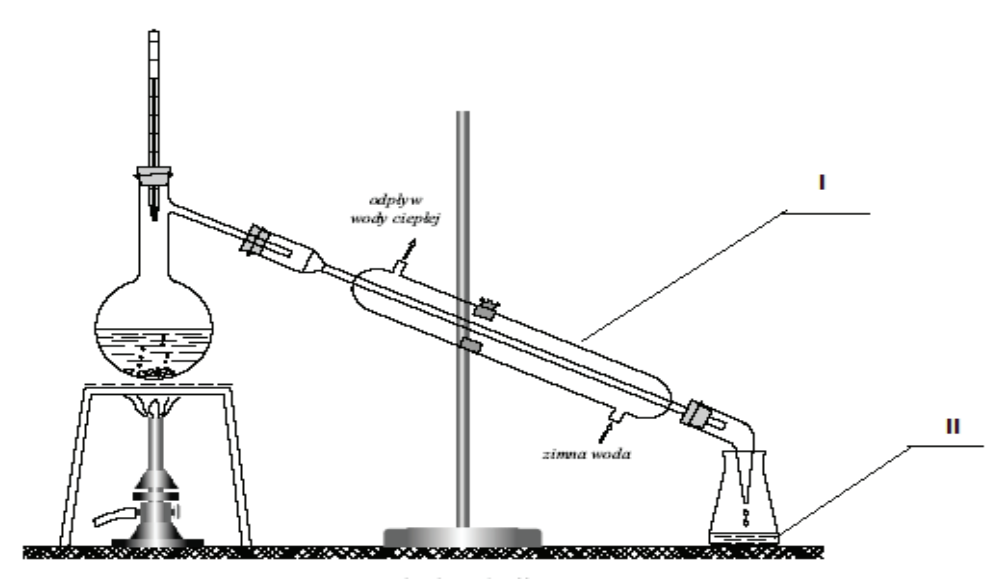
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Ekstrakcję w trybie ciągłym przeprowadza się
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Przy transporcie próbek wody zaleca się, aby próbki były
Błąd związany z odczytem poziomu cieczy w kolbie miarowej, spowodowany niewłaściwą pozycją oka w stosunku do skali, nazywany jest błędem
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Przykładem piany stałej jest
| faza rozproszona | faza rozpraszająca | ||
|---|---|---|---|
| gaz | ciecz | ciało stałe | |
| gaz | - | piana | piana stała |
| ciecz | aerozol ciekły | emulsja | emulsja stała |
| ciało stałe | aerozol stały | zol | zol stały |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na ilustracji przedstawiono sprzęt stosowany do sączenia osadu
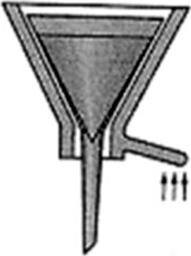
Sączenie osadów kłaczkowatych odbywa się przy użyciu sączków