Pytanie 1
Rozdział składników mieszaniny w chromatografii odbywa się dzięki ich różnym
Wynik: 1/40 punktów (2,5%)
Wymagane minimum: 20 punktów (50%)
Rozdział składników mieszaniny w chromatografii odbywa się dzięki ich różnym
Zapis "20°C" umieszczony na pipecie oznacza, że

Brak odpowiedzi na to pytanie.
Jakie urządzenie wykorzystuje się do pomiaru lepkości cieczy?
Brak odpowiedzi na to pytanie.
Na rysunku przedstawiono przyrząd do pobierania próbek

Aby uzyskać roztwór CuSO4 o stężeniu 15%, w jakim stosunku należy połączyć roztwory 10% oraz 20%?
Brak odpowiedzi na to pytanie.
W którym wierszu są zapisane nazwy wyłącznie rozpuszczalników palnych?
| Właściwości wybranych rozpuszczalników. | ||||
|---|---|---|---|---|
| Rozpuszczalnik | Gęstość [g/cm3] | Temperatura wrzenia [°C] | Temperatura zapłonu [°C] | Rozpuszczalność w wodzie [g/100 cm3] |
| Eter dietylowy | 0,71 | 35 | -45 | 7 |
| Heksan | 0,66 | 60-80 | -23 | 0,01 |
| Aceton | 0,79 | 57 | -18 | ∞ |
| Benzen | 0,88 | 80 | -11 | 0,07 |
| Chloroform | 1,49 | 61 | - | 0,82 |
| Tetrachlorometan | 1,59 | 77 | - | 0,08 |
| Etanol | 0,81 | 78 | 12 | ∞ |
| Chlorometan | 1,34 | 41 | - | 2 |
Brak odpowiedzi na to pytanie.
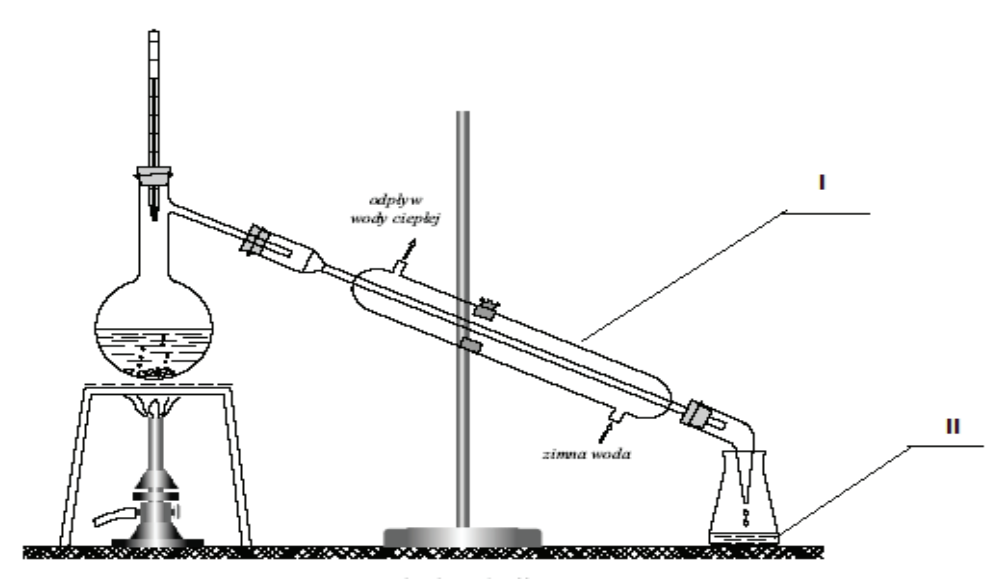
Na rysunku numerami rzymskimi oznaczono
Brak odpowiedzi na to pytanie.
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
Brak odpowiedzi na to pytanie.
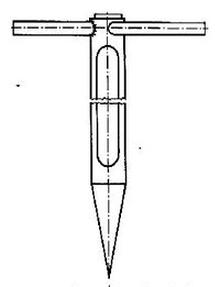
Przyrząd przedstawiony na rysunku służy do pobierania próbek substancji
Brak odpowiedzi na to pytanie.
W przypadku odczynnika, w którym nawet najczulsze techniki analizy chemicznej nie są w stanie wykryć zanieczyszczeń, a jego badanie wymaga zastosowania metod opartych na zjawiskach fizycznych, zalicza się on do kategorii czystości
Brak odpowiedzi na to pytanie.
W celu uzyskania 500 g mieszaniny oziębiającej o temperaturze -18oC należy zmieszać
| Tabela. Mieszaniny oziębiające | ||
|---|---|---|
| Temperatura mieszaniny [°C] | Skład mieszaniny | Stosunek masowy |
| -2 | Woda + chlorek amonu | 10 : 3 |
| -15 | Woda + rodanek amonu | 10 : 13 |
| -18 | Lód + chlorek amonu | 10 : 3 |
| -21 | Lód + chlorek sodu | 3 : 1 |
| -22 | Lód + chlorek amonu + azotan(V) amonu | 25 : 5 : 11 |
| -25 | Lód + azotan(V) amonu | 1 : 1 |
Brak odpowiedzi na to pytanie.
Aby w badanej próbie w trakcie zmiany pH nastąpiła zmiana barwy na malinową, należy użyć
| Zmiany barw najważniejszych wskaźników kwasowo-zasadowych | ||||
|---|---|---|---|---|
| Wskaźnik | Barwa w środowisku | Zakres pH zmiany barwy | ||
| Kwasowym | Obojętnym | Zasadowym | ||
| oranż metylowy | czerwona | żółta | żółta | 3,2÷4,4 |
| lakmus (mieszanina substancji) | czerwona | fioletowa | niebieska | 4,5÷8,2 |
| fenoloftaleina | bezbarwna | bezbarwna | malinowa | 8,2÷10,0 |
| wskaźnik uniwersalny (mieszanina substancji) | czerwona (silnie kwaśne) pomarańczowa (słabo kwaśne) | żółta | niebieska (silnie zasadowe) zielona (słabo zasadowe) | co jeden stopień skali |
| herbata | żółta | czerwona-brunatna | brązowa | |
| sok z czerwonej kapusty | fioletowa | niebieska | zielona | |
Brak odpowiedzi na to pytanie.
Zaleca się schładzanie próbek wody transportowanych do laboratorium do temperatury
Brak odpowiedzi na to pytanie.
Które spośród substancji wymienionych w tabeli pozwolą pochłonąć wydzielający się tlenek węgla(IV)?
| I | II | III | IV | V |
|---|---|---|---|---|
| Ca(OH)2(aq) | NaOH(s) | HNO3(stęż) | CuO(s) | CaO(s) |
Brak odpowiedzi na to pytanie.
Aby przygotować mianowany roztwór KMnO4, należy odważyć wysuszone Na2C2O4 o masie zbliżonej do 250 mg, z dokładnością wynoszącą 1 mg. Jaką masę powinna mieć prawidłowo przygotowana odważka?
Brak odpowiedzi na to pytanie.
Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Brak odpowiedzi na to pytanie.
Którego związku chemicznego, z uwagi na jego silne właściwości higroskopijne, nie powinno się używać w analizie miareczkowej jako substancji podstawowej?
Brak odpowiedzi na to pytanie.
W laboratorium chemicznym przewody instalacji rurowych są oznaczane różnymi kolorami, zgodnie z obowiązującymi normami. Polska Norma PN-70 N-01270/30 określa kolor dla wody jako
Brak odpowiedzi na to pytanie.
Zestaw do filtracji nie zawiera
Brak odpowiedzi na to pytanie.
Jakie jest pH 0,001-molowego roztworu NaOH?
Brak odpowiedzi na to pytanie.
Na podstawie danych w tabeli określ, jaką masę próbki należy pobrać, jeżeli wielkość ziarna wynosi 1·10-5 m.
| Wielkość ziaren lub kawałków [mm] | Poniżej 1 | 1-10 | 11-50 | Ponad 50 |
|---|---|---|---|---|
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Brak odpowiedzi na to pytanie.
Metoda przygotowania próbki do badania, która nie jest
Brak odpowiedzi na to pytanie.
Proces nastawiania miana kwasu solnego na wodorowęglan potasu KHCO3 przebiega zgodnie z następującą instrukcją:
Na wadze analitycznej odmierzyć 1 g KHCO3 (z precyzją 0,00001 g) i przesypać go ilościowo do kolby stożkowej, dodać około 50 cm3 destylowanej wody i dokładnie wymieszać roztwór. Następnie dodać kilka kropel roztworu czerwieni metylowej. Przeprowadzić miareczkowanie kwasem aż do pierwszej zmiany koloru wskaźnika.
W tym przypadku titrantem jest
Brak odpowiedzi na to pytanie.
Co oznacza skrót AKT?
Brak odpowiedzi na to pytanie.
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
Brak odpowiedzi na to pytanie.
Aby przygotować 200 g roztworu chlorku potasu o stężeniu 5% (m/m), ile substancji należy zastosować?
Brak odpowiedzi na to pytanie.
Próbka wzorcowa to próbka
Brak odpowiedzi na to pytanie.
Osoba pracująca z lotnym rozpuszczalnikiem straciła przytomność. Jakie działania należy podjąć, aby udzielić pierwszej pomocy?
Brak odpowiedzi na to pytanie.
Aby uzyskać całkowicie bezwodny Na2CO3, przeprowadzono prażenie 143 g Na2CO3·10H2O (M = 286 g/mol). Po upływie zalecanego czasu prażenia odnotowano utratę masy 90 g. W związku z tym prażenie należy
Brak odpowiedzi na to pytanie.
Reagenty o najwyższej czystości to reagenty
Brak odpowiedzi na to pytanie.
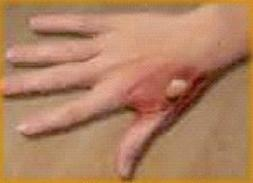
Zdjęcie przedstawia oparzenie cieplne
Brak odpowiedzi na to pytanie.
Substancje utleniające opisuje piktogram

Brak odpowiedzi na to pytanie.
Woda, która została poddana dwukrotnej destylacji, to woda
Brak odpowiedzi na to pytanie.
Na podstawie zamieszczonych w tabeli opisów metod rozdzielania mieszanin, dobierz odpowiadające im nazwy.
| Tabela. Metody rozdzielania mieszanin | |
|---|---|
| Lp. | Opis metody |
| I. | Zlewanie cieczy znad osadu. |
| II. | Przeprowadzenie ciekłego rozpuszczalnika w stan pary. |
| III. | Wyodrębnianie z mieszaniny ciał stałych lub cieczy składnika przy pomocy rozpuszczalnika tak dobranego, aby rozpuszczał żądany związek chemiczny. |
| IV. | Powolne opadanie cząstek substancji stałej w cieczy pod wpływem własnego ciężaru. |
Brak odpowiedzi na to pytanie.
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
Brak odpowiedzi na to pytanie.
Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Brak odpowiedzi na to pytanie.
Jak definiuje się próbkę wzorcową?
Brak odpowiedzi na to pytanie.
Deminimalizowaną wodę można uzyskać przez
Brak odpowiedzi na to pytanie.
Jakim przyrządem nie jest możliwe określenie gęstości cieczy?
Brak odpowiedzi na to pytanie.
Na zdjęciu przedstawiono proces

Brak odpowiedzi na to pytanie.