Pytanie 1
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
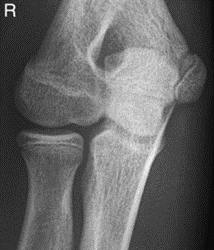
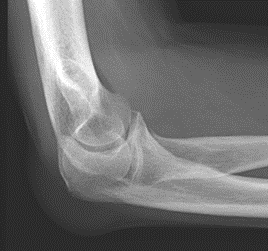
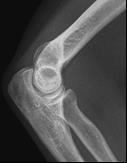
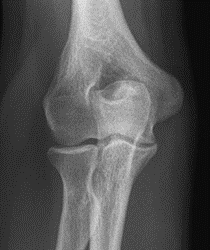
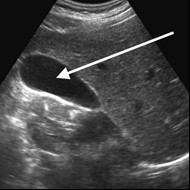
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Obiektywną metodą badania słuchu jest audiometria
W radiografii mianem SID określa się
Zwiększenie napięcia na lampie rentgenowskiej powoduje
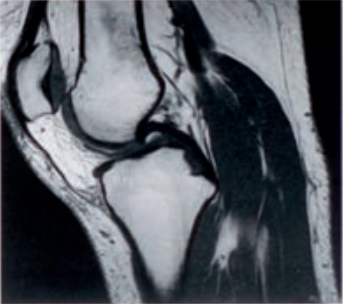
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
Do planowego badania TK klatki piersiowej z użyciem środka cieniującego pacjent powinien zgłosić się
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm × 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W radiologii stomatologicznej ząb o numerze 23 to kieł
Pielografia to badanie układu
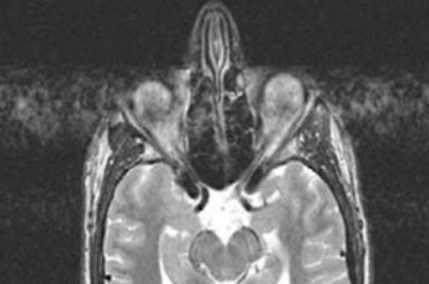
Co jest przyczyną artefaktu widocznego na obrazie MR?
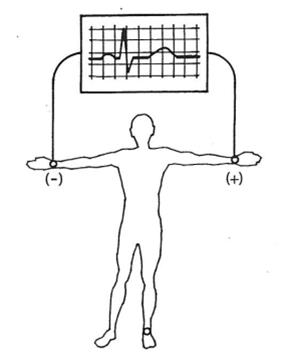
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
Rytm alfa i beta rejestruje się podczas badania
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
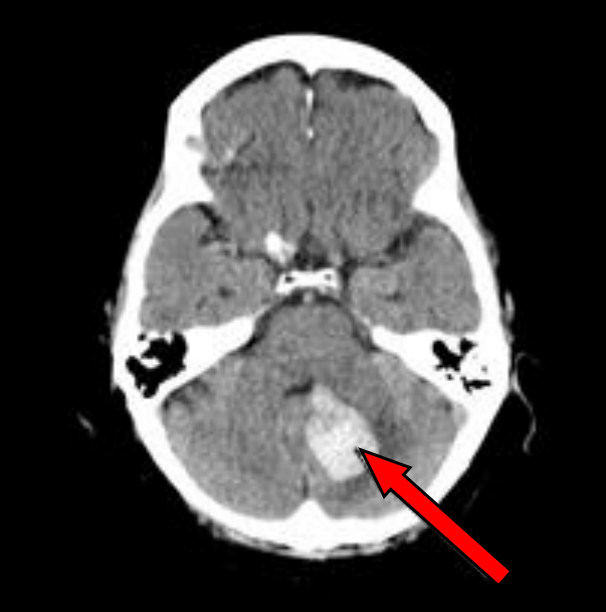
Na przekroju poprzecznym TK mózgu strzałką wskazano obszar
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
Które urządzenia pomocnicze służą do unieruchomienia pacjenta do zabiegu radioterapii?
Rytm alfa i beta rejestruje się podczas badania
Promieniowanie jonizujące pośrednio to
Ligand stosuje się
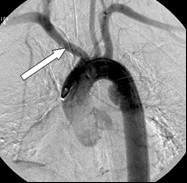
Na obrazie cyfrowej angiografii subtrakcyjnej strzałką zaznaczono
Ultrasonograficzne środki kontrastowe to
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W zapisie EKG zespół QRS odzwierciedla
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
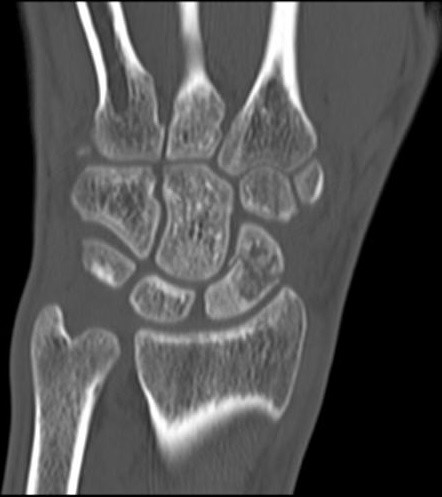
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
Chorobą układu oddechowego typu obturacyjnego jest
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy