Pytanie 1
W oparciu o wyniki analizy zamieszczone w tabeli wskaż, który kation był obecny w roztworze badanej próbki.
| Odczynnik | Wynik |
|---|---|
| HCl | Brak osadu |
| NaOH | Brunatny koloidalny osad |
| KSCN | Krwistoczerwone zabarwienie roztworu |
Wynik: 39/40 punktów (97,5%)
Wymagane minimum: 20 punktów (50%)
W oparciu o wyniki analizy zamieszczone w tabeli wskaż, który kation był obecny w roztworze badanej próbki.
| Odczynnik | Wynik |
|---|---|
| HCl | Brak osadu |
| NaOH | Brunatny koloidalny osad |
| KSCN | Krwistoczerwone zabarwienie roztworu |
W jakich oznaczeniach analitycznych wykorzystuje się fenoloftaleinę jako wskaźnik?
Na rysunkach przedstawiono serie pomiarów o różnej dokładności i precyzji (środek najmniejszego okręgu oznacza wartość prawdziwą). Serię pomiarów nieprecyzyjnych, ale dokładnych, przedstawiono na rysunku
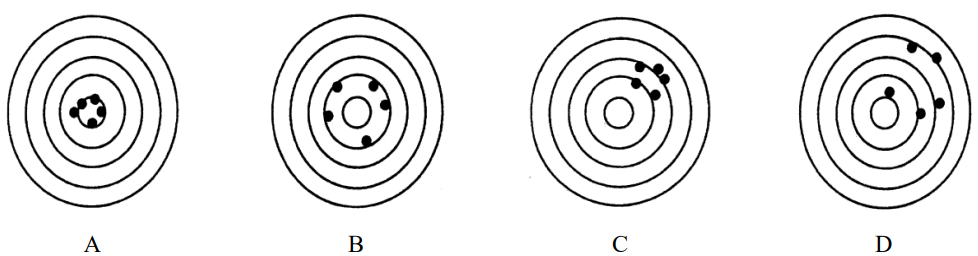
Określenie stężenia jonów Fe3+ w wodzie pitnej powinno być zrealizowane przy użyciu metody
W procesie oddzielania osadu od cieczy podczas realizacji analiz jakościowych metodą półmikro, używa się
Na ilustracji przedstawiono bieg promieni świetlnych
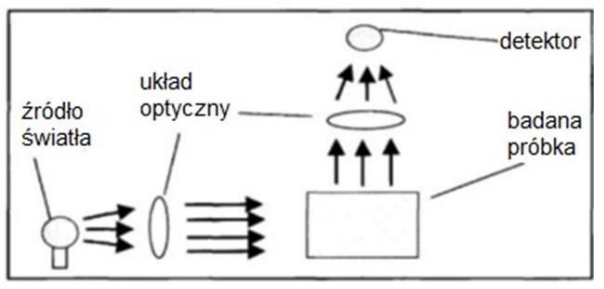
Zjawisko, w którym obce jony są mechanicznie zatrzymywane przez szybko rosnący kryształ, określane jest mianem
Przedstawiony na rysunku zestaw jest stosowany podczas oznaczania
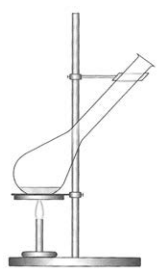
Liczba wskazująca ilość (w mg) KOH potrzebną do zneutralizowania wolnych kwasów tłuszczowych obecnych w badanym tłuszczu, to liczba
W procedurze analitycznej zapisano:
Ile wynosi zawartość procentowa Na2B4O7·10H2O w badanej próbce boraksu, jeżeli na zmiareczkowanie 0,3 g próbki zużyto 15,4 cm3 roztworu NaOH?
| 1 cm3 roztworu NaOH o stężeniu 0,1 mol/dm3 odpowiada 19,07 mg tetraboranu sodu Na2B4O7 · H2O |
Wskaź kationy, które są możliwe do wykrycia poprzez próbę płomieniową?
Na rysunku przedstawiono schemat blokowy
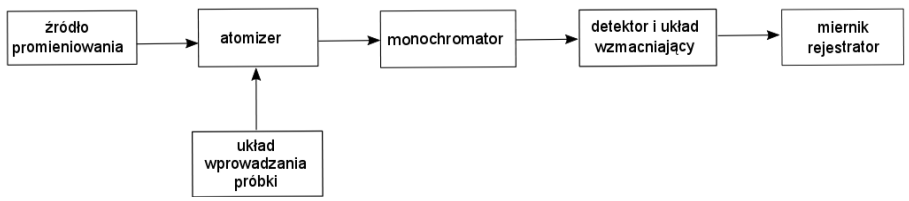
Reakcja ksantoproteinowa umożliwia identyfikację aminokwasu, który zawiera w swojej budowie
Do oznaczania stężenia nadtlenku wodoru w roztworze wody utlenionej jako titrant wykorzystuje się roztwór o znanym mianie
Skalę wzorców do oznaczenia zawartości ołowiu przygotowano w cylindrach Nesslera o pojemności 100 cm3. Zawartość ołowiu oznaczona w tabeli jako X wynosi
| Ilość wzorcowego roztworu roboczego ołowiu w cm3 | 0,0 | 0,5 | 1,0 | 2,0 | 3,0 |
| Zawartość ołowiu w mg | 0,0 | 0,005 | X | 0,020 | 0,030 |
Aby określić wartość absorbancji substancji X, zmierzono, przy tych samych długościach fali, absorbancję mieszaniny X i Y oraz osobno substancji Y.
Jeśli AX+Y = 0,84, a AY = 0,56, to jaka jest wartość AX?
Na rysunku przedstawiono wykonanie analizy metodą
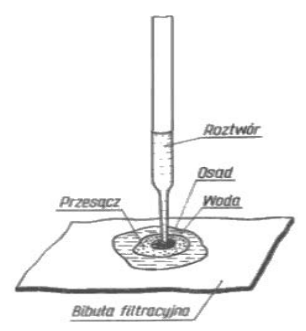
Skręcalność optyczną cukrów mierzy się przy użyciu
Do kationów trzeciej grupy analitycznej, wytrącanych w postaci siarczków roztworem AKT w środowisku amoniakalnym, należą:
| A. Ba2+, Ca2+, Sr2+ |
| B. Fe2+, Mg2+, Pb2+, Al3+, Ca2+ |
| C. Ni2+, Co2+, Fe2+, Fe3+, Mn2+, Zn2+ |
| D. Pb2+, Cu2+, Cd2+, Cr3+, Ag+, K+, Al3+ |
Na rysunku przedstawiono schemat aparatury do oznaczania w wodzie
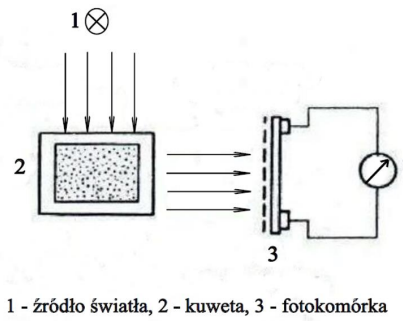
Część opisu skutków analizy
(...) generuje kation jednowartościowy, a sole powstałe z tym kationem to w przeważającej mierze substancje trudnorozpuszczalne. Większość jego soli jest bezbarwna. Ten bezbarwny jon ma zdolność do tworzenia jonów kompleksowych, na przykład z tiosiarczanem sodowym. Związki tego kationu są wrażliwe na światło (ciemnieją pod jego działaniem), dlatego powinny być przechowywane w pojemnikach z ciemnego szkła (...) Z opisu wynika, że w analizowanym surowcu jakościowo oznaczano kation
Do analizy pobrano próbkę o masie 200 mg. Na podstawie informacji zamieszczonych w tabeli określ, w której skali będzie wykonana ta analiza.
| Wielkość próbki | Skala analizy |
|---|---|
| > 0,1 g | makro |
| 0,01 – 0,1 g | semimikro |
| 0,0001 – 0,01 g | mikro |
| < 10-4 g | ultramikro |
Na schemacie przedstawiono bieg promieni świetlnych
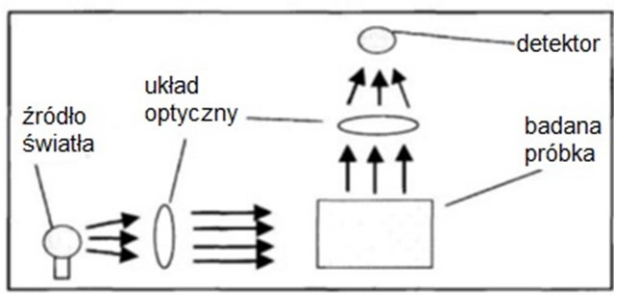
Sprzyja tworzeniu osadów grubokrystalicznych w czystszej formie oraz umożliwiających łatwiejsze sączenie
Ile miligramów wapnia (MCa = 40,0 g/mol) znajdowało się w analizowanym roztworze, jeśli do zmiareczkowania próbki wykorzystano 20 cm3 0,0100-molowego roztworu EDTA?
Na podstawie informacji zawartych w tabeli wskaż, który adsorbent należy zastosować podczas oznaczania karotenów.
| Podział adsorbentów według zastosowania | |
|---|---|
| Adsorbent | Przykłady zastosowania |
| Tlenek glinu zasadowy | aminy, węglowodory, alkaloidy, zasady heterocykliczne |
| Tlenek glinu obojętny | aminy, amidy, alkaloidy, glikozydy |
| Tlenek glinu kwasowy | barwniki, związki kwasowe |
| Żel krzemionkowy | aminy, kwasy karboksylowe, amidy, węglowodory, inne związki obojętne |
Jakie urządzenia są wykorzystywane do segregacji materiału na frakcje, które zawierają ziarna o różnych rozmiarach?
Na rysunku przedstawiono schemat aparatury do
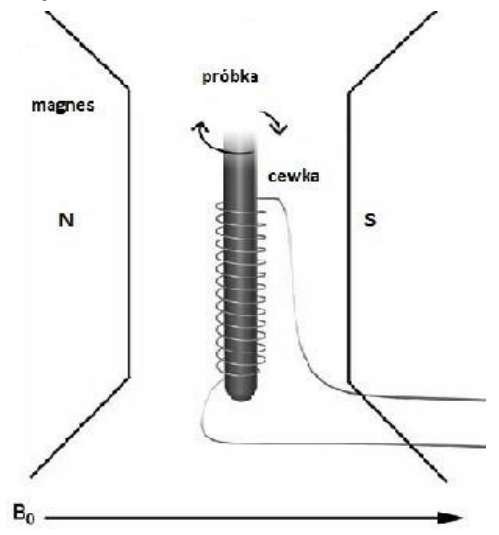
Na podstawie zamieszczonego schematu ilustrującego przeprowadzone badania wskaż, jaką barwę przyjmie roztwór w probówce oznaczonej numerem 2.
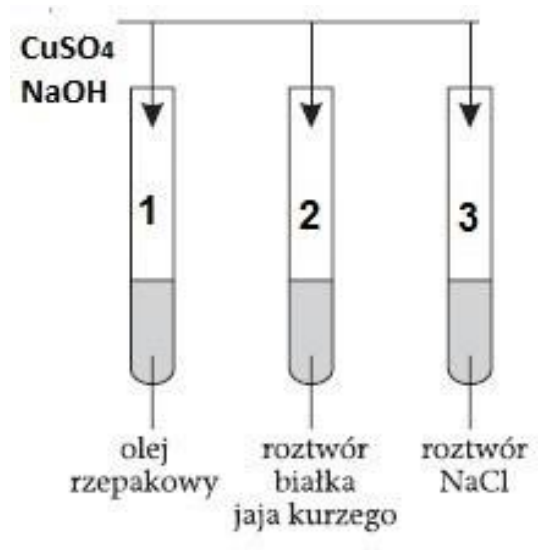
Na schemacie przedstawiono oznaczanie mieszaniny
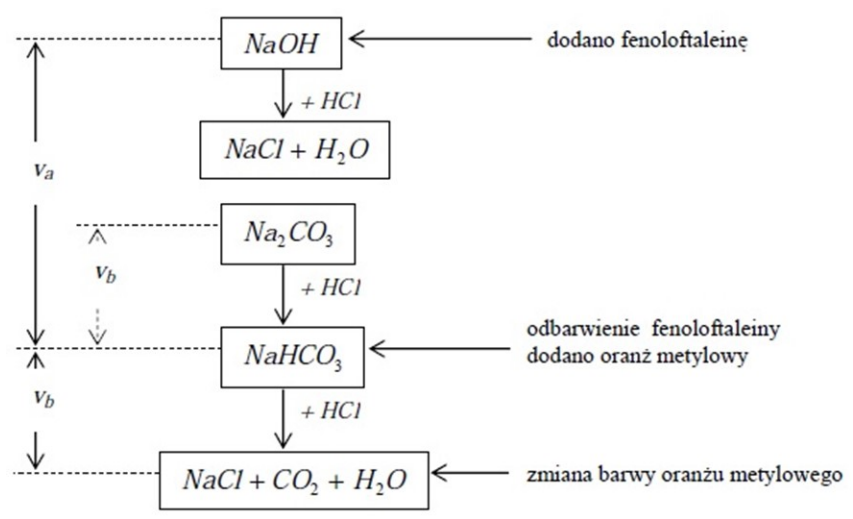
Na ilustracji przedstawiono

Jakie składniki odżywcze w żywności są identyfikowane za pomocą odczynników Fehlinga I i II?
Wykonano jodometryczne oznaczenie zawartości kwasu askorbinowego dla 4 próbek tabletek witaminy C, uzyskując wyniki. Na podstawie informacji zawartych w opisie i wyników analizy można stwierdzić, że zawartość witaminy C
| Opis Na opakowaniach tabletek witaminy C producenci deklarują zawartość 200 mg kwasu askorbinowego. Zgodnie z normą odchylenia od deklarowanej zawartości substancji leczniczej nie mogą przekraczać ±10% dla tabletek o zawartości poniżej 100 mg i ±5% dla tabletek o deklarowanej zawartości 100 mg i więcej. | ||||
| Próbka | 1 | 2 | 3 | 4 |
| Zawartość kwasu askorbinowego | 198,5 mg | 211 mg | 201 mg | 205 mg |
Podczas reakcji ksantoproteinowej obecność białka jest potwierdzana przez zmianę koloru na żółty, co wskazuje na obecność w białku
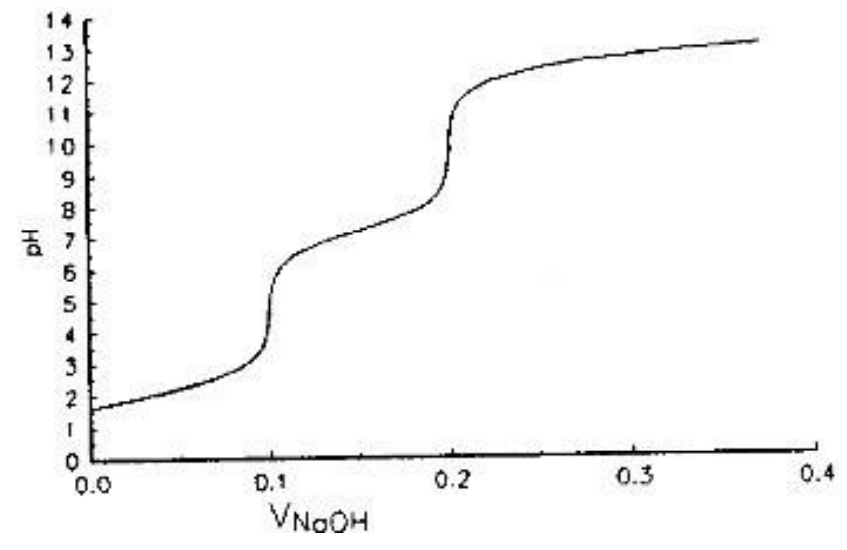
Przedstawiona na rysunku krzywa miareczkowania jest charakterystyczna dla
Posługując się wagą techniczną o dokładności 0,1 g, odważono trzy próbki stopu żelaza. Masy stopów żelaza wynosiły odpowiednio:
Próbka 1 — masa 100 g Próbka 2 — masa 10 g Próbka 3 — masa 1 g Obliczone błędy względne oznaczenia wynoszą:
| Próbka 1 | Próbka 2 | Próbka 3 | |
|---|---|---|---|
| A. | 0,1% | 1% | 10% |
| B. | 10% | 1% | 0,1% |
| C. | 1% | 1% | 1% |
| D. | 0,1% | 0,1% | 0,1% |
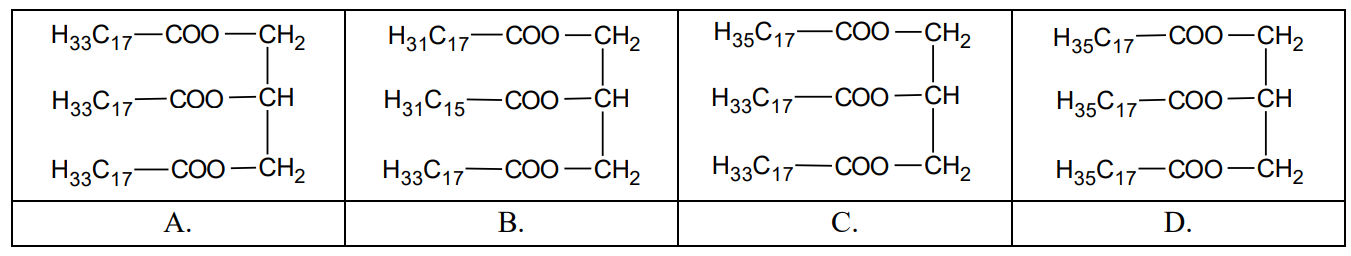
Próbkę tłuszczu poddano reakcji z wodą bromową. Nie zaobserwowano zmian. Wskaż wzór tłuszczu, który mógł znajdować się w tej próbce.
Gdzie wykorzystuje się efekt Tyndalla?
Jaką objętość rozcieńczalnika zużyto na przygotowanie wskazanego w opisie rozcieńczenia próbki mleka?
| Wykonać dziesiętne rozcieńczenia mleka z 10 cm3 próbki. Pierwsze rozcieńczenie wykonać w kolbie o pojemności 250 cm3: do 90 cm3 rozcieńczalnika dodać 10 cm3 próby, dokładnie wymieszać; z tego rozcieńczenia pobrać 0,5 cm3 i przenieść do 4,5 cm3 rozcieńczalnika. Postępować w ten sam sposób, aż do uzyskania rozcieńczenia 1:100000. |
Czym jest płyn Lugola?