Pytanie 1
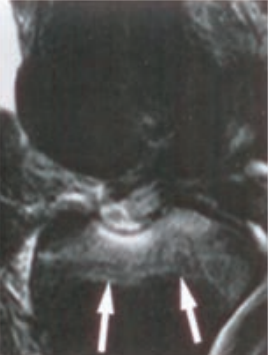
Obraz stawu kolanowego otrzymano metodą
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Obraz stawu kolanowego otrzymano metodą

W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Zamieszczone obrazy związane są z badaniem
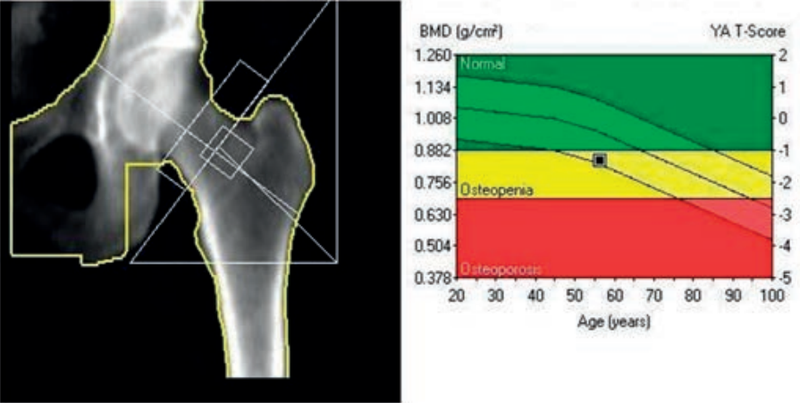
Warstwa półchłonna (WP) służy do obliczania
Na obrazie radiologicznym uwidoczniono złamanie kości
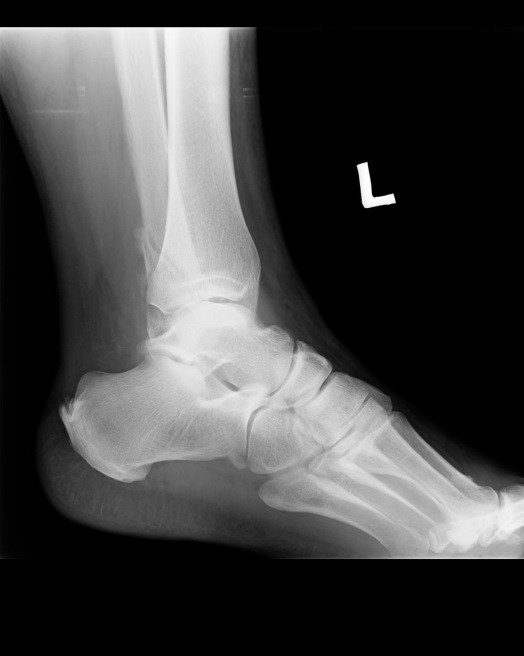
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
Obrazy DDR są tworzone w trakcie
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Promieniowanie jonizujące pośrednio to
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Powierzchnia gabinetu rentgenowskiego, w którym zainstalowany jest aparat rentgenowski wyposażony w oddzielną lampę, nie może być mniejsza niż
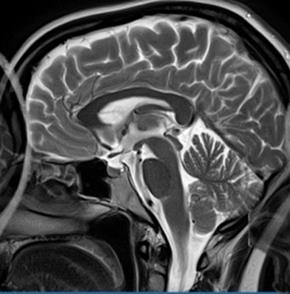
Na obrazie rezonansu magnetycznego głowy strzałką wskazano zatokę
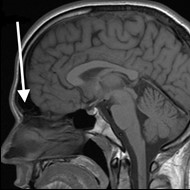
Jednostką indukcji magnetycznej jest
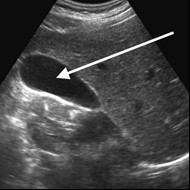
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
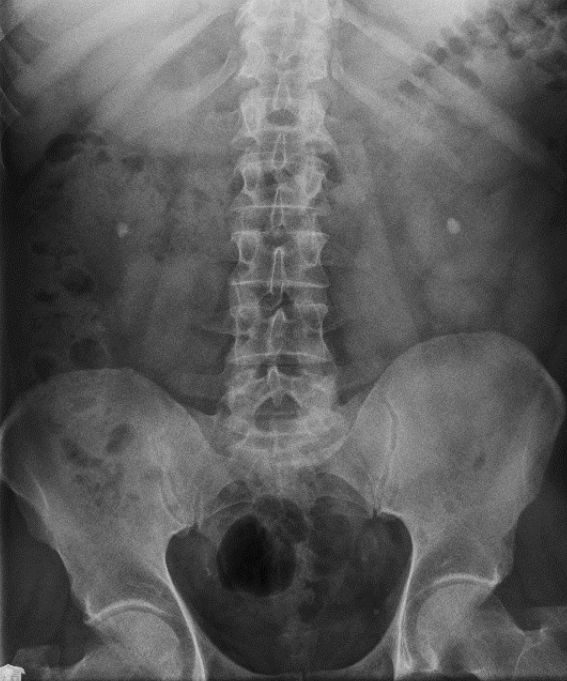
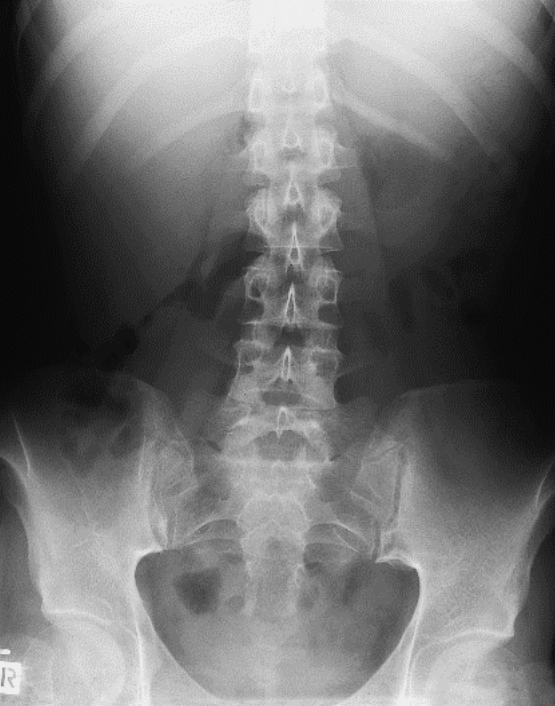
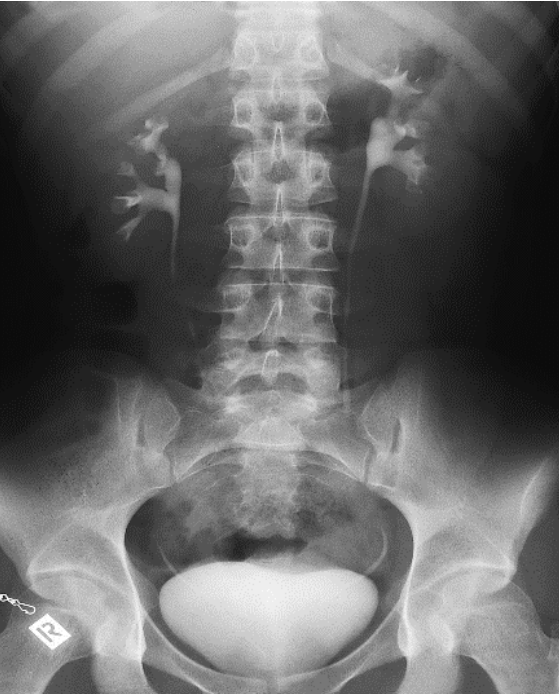
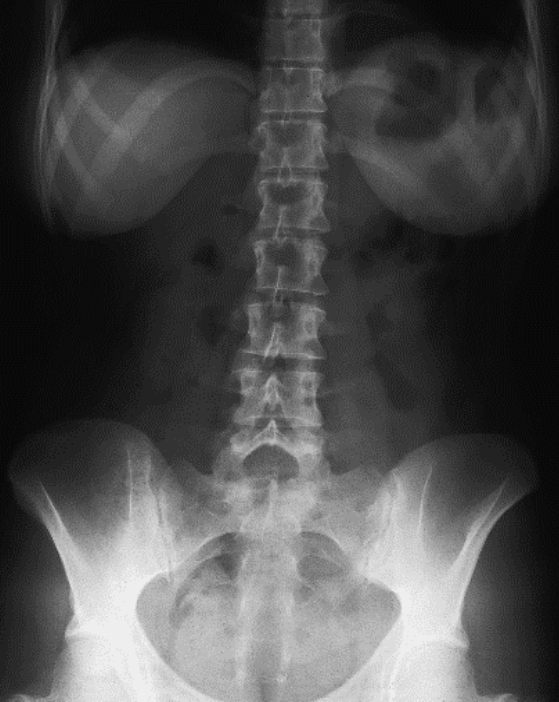
Na którym radiogramie uwidoczniona jest kamica nerkowa?
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Na ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
W medycynie nuklearnej wykorzystuje się:
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
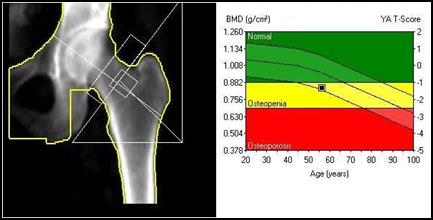
Zamieszczone na ilustracji obrazy dotyczą badania
Który radioizotop jest emiterem promieniowania alfa?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
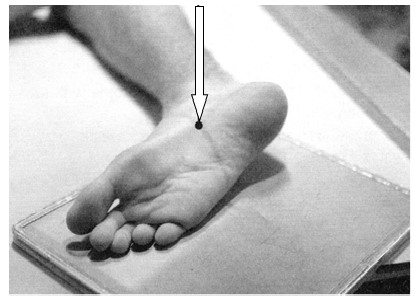
W badaniu EKG elektrodę przedsercową V4 należy umocować
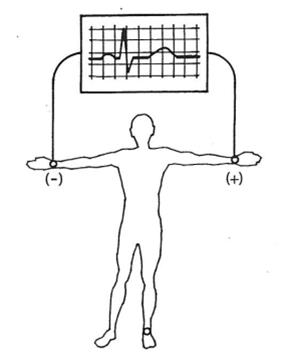
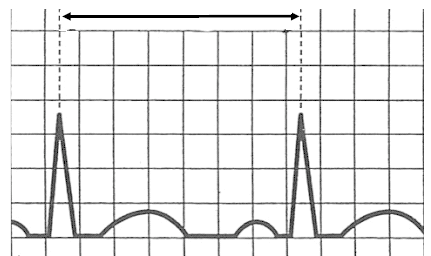
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
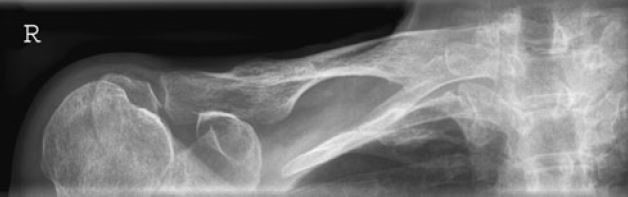
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
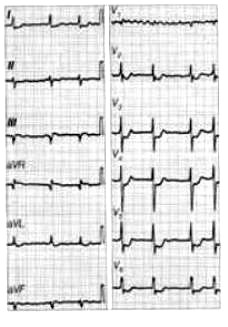
Na elektrokardiogramie uwidoczniono
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
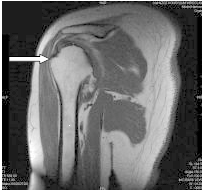
Na schemacie oznaczono
Do badania MR nadgarstka pacjenta należy ułożyć
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu
Lordoza to fizjologiczna krzywizna kręgosłupa występująca