Pytanie 1
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Sączków o najmniejszych średnicach, nazywanych "twardymi" i oznaczonych kolorem niebieskim, używa się do filtracji osadów?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Czystość konkretnego odczynnika chemicznego wynosi: 99,9-99,99%. Jakiego rodzaju jest ten odczynnik?
Z podanych w tabeli danych wybierz sprzęt potrzebny do zmontowania zestawu do destylacji z parą wodną.
| 1 | 2 | 3 | 4 | 5 |
| manometr | kociołek miedziany | chłodnica powietrzna | kolba destylacyjna | odbieralnik |
Skalę wzorców do oznaczenia barwy przygotowano w cylindrach Nesslera o pojemności 100 cm3. Barwa oznaczona w tabeli jako X wynosi
| Skala wzorców do barwy | ||||
|---|---|---|---|---|
| Ilość wzorcowego roztworu podstawowego cm3 (c=500 mg Pt/dm3) | 0 | 1,0 | 2,0 | 3,0 |
| Barwa w stopniach mg Pt/dm3 | 0 | 5 | X | 15 |
Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
Który symbol literowy umieszczany na naczyniach miarowych wskazuje na kalibrację do "wlewu"?
Jaką metodą nie można rozdzielać mieszanin?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jaką masę chlorku sodu można znaleźć w 150 g roztworu soli o stężeniu 5% (m/m)?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Roztwór o dokładnej masie z odważki analitycznej powinien być sporządzony
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Ile gramów chlorku baru powinno się rozpuścić w wodzie, aby uzyskać 200 cm3 roztworu o stężeniu 10% i gęstości 1,203 g/cm3?
Jakiego koloru nabierze lakmus w roztworze NaOH?
Jakie jest stężenie procentowe roztworu uzyskanego poprzez rozpuszczenie 25 g jodku potasu w 100 cm3 destylowanej wody (o gęstości 1 g/cm3)?
Na rysunku numerem 3 oznaczono
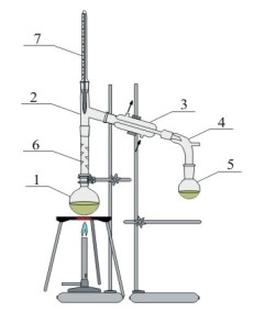
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Gęstość próbki cieczy wyznacza się przy użyciu
Wapno palone uzyskuje się poprzez prażenie wapienia według równania: CaCO3 → CaO + CO2. Ile kilogramów wapienia należy zastosować, aby w efekcie jego prażenia otrzymać 7 kg wapna palonego, jeśli wydajność reakcji wynosi 50%?
Masy molowe: MCa = 40 g/mol, MC = 12 g/mol, MO = 16 g/mol.
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Aspirator jest urządzeniem wykorzystywanym do pobierania próbek
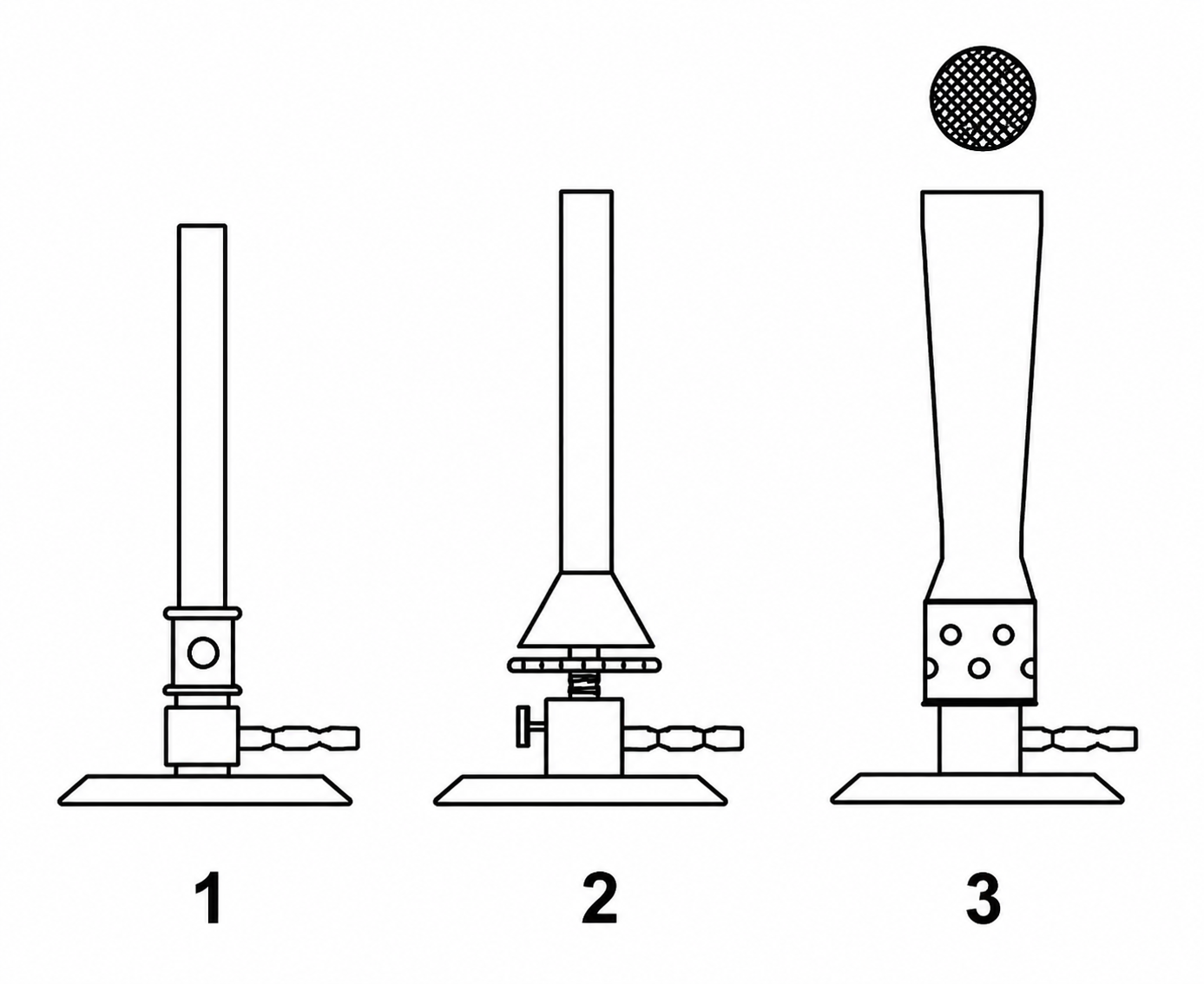
Rysunek przedstawia palniki
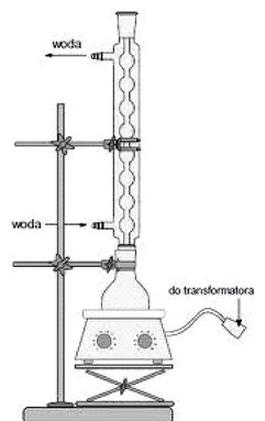
Na rysunku przedstawiono zestaw
Na rysunku przedstawiono próbnik do pobierania próbek

Do rozpuszczania próbek wykorzystuje się wodę królewską, która stanowi mieszaninę stężonych kwasów
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Proces nitrowania najczęściej realizuje się, stosując organiczny substrat
Aby uzyskać całkowicie bezwodny Na2CO3, przeprowadzono prażenie 143 g Na2CO3·10H2O (M = 286 g/mol). Po upływie zalecanego czasu prażenia odnotowano utratę masy 90 g. W związku z tym prażenie należy
Który z wymienionych roztworów NaOH, o określonych stężeniach, nie jest roztworem mianowanym?
W celu uzyskania czystej substancji próbkę zawierającą nitroanilinę poddano krystalizacji. Oblicz masę odważki nitroaniliny, pobranej do krystalizacji, jeśli uzyskano 1,5 g czystego związku, a wydajność krystalizacji wynosiła 75%.
Na podstawie zamieszczonych informacji, wskaż ilości odczynników, które są niezbędne do przygotowania skali wzorców do kolorymetrycznego oznaczania rozpuszczalnych fosforanów(V).
| Przygotowanie skali wzorców do kolometrycznego oznaczania fosforanów(V) | ||||||||
| Do ośmiu cylindrów Nesslera o pojemności 100 cm3 odmierzyć kolejno wzorcowy roztwór roboczy KH2PO4 według poniższej tabeli SKALA WZORCÓW (PO43-) i uzupełnić wodą do kreski. Do każdego cylindra dodać 2 cm3 roztworu molibdenianu amonu (heksaamonoheptamolibdenian(VI)), wymieszać, dodać 0,2 cm3 roztworu SnCl2 i ponownie wymieszać. | ||||||||
| SKALA WZORCÓW (PO43-) | ||||||||
| Wzorcowy roztwór roboczy [cm3] | 0,0 | 0,5 | 1,0 | 2,0 | 3,0 | 5,0 | 7,0 | 10,0 |
| Zawartość PO43- [mg] | 0,0 | 0,005 | 0,01 | 0,02 | 0,03 | 0,05 | 0,07 | 0,10 |
| Roztwór | KH₂PO₄ | (NH₄)₆Mo₇O₂₄ | SnCl₂ |
|---|---|---|---|
| A. | 28,5 cm³ | 8,0 cm³ | 0,16 cm³ |
| B. | 0,285 cm³ | 16,0 cm³ | 1,6 cm³ |
| C. | 28,5 cm³ | 16,0 cm³ | 1,6 cm³ |
| D. | 0,285 cm³ | 8,0 cm³ | 16 cm³ |
Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
Z partii materiału należy pobrać ogólną próbkę w ilości odpowiadającej promilowi całej partii. Na podstawie podanej informacji określ, ile pierwotnych próbek, każda ważąca 10 g, trzeba pobrać z partii cukru o masie 0,5 t, aby uzyskać reprezentatywną próbkę ogólną?
Jakie metody można zastosować do rozdzielania i koncentracji składników próbki?
Aparat przedstawiony na ilustracji służy do

Na podstawie danych w tabeli określ, dla oznaczania którego parametru zalecaną metodą jest chromatografia jonowa.
| Parametr | Metoda podstawowa |
|---|---|
| pH | metoda potencjometryczna, kalibracja przy zastosowaniu minimum dwóch wzorców o pH zależnym od wartości oczekiwanych w próbkach wody |
| azotany(V) | chromatografia jonowa |
| fosforany(V) | spektrofotometria |
| Na, K, Ca, Mg | AAS (spektrometria absorpcji atomowej) |
| zasadowość | miareczkowanie wobec fenoloftaleiny oraz oranżu metylowego |
| tlen rozpuszczony, BZT₅ | metoda potencjometryczna |
Podczas pobierania próby wody do oznaczania metali ciężkich zaleca się stosowanie butelek wykonanych z: