Pytanie 1
W której pozycji wykonuje się zdjęcie jamy brzusznej u pacjenta z podejrzeniem perforacji żołądka?
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
W której pozycji wykonuje się zdjęcie jamy brzusznej u pacjenta z podejrzeniem perforacji żołądka?
Więzka promieniowania X to
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
W których projekcjach wykonuje się standardowe badanie mammograficzne?
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Jak oznacza się w systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej?
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
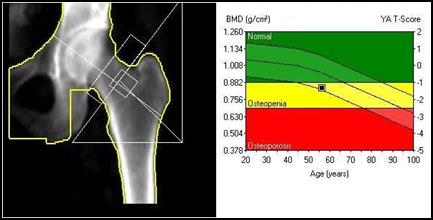
Zamieszczone na ilustracji obrazy dotyczą badania
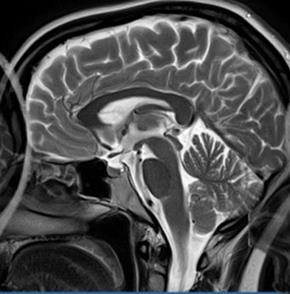
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
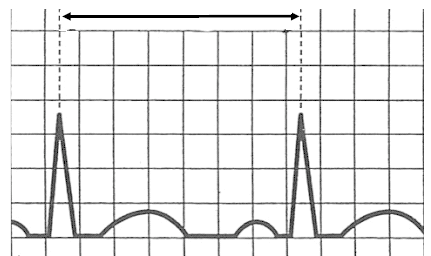
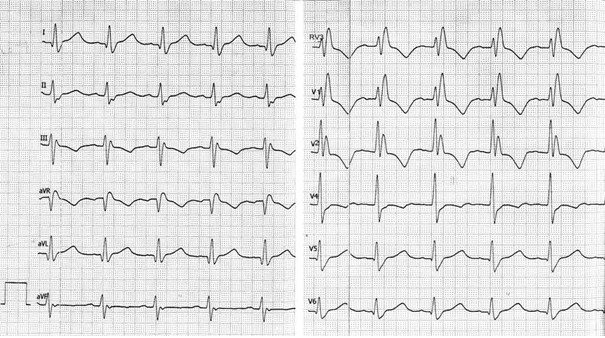
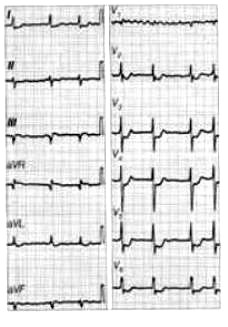
Przedstawiony zapis elektrokardiograficzny może wskazywać na
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
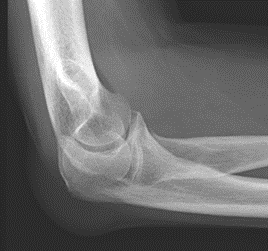
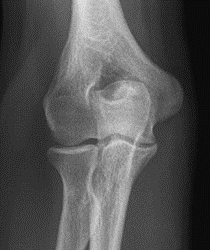
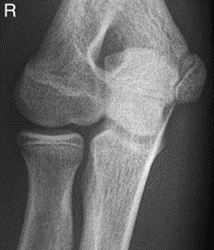
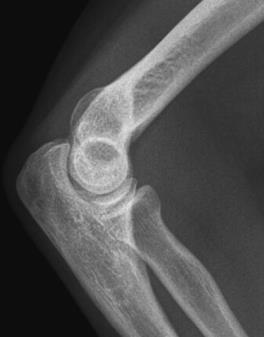
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
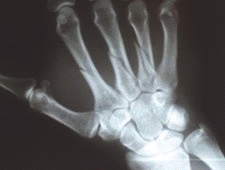
Na radiogramie uwidoczniono złamanie
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
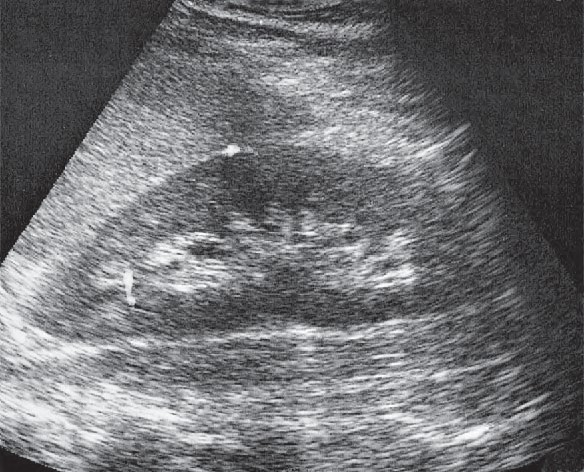
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
Na elektrokardiogramie uwidoczniono
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Urografia polega na
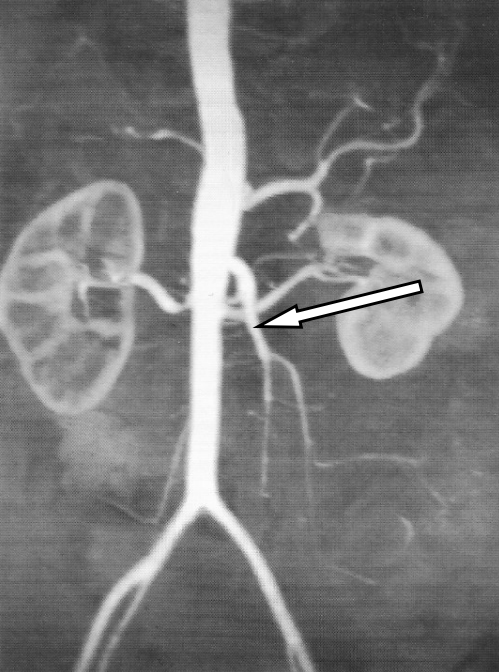
Którą tętnicę zaznaczono strzałką na obrazie MR?
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
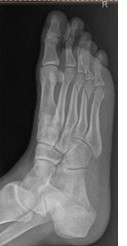
Na rentgenogramie stopy uwidocznione jest złamanie
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
Jaki jest cel stosowania bolusa w radioterapii?
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
W obrazowaniu MR wykorzystuje się moment magnetyczny
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
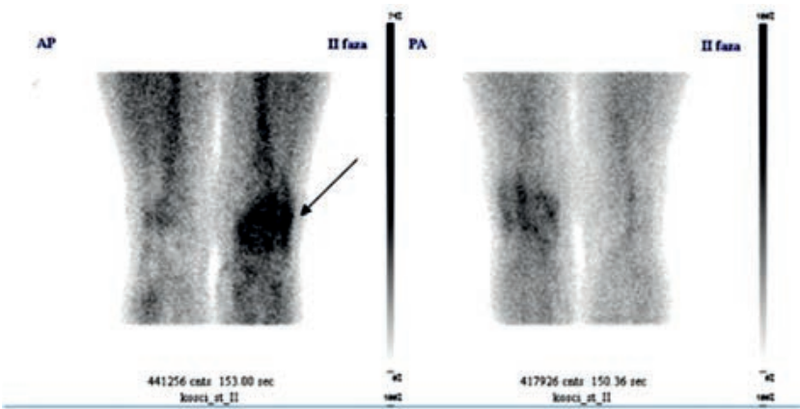
Na przedstawionym scyntygramie ukazano duży obszar
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Na schemacie oznaczono