Pytanie 1
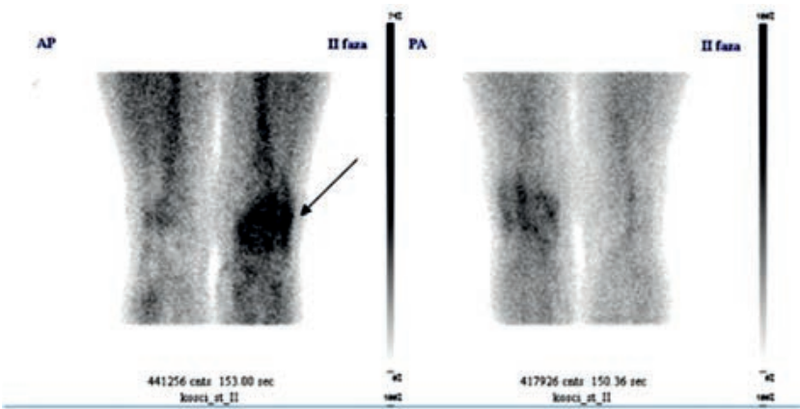
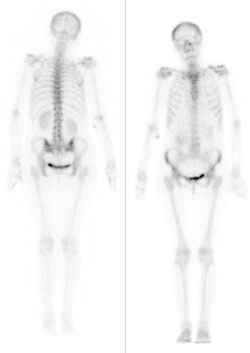
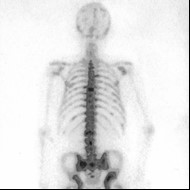
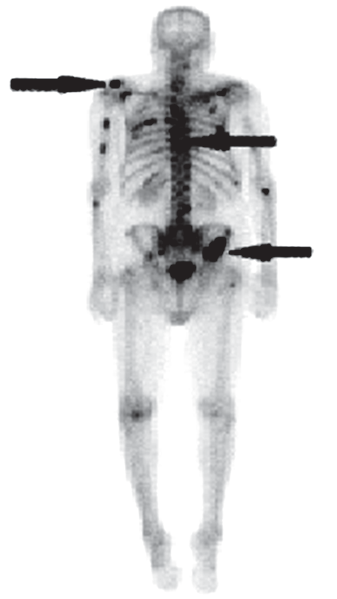
Na scyntygramie kości strzałkami oznaczono ogniska
Brak odpowiedzi na to pytanie.
Na przedstawionym obrazie widzisz klasyczne scyntygram kości całego ciała po podaniu radiofarmaceutyku znakowanego technetem-99m (najczęściej MDP lub HDP). Ogniska zaznaczone strzałkami to tzw. „hot spots” – miejsca wzmożonego gromadzenia znacznika. W praktyce klinicznej, przy takim rozsianym, wieloogniskowym, asymetrycznym wychwycie w kościach osiowych i w nasadach kości długich, najbardziej typowy obraz dotyczy właśnie przerzutów nowotworowych do kości. Moim zdaniem to jest wręcz podręcznikowy przykład rozsianej choroby przerzutowej, np. w raku prostaty czy raku piersi. Radiofarmaceutyk kumuluje się w miejscach zwiększonego obrotu kostnego i aktywności osteoblastów. Przerzut osteoblastyczny powoduje intensywną przebudowę kostną, dlatego na scyntygrafii widzimy liczne, nieregularne, mocno świecące ogniska. Standardy medycyny nuklearnej (EANM, SNMMI) podkreślają, że w ocenie scyntygrafii kości kluczowy jest rozkład zmian: mnogie, rozsiane, różnej wielkości ogniska, szczególnie w kręgosłupie, żebrach, miednicy i bliższych częściach kości udowych, są wysoce podejrzane o przerzuty. W praktyce technik i lekarz zawsze korelują obraz scyntygrafii z wywiadem onkologicznym pacjenta, poziomem PSA, markerami nowotworowymi, a także z badaniami RTG, TK lub MR, żeby potwierdzić charakter zmian. Scyntygrafia jest bardzo czuła, ale mniej swoista, dlatego interpretacja wymaga doświadczenia i znajomości typowych pułapek, takich jak złamania, zwyrodnienia czy ogniska zapalne. W badaniach kontrolnych po leczeniu onkologicznym ten typ obrazu pozwala ocenić progresję lub regresję zmian przerzutowych, co ma duże znaczenie dla dalszego planowania terapii.