Pytanie 1
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
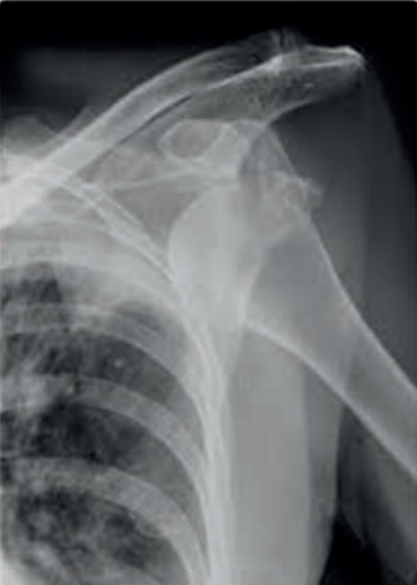
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Jakie źródła promieniowania stosowane są w brachyterapii?
Gdzie znajduje się węzeł zatokowo-przedsionkowy wywołujący rytmiczne skurcze mięśnia serca?
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
W medycynie nuklearnej wykorzystuje się:
Który załamek w zapisie EKG odpowiada zjawisku depolaryzacji przedsionków mięśnia sercowego?
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
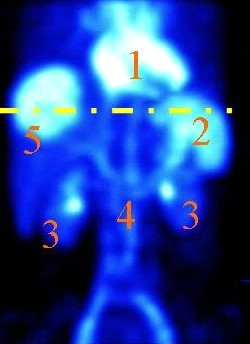
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
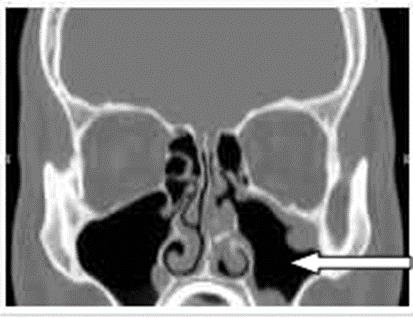
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
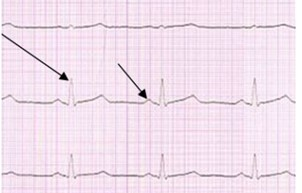
Na elektrokardiogramie strzałki wskazują załamki
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
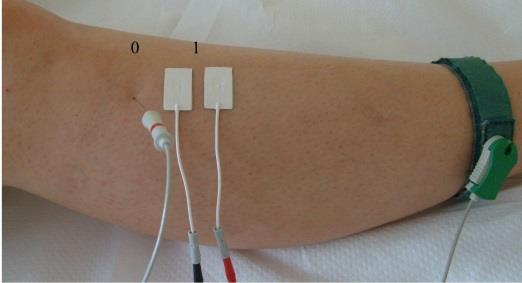
Na ilustracji przedstawiono przygotowanie pacjenta do badania
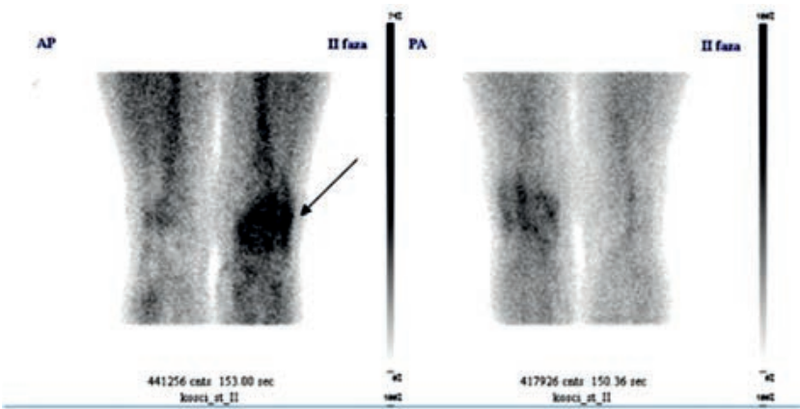
Na przedstawionym scyntygramie ukazano duży obszar
W radioterapii konwencjonalnej pacjent jest leczony promieniowaniem pochodzącym
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Objawem późnego odczynu popromiennego po teleradioterapii jest
Który radioizotop stosuje się do badania scyntygraficznego kości?
Jak przebiega promień centralny w projekcji AP czaszki?
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Fistulografia to badanie kontrastowe
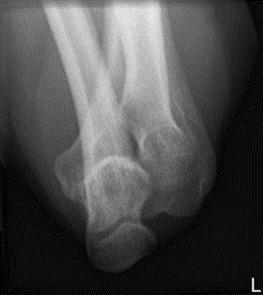
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
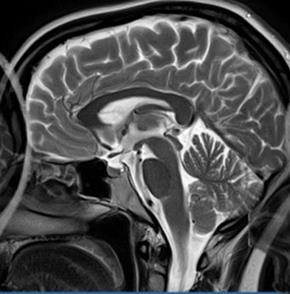
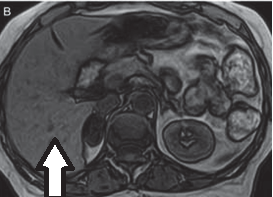
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
W badaniu PET stosuje się tylko radioizotopy emitujące
W badaniu EKG elektrodę przedsercową V4 należy umocować
W ultrasonografii występuje zależność:
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
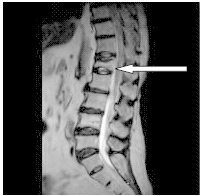
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg