Pytanie 1
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
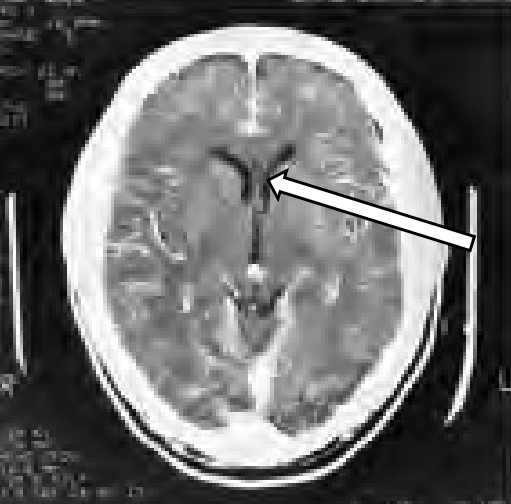
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Cholangiografia to badanie radiologiczne
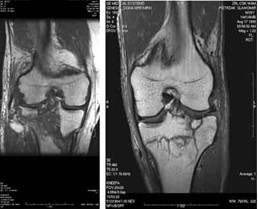
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
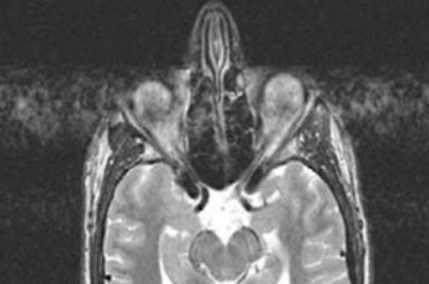
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
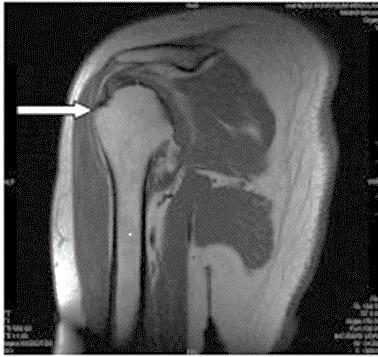
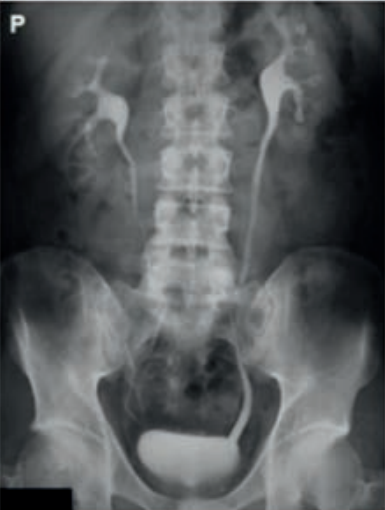
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
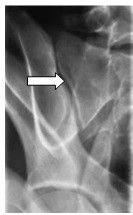
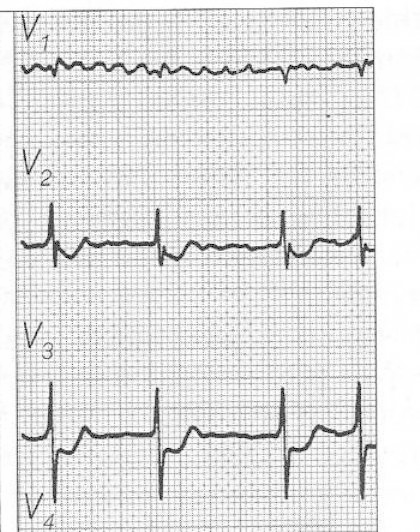
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
Celiakografia jest badaniem kontrastowym
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W radiologii stomatologicznej ząb o numerze 23 to kieł
Rumień skóry pojawiający się podczas radioterapii jest objawem
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
W leczeniu izotopowym tarczycy należy podać
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
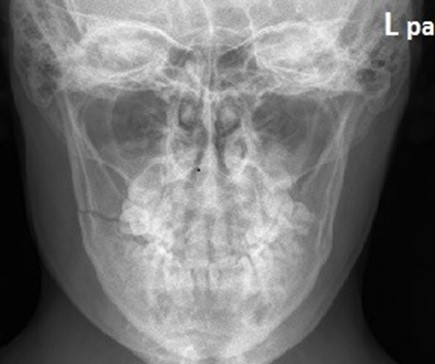
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

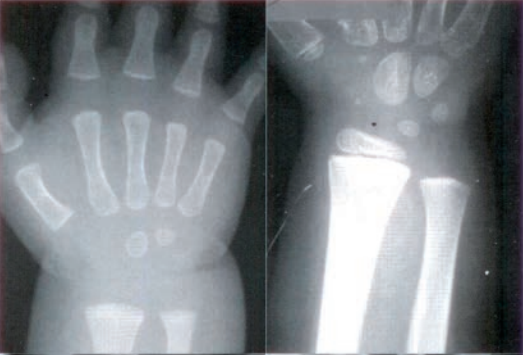
Zestaw rentgenogramów przedstawia
Objawem późnego odczynu popromiennego po teleradioterapii jest
Co jest przyczyną artefaktu widocznego na obrazie MR?
W zapisie EKG załamki P dodatnie w odprowadzeniu I i II, a ujemne w aVR oraz częstotliwość rytmu mniejsza niż 60/min wskazują na
Szczytowy przepływ wydechowy zarejestrowany w trakcie badania maksymalnie natężonego wydechu jest oznaczany skrótem
Na rentgenogramie uwidoczniono badanie
Zarejestrowane na elektrokardiogramie miarowe fale f w kształcie „zębów piły” poprzedzielane prawidłowymi zespołami QRS są charakterystyczne dla
Przyczyną zaniku kostnego jest
Zamieszczony elektrokardiogram przedstawia
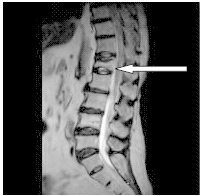
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg