Pytanie 1
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
W leczeniu izotopowym tarczycy należy podać
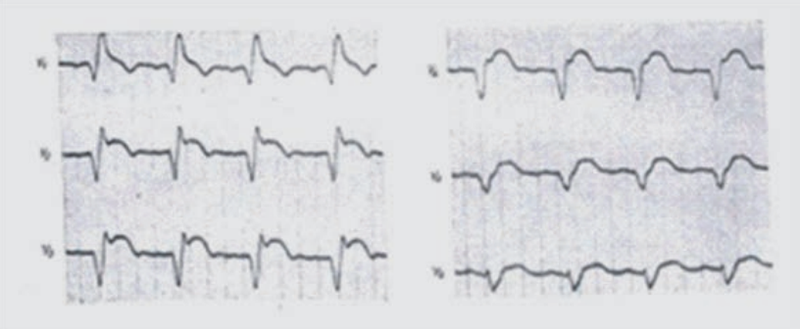
Na elektrokardiogramie zarejestrowano
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Fala głosowa rozchodzi się
Wskazaniem do wykonania badania spirometrycznego jest
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Zgodnie z obowiązującą procedurą radiologiczną zdjęcie jamy brzusznej przy podejrzeniu zapalenia nerek zostanie wykonane w projekcji
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
Zamieszczone obrazy związane są z badaniem
Które badanie, zgodnie z zakresem kompetencji, może samodzielnie wykonać technik elektroradiolog?
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
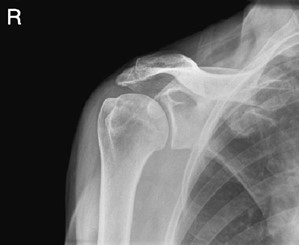
Na radiogramie uwidoczniono
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
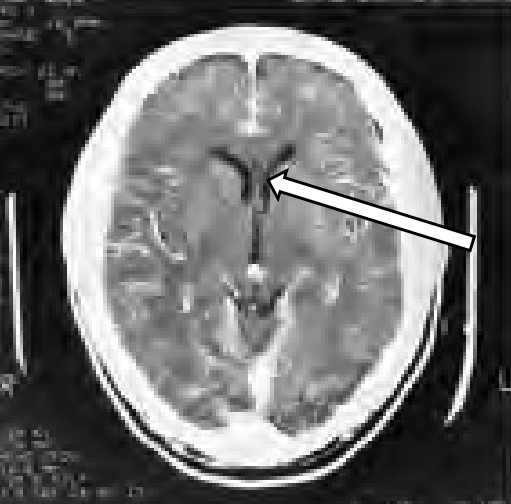
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
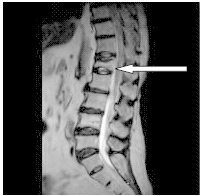
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
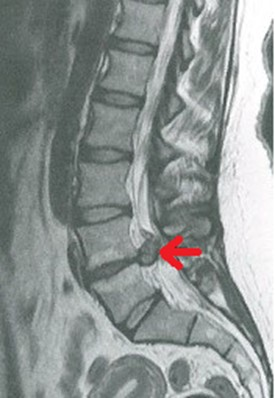
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
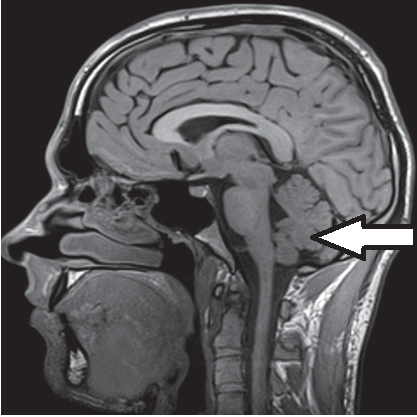
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
Chorobą układu oddechowego typu obturacyjnego jest
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
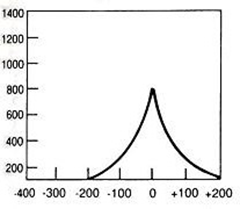
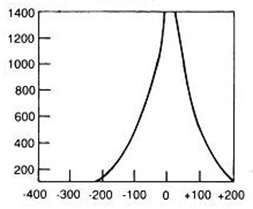
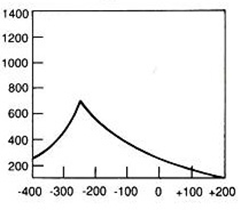
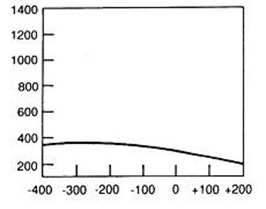
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
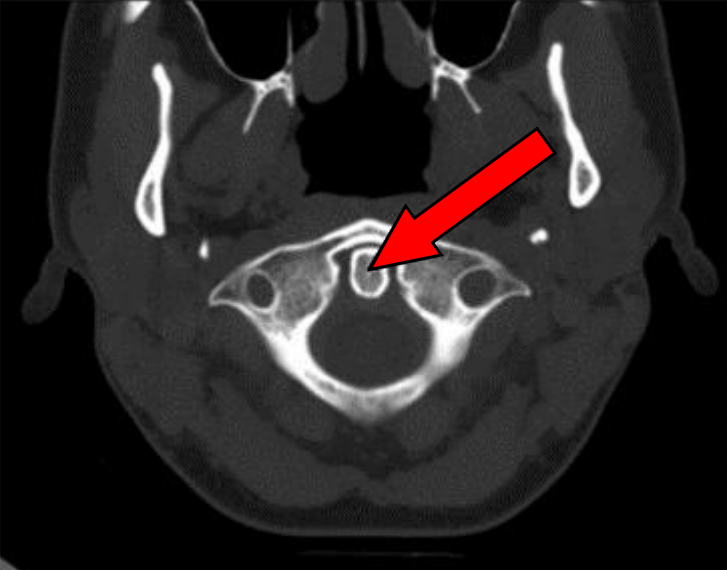
Na przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
W audiometrii badanie polegające na maskowaniu (zagłuszaniu) tonów szumem białym to próba
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
Pielografia zstępująca umożliwia diagnostykę
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Przy podejrzeniu ciała obcego w oczodole należy wykonać
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
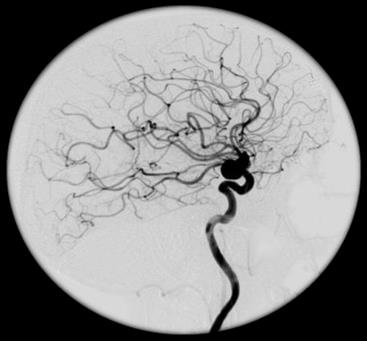
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
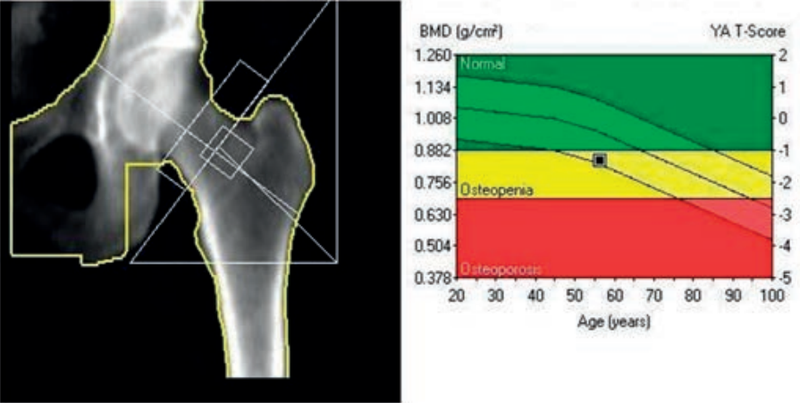
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi