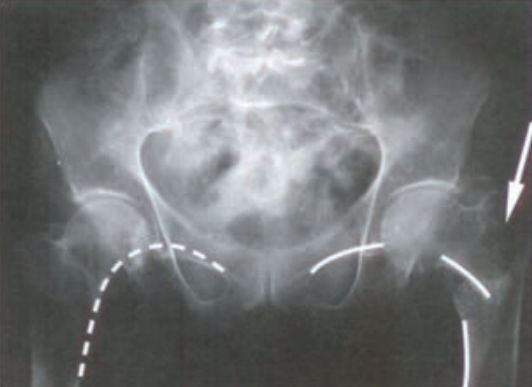
Pytanie 1
W leczeniu izotopowym tarczycy należy podać
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
W leczeniu izotopowym tarczycy należy podać
Który radioizotop jest emiterem promieniowania alfa?
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Wskazaniem do wykonania przesiewowego badania densytometrycznego jest
Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Audiometria impedancyjna polega na pomiarze
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
SPECT to
Obraz stawu kolanowego otrzymano metodą
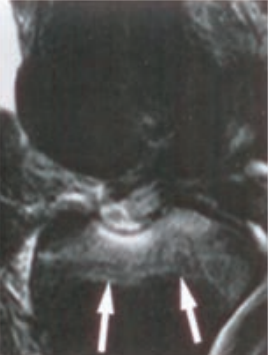
W badaniu cystografii wstępującej środek kontrastowy należy podać
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
Przy podejrzeniu ciała obcego w oczodole należy wykonać
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
W badaniu audiometrycznym do oceny przewodnictwa kostnego wybranego ucha słuchawkę kostną należy przyłożyć do
Który artefakt uwidoczniono na skanie RM głowy?
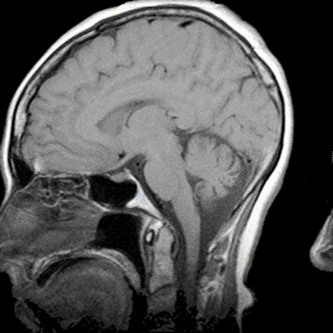
Czym charakteryzuje się późny odczyn popromienny?
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
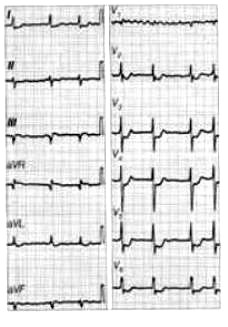
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
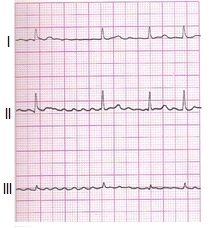
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Na elektrokardiogramie uwidoczniono
Pielografia to badanie układu
Chorobą układu oddechowego typu obturacyjnego jest
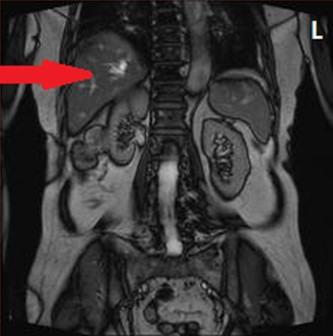
Na obrazie MR jamy brzusznej strzałką wskazano
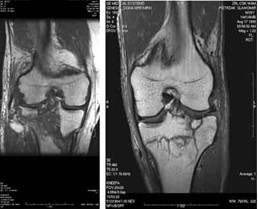
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
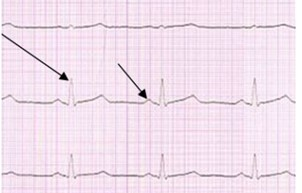
Na elektrokardiogramie strzałki wskazują załamki
Radiogram przedstawia