Pytanie 1
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
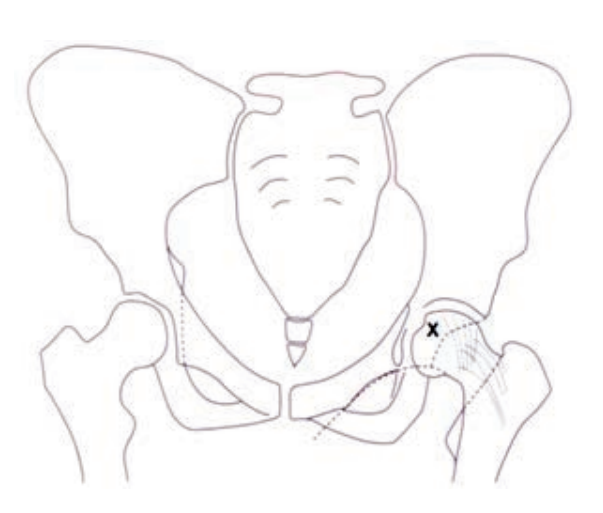
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
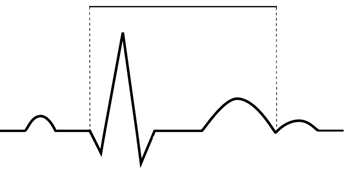
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
Zamieszczony obraz został wykonany metodą
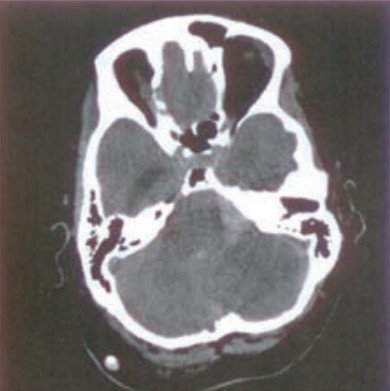
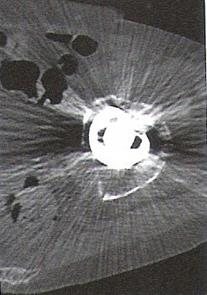
Zarejestrowany na obrazie TK artefakt jest spowodowany
W leczeniu izotopowym tarczycy należy podać
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
W radioterapii hadronowej leczenie odbywa się przy użyciu
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
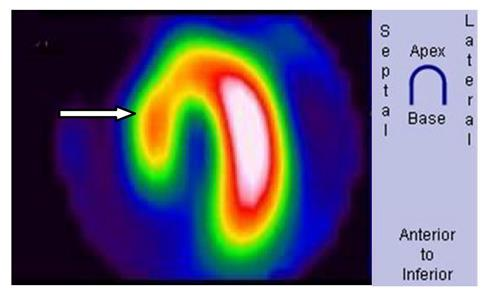
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
Diagnozowanie metodą PET oparte jest na zjawisku
Na wykresie EKG zaznaczono
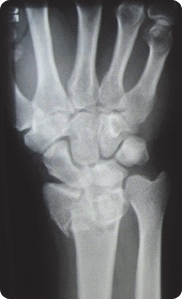
Na radiogramie uwidoczniono złamanie nasady
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
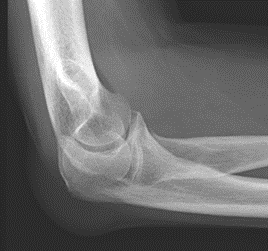
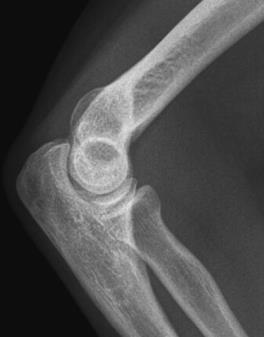
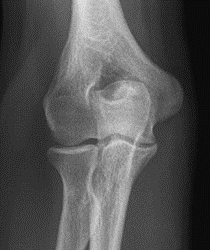
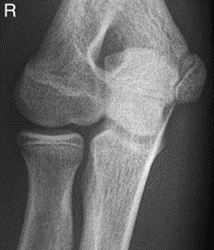
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Pielografia zstępująca umożliwia diagnostykę
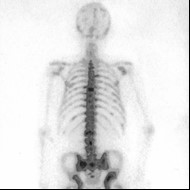
Przedstawiony obraz został zarejestrowany podczas wykonywania
Jakie wymagania techniczne muszą spełniać aparaty terapeutyczne stosowane w zakładach brachyterapii, służące bezpośrednio do napromieniania pacjenta metodą zdalnego wprowadzania źródeł promieniotwórczych?
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
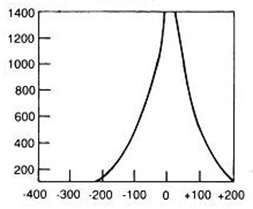
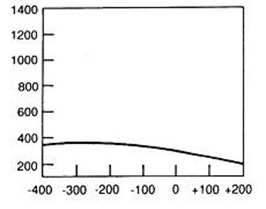
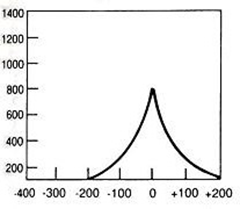
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
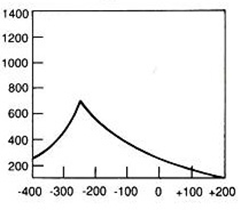
Na ilustracji przedstawiono zjawisko
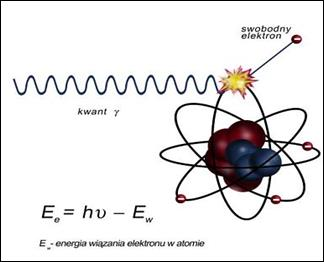
Co zostało uwidocznione na zamieszczonym radiogramie?
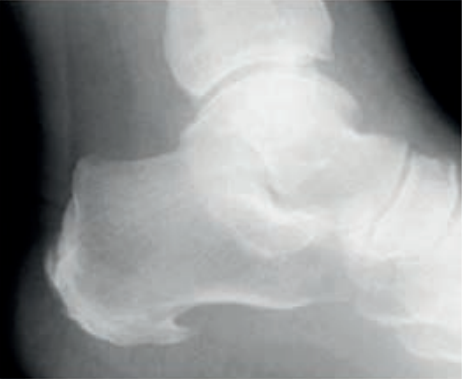
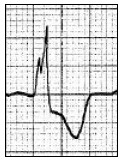
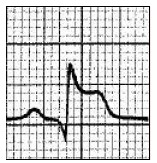
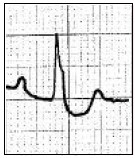
Który zapis EKG przedstawia falę Pardee'go?

Wskazaniem do wykonania badania spirometrycznego jest
W jakich jednostkach mierzy się natężenie dźwięku?
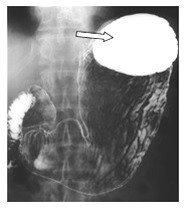
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
SPECT to