Pytanie 1
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wynik: 36/40 punktów (90,0%)
Wymagane minimum: 20 punktów (50%)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
W celu sprawdzenia stężenia kwasu siarkowego(VI) odważono 1 g badanego kwasu i przeprowadzono analizę miareczkową, w której zużyto 20,4 \( \text{cm}^3 \) roztworu NaOH.
Stężenie procentowe badanego kwasu, obliczone na podstawie wzoru wynosi
$$ C_p = \frac{0,02452 \cdot V_{NaOH}}{mp} \cdot 100\% $$gdzie:
\( C_p \) – stężenie procentowe badanego kwasu; \( \% \)
\( 0,02452 \) – współczynnik przeliczeniowy; \( \text{g/cm}^3 \)
\( V_{NaOH} \) – objętość roztworu NaOH, zużyta w miareczkowaniu; \( \text{cm}^3 \)
\( mp \) – odważka badanego kwasu; g
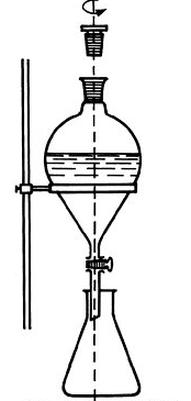
Na rysunku przedstawiono proces
Który symbol literowy umieszczany na naczyniach miarowych wskazuje na kalibrację do "wlewu"?
W wyniku reakcji 100 g azotanu(V) ołowiu(II) z jodkiem potasu otrzymano 120 g jodku ołowiu(II). Wydajność reakcji wyniosła
| Pb(NO3)2 + 2KI → PbI2 + 2KNO3 | |
| (MPb(NO3)2 = 331 g/mol, MKI = 166 g/mol, MPbI2 = 461 g/mol, MKNO3 = 101 g/mol) |
Jakie jest znaczenie skrótu: cz. na etykiecie reagentu chemicznego?
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
W trakcie korzystania z odczynnika opisanego na etykiecie, należy szczególnie zwrócić uwagę na zagrożenia związane
Jakie jest stężenie molowe roztworu, jeśli w 100 cm3 roztworu znajduje się 5,6 g KOH?
MK = 39 g/mol, MO = 16 g/mol, MH = 1 g/mol
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Rysunek przedstawia

W celu wydania świadectwa kontroli jakości odczynnika chemicznego - jodku potasu cz.d.a. przeprowadzono jego analizę. Wymagania oraz wyniki badań zapisano w tabeli:
Z analizy danych zawartych w tabeli wynika, że jodek potasu cz.d.a.
| Wymagania | Wynik badania | |
|---|---|---|
| Zawartość KI | min. 99,5% | 99,65% |
| Wilgoć | max. 0,1% | 0,075% |
| Substancje nierozpuszczalne w wodzie | max. 0,005% | 0,002% |
| pH (5%, H2O) | 6 ÷ 8 | 6,8 |
| Azot ogólny (N) | max. 0,001% | 0,0007% |
| Chlorki i bromki (j. Cl) | max. 0,01% | 0,004% |
| Fosforany (PO4) | max. 0,001% | 0,0006% |
| Jodany (IO3) | max. 0,0003% | 0,0001% |
| Siarczany (SO4) | max. 0,001% | 0,0004% |
| Metale ciężkie (j. Pb) | max. 0,0005% | 0,00025% |
| Arsen (As) | max. 0,00001% | 0,000006% |
| Magnez (Mg) | max. 0,001% | 0,0004% |
| Sód (Na) | max. 0,05% | 0,015% |
| Wapń (Ca) | max. 0,001% | 0,0006% |
| Żelazo (Fe) | max. 0,0003% | 0,0003% |
Naczynia z roztworem kwasu siarkowego(VI) o dużym stężeniu nie powinny być pozostawiane otwarte nie tylko za względów bezpieczeństwa, ale także dlatego, że kwas
Ogólna próbka, jednostkowa lub pierwotna powinna
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby przygotować 250 cm3 roztworu wodorotlenku potasu o stężeniu 0,25 mola, potrzebne będzie
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

Roztwory o ściśle określonym stężeniu, używane w analizach miareczkowych, nazywamy
W wyniku reakcji 20 g tlenku magnezu z wodą uzyskano 20 g wodorotlenku magnezu. Oblicz efektywność reakcji.
MMg = 24 g/mol, MO = 16 g/mol, MH = 1 g/mol?
Instalacja, do której należy podłączyć palnik, powinna być pokryta farbą w kolorze
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Z kolby miarowej o pojemności 1 dm3, zawierającej roztwór HCl o stężeniu 0,1 mol/dm3, pobrano pipetą 2,5 cm3, a następnie przeniesiono do kolby miarowej o pojemności 20 cm3 i rozcieńczono wodą "do kreski" miarowej. Jakie stężenie ma otrzymany roztwór?
Etykieta roztworu kwasu azotowego(V) o koncentracji 6 mol/dm3 powinna zawierać nazwę substancji oraz
Po przeprowadzeniu krystalizacji z 120 g kwasu szczawiowego uzyskano 105 g produktu o wysokiej czystości. Jaki był poziom zanieczyszczeń w kwasie szczawiowym?
Próbka laboratoryjna posiadająca cechy higroskopijne powinna być pakowana
Podczas krystalizacji 210 g technicznego bezwodnego siarczanu(VI) cynku uzyskano 250 g ZnSO4 x 7H2O. Jaka była wydajność procesu krystalizacji?
Ropa naftowa stanowi mieszankę węglowodorów. Jaką metodę wykorzystuje się do jej rozdzielania na składniki?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Rozpuszczalnik stosowany w procesie krystalizacji powinien
Jaką substancję należy koniecznie oddać do utylizacji?
Zbiór próbek pierwotnych tworzy próbkę
Aby przygotować 500 g roztworu o stężeniu 10% (m/m), ile substancji należy odważyć?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Poniżej jest równanie reakcji prażenia węglanu wapnia. 200 g węglanu wapnia zawierającego 10% zanieczyszczeń poddano prażeniu. Masa otrzymanego tlenku wapnia wyniosła
| CaCO3 → CaO + CO2 |
| (MCaCO3 = 100 g/mol, MCaO = 56 g/mol, MCO2 = 44 g/mol) |
Jakie jest przeznaczenie pieca muflowego?
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?
Aby uzyskać sole sodowe fenoli, należy stopić dany fenol z sodą (M = 106 g/mol), stosując 10% nadmiar w porównaniu do ilości stechiometrycznej, według równania:
2 ArOH + Na2CO3 → 2 ArONa + H2O + CO2 Ile sody jest wymagane do reakcji z 7,2 g 2-naftolu (M = 144 g/mol)?
Między wodorotlenkiem baru a chlorkiem amonu dochodzi do spontanicznej reakcji, która powoduje silne schłodzenie mieszaniny oraz wydobycie się charakterystycznego zapachu amoniaku.
Ba(OH)2(s) + 2 NH4Cl(s) → BaCl2(aq) + 2 H2O(c) + 2 NH3(g) Wskaź, które sformułowanie właściwie wyjaśnia to zjawisko.
nieodwracalnie jej równowagę.