Pytanie 1
SPECT to
Wynik: 15/40 punktów (37,5%)
Wymagane minimum: 20 punktów (50%)
SPECT to
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
Rytm alfa i beta rejestruje się podczas badania
Celem radioterapii paliatywnej nie jest
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
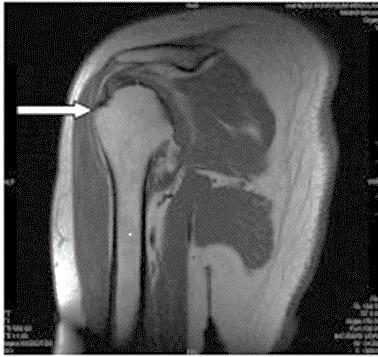
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
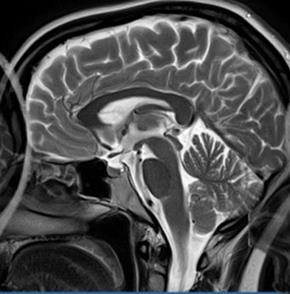
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
W badaniu EKG elektrodę przedsercową V4 należy umocować
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
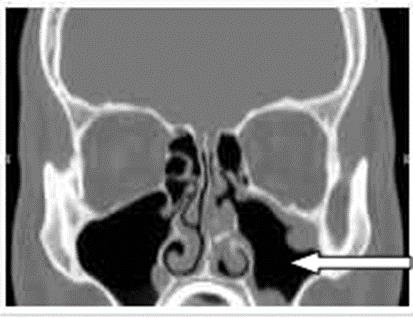
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
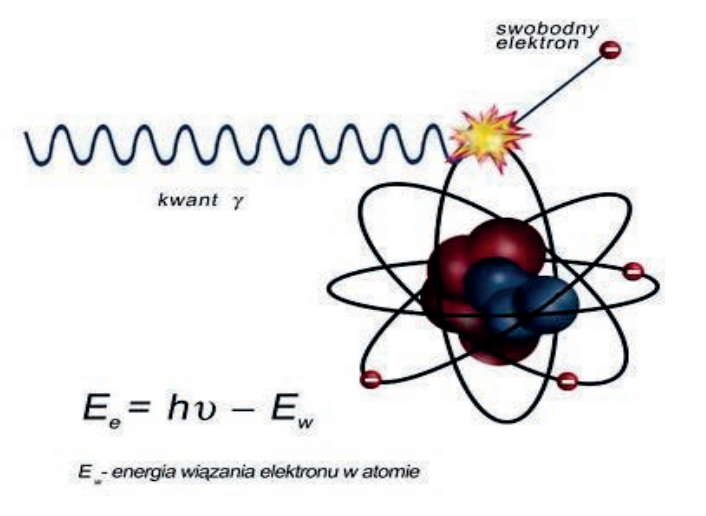
Promieniowanie rentgenowskie powstaje w wyniku hamowania
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
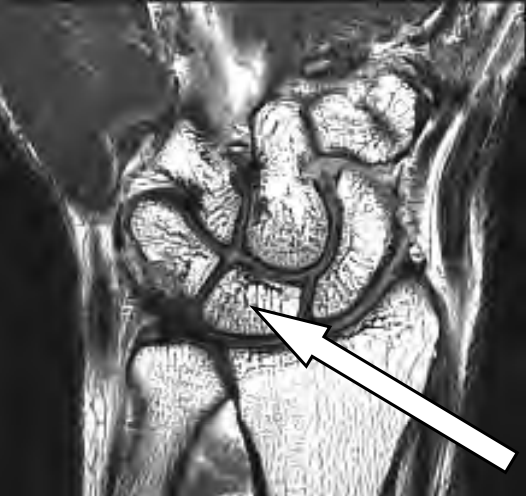
W badaniu EKG elektrodę przedsercową V4 należy umocować
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
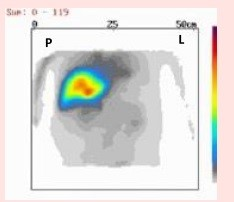
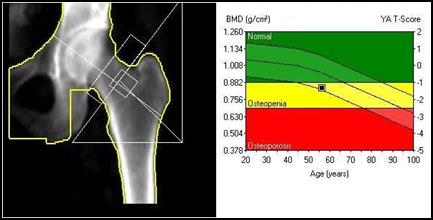
Zamieszczone na ilustracji obrazy dotyczą badania
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Ultrasonograficzne środki kontrastowe to
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
Na zamieszczonej rycinie przedstawiono
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
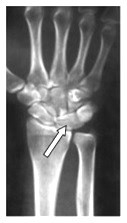
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Który załamek odzwierciedla repolaryzację komór w zapisie EKG?
Urografia polega na
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
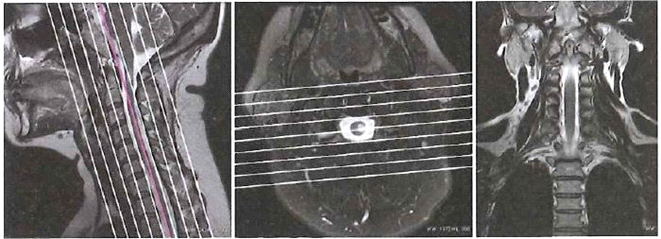
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?