Pytanie 1
Korzystając z wykresu określ, w jakiej temperaturze należy rozpuszczać azotan(V) potasu, aby całkowicie rozpuścić 110 g soli w 100 g wody.
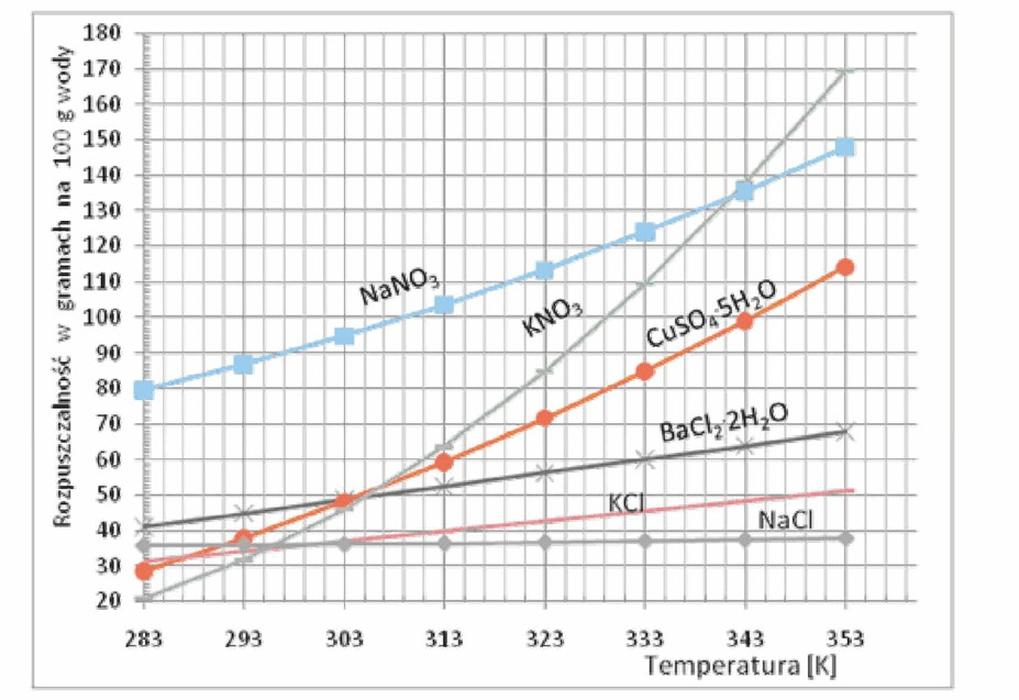
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Korzystając z wykresu określ, w jakiej temperaturze należy rozpuszczać azotan(V) potasu, aby całkowicie rozpuścić 110 g soli w 100 g wody.

Aby przygotować 250 cm3 0,2-molowego roztworu wodorotlenku sodu, należy odważyć
| MNaOH = 40g / mol |
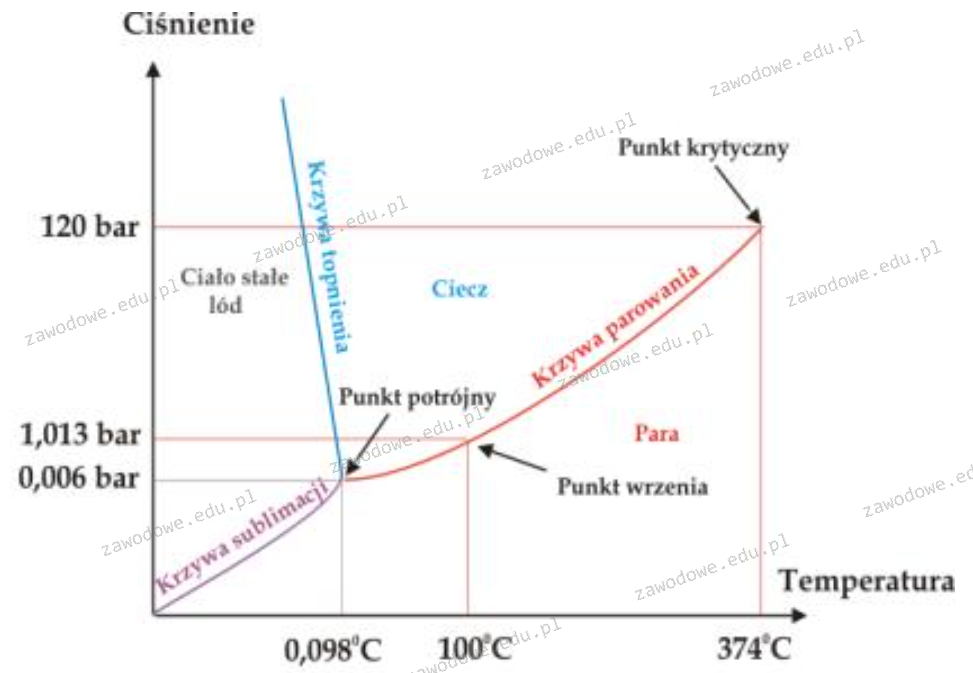
Korzystając z wykresu wskaż, w jakiej postaci występuje woda w temperaturze 10°C i pod ciśnieniem 100 barów.
Laboratoryjna apteczka powinna zawierać m.in.
Na rysunku przedstawiono pipetę

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Odważka analityczna wodorotlenku sodu, przygotowana fabrycznie, zawiera 0,1 mola NaOH. Jaką objętość wody destylowanej należy dodać w kolbie miarowej, aby uzyskać roztwór wodorotlenku sodu o stężeniu 0,0500 mol/dm3?
Proces mineralizacji próbki, który polega na jej spopieleniu w piecu muflowym w temperaturze 300-500°C i rozpuszczeniu pozostałych resztek w kwasach w celu oznaczenia zawartości metali ciężkich, to mineralizacja
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Średnia masa wody wypływająca z pipety o deklarowanej pojemności 25 cm3, w temperaturze 25°C wynosi 24,80 g. Korzystając z danych zamieszczonych w tabeli wskaż wartość poprawki kalibracyjnej dla tej pipety.
| Masa wody zajmującej objętość 1 dm3 w zależności od temperatury pomiaru | |
|---|---|
| Temperatura °C | Masa wody g |
| 20 | 997,17 |
| 21 | 997,00 |
| 22 | 996,80 |
| 23 | 996,59 |
| 24 | 996,38 |
| 25 | 996,16 |
| 26 | 995,93 |
| 27 | 995,69 |
| 28 | 995,45 |
| 29 | 995,18 |
| 30 | 994,92 |
Jaką substancję należy koniecznie oddać do utylizacji?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby przygotować 250 cm3 roztworu wodorotlenku potasu o stężeniu 0,25 mola, potrzebne będzie
Zabieg, który wykonuje się podczas pobierania próbki wody do analizy, mający na celu zachowanie jej składu chemicznego w trakcie transportu, określa się mianem
W celu przygotowania 100 cm3 roztworu mianowanego, jaką kolbę należy zastosować?
W trakcie korzystania z odczynnika opisanego na etykiecie, należy szczególnie zwrócić uwagę na zagrożenia związane
Jaką metodę poboru próbek przedstawiono na rysunku?

Aby podnieść stężenie mikroelementów w roztworze, próbkę należy poddać
Jakim kolorem zazwyczaj oznacza się przewody w instalacji gazowej w laboratorium?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Który z procesów jest endotermiczny?
Piktogramem przedstawionym na rysunku znakuje się opakowanie substancji

Do rozpuszczania próbek wykorzystuje się wodę królewską, która stanowi mieszaninę stężonych kwasów
Intensywna reakcja z FeCl3 jest wykorzystywana do identyfikacji
Zestaw przedstawiony na rysunku może służyć do
Połączono równe ilości cynku i bromu, a następnie poddano je reakcji Zn + Br2 → ZnBr2. W tych warunkach stopień reakcji cynku wynosi (masy atomowe: Zn – 65u, Br – 80u)?
Na podstawie zamieszczonych informacji, wskaż ilości odczynników, które są niezbędne do przygotowania skali wzorców do kolorymetrycznego oznaczania rozpuszczalnych fosforanów(V).
| Przygotowanie skali wzorców do kolometrycznego oznaczania fosforanów(V) | ||||||||
| Do ośmiu cylindrów Nesslera o pojemności 100 cm3 odmierzyć kolejno wzorcowy roztwór roboczy KH2PO4 według poniższej tabeli SKALA WZORCÓW (PO43-) i uzupełnić wodą do kreski. Do każdego cylindra dodać 2 cm3 roztworu molibdenianu amonu (heksaamonoheptamolibdenian(VI)), wymieszać, dodać 0,2 cm3 roztworu SnCl2 i ponownie wymieszać. | ||||||||
| SKALA WZORCÓW (PO43-) | ||||||||
| Wzorcowy roztwór roboczy [cm3] | 0,0 | 0,5 | 1,0 | 2,0 | 3,0 | 5,0 | 7,0 | 10,0 |
| Zawartość PO43- [mg] | 0,0 | 0,005 | 0,01 | 0,02 | 0,03 | 0,05 | 0,07 | 0,10 |
| Roztwór | KH₂PO₄ | (NH₄)₆Mo₇O₂₄ | SnCl₂ |
|---|---|---|---|
| A. | 28,5 cm³ | 8,0 cm³ | 0,16 cm³ |
| B. | 0,285 cm³ | 16,0 cm³ | 1,6 cm³ |
| C. | 28,5 cm³ | 16,0 cm³ | 1,6 cm³ |
| D. | 0,285 cm³ | 8,0 cm³ | 16 cm³ |
Temperatura wrzenia aniliny przy normalnym ciśnieniu wynosi 457,13 K. W trakcie jej oczyszczania metodą destylacji prostej pod ciśnieniem atmosferycznym należy zebrać frakcję wrzącą w przedziale temperatur
Reagenty o czystości na poziomie 99,999% — 99,9999% to reagenty
Jaka minimalna pojemność powinna mieć miarka, aby jednorazowo zmierzyć 60,0 cm3 wody?
Którą substancję można bezpośrednio wyrzucić do odpadów komunalnych?
Z etykiety wynika, że dany związek mógł być

Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

Transportuje się pobrane próbki wody do analiz fizykochemicznych
Ropa naftowa stanowi mieszankę węglowodorów. Jaką metodę wykorzystuje się do jej rozdzielania na składniki?
Jakie jest przeznaczenie pieca muflowego?
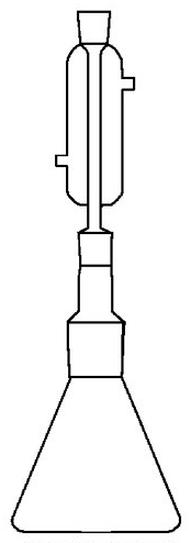
Aparat przedstawiony na ilustracji służy do

Na podstawie danych w tabeli określ, jaką masę próbki należy pobrać, jeżeli wielkość ziarna wynosi 1·10-5 m.
| Wielkość ziaren lub kawałków [mm] | Poniżej 1 | 1-10 | 11-50 | Ponad 50 |
|---|---|---|---|---|
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?