Pytanie 1
Fistulografia to badanie kontrastowe
Wynik: 33/40 punktów (82,5%)
Wymagane minimum: 20 punktów (50%)
Fistulografia to badanie kontrastowe
Na radiogramie uwidoczniono
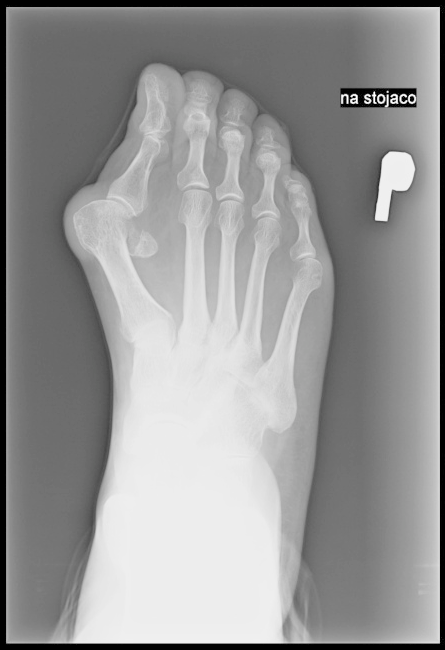
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Rumień skóry pojawiający się podczas radioterapii jest objawem
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Na schemacie oznaczono
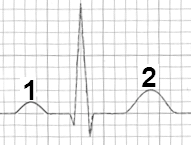
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
Który załamek odzwierciedla repolaryzację komór w zapisie EKG?
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
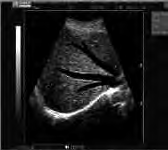
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
Który elektrokardiogram jest poprawny technicznie?
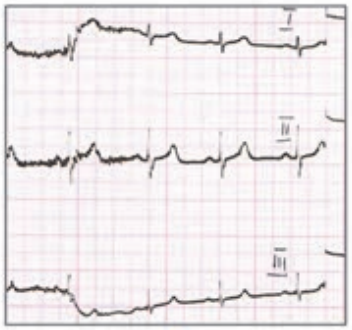
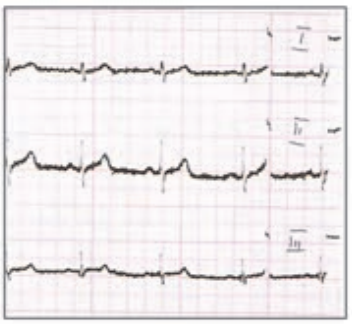
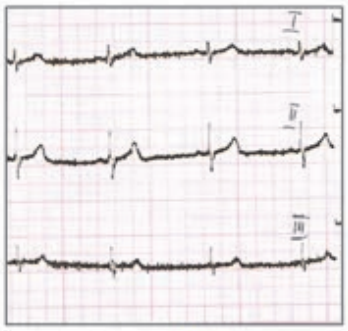
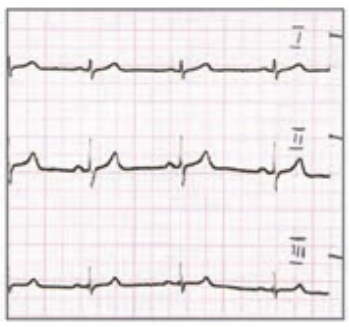
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
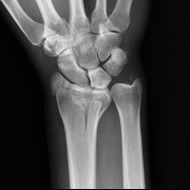
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
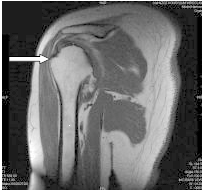
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
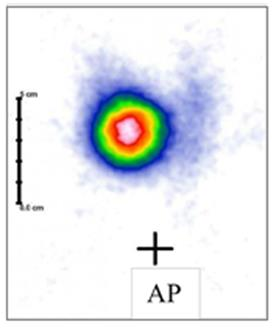
„Ognisko zimne” w obrazie scyntygraficznym oznacza
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Którą kość oznaczono na obrazie rezonansu magnetycznego?
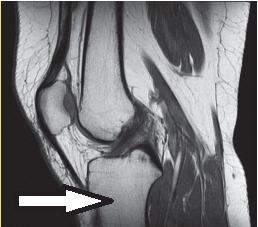
Rytm alfa i beta rejestruje się podczas badania
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
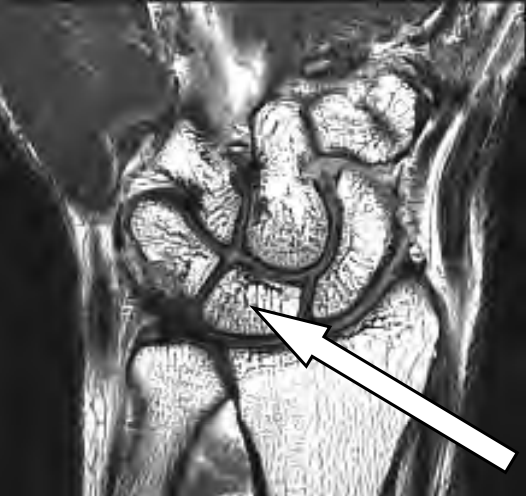
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
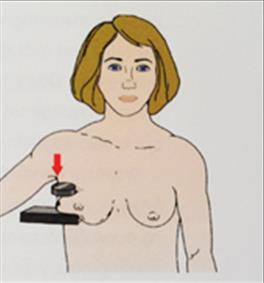
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Na scyntygramie tarczycy uwidoczniono guzek
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
Do wykonania stomatologicznego zdjęcia rentgenowskiego techniką kąta prostego promień centralny należy ustawić prostopadle do
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Na obrazie uwidoczniono
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
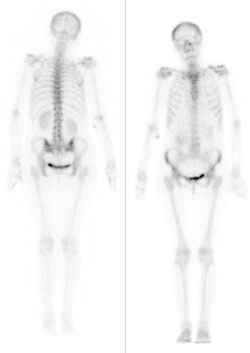
Podczas badania gammakamerą źródłem promieniowania jest