Pytanie 1
Który radioizotop jest emiterem promieniowania alfa?
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Który radioizotop jest emiterem promieniowania alfa?
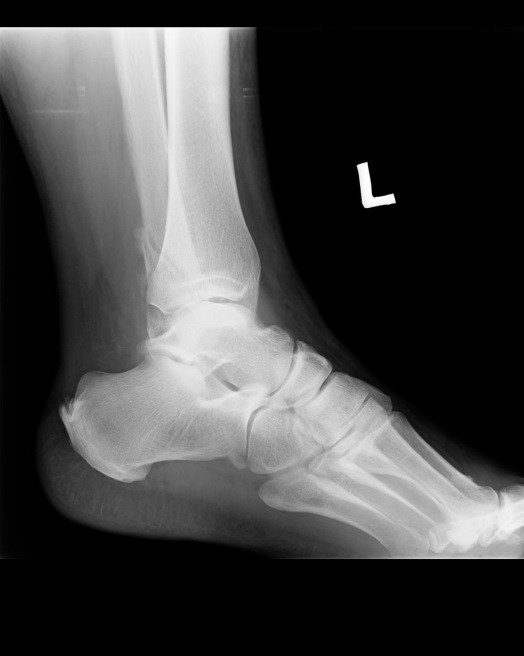
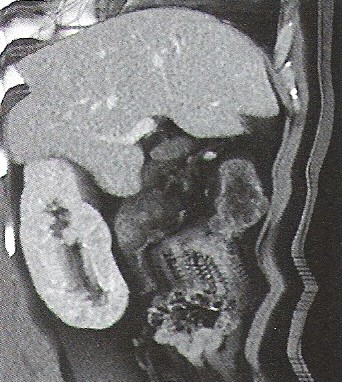
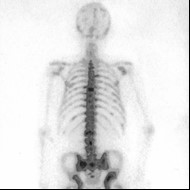
Na radiogramie uwidoczniono
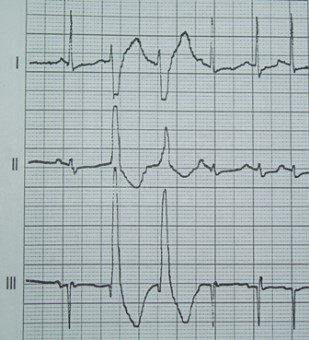
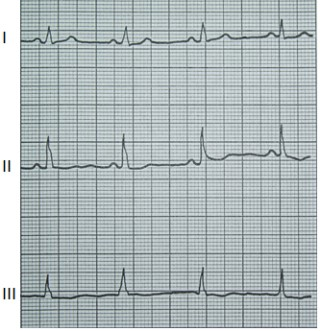
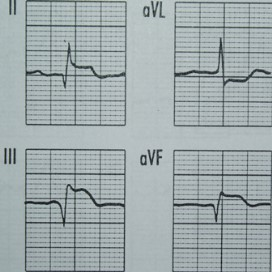
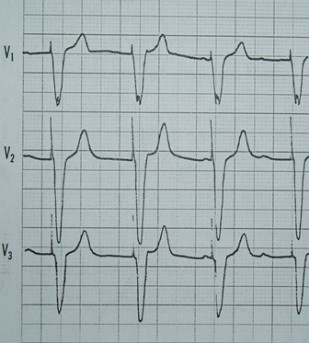
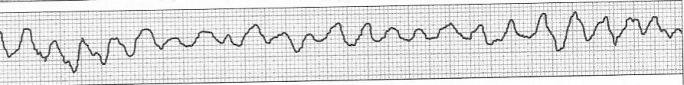
Na którym z zapisów EKG została uwidoczniona fala Pardee'go?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
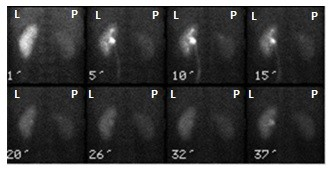
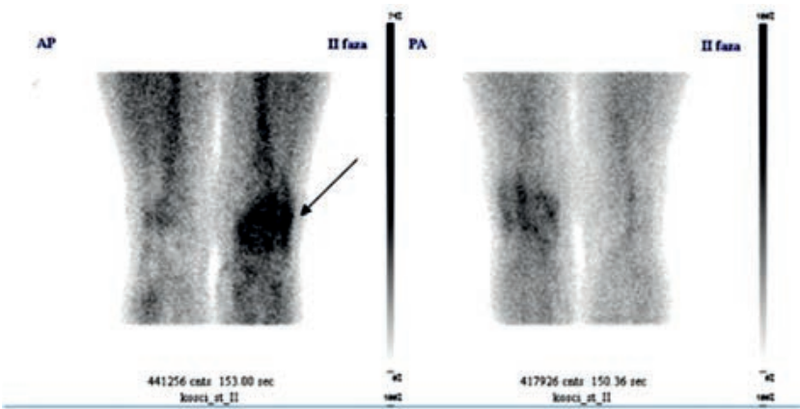
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
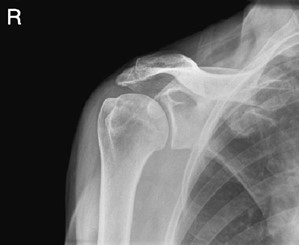
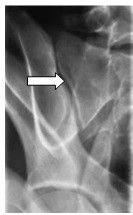
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
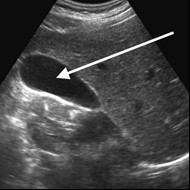
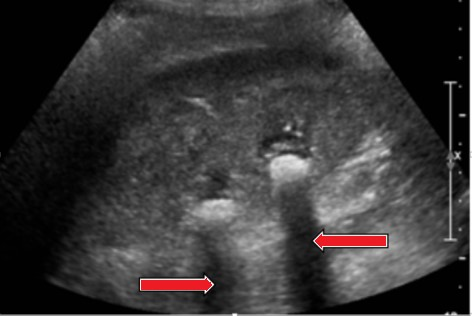
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Badanie gęstości mineralnej kości metodą DXA należy wykonać
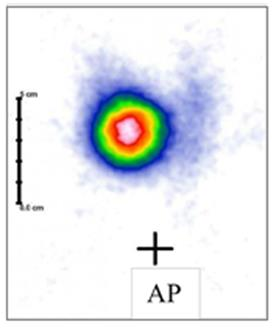
Na scyntygramie tarczycy uwidoczniono guzek
Badanie przewodu pokarmowego metodą podwójnego kontrastu wiąże się z podaniem pacjentowi
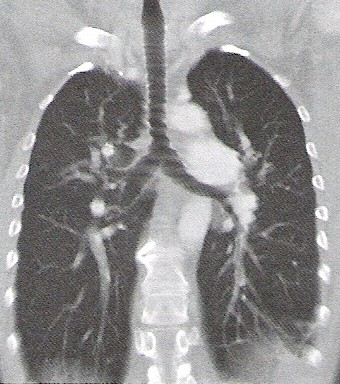
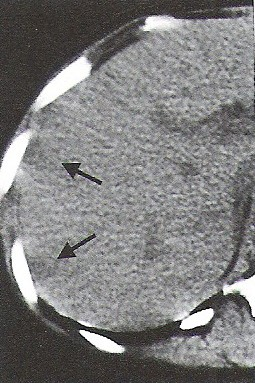
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Który artefakt wskazano strzałkami na obrazie USG nerki?
Na przedstawionym scyntygramie ukazano duży obszar
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie
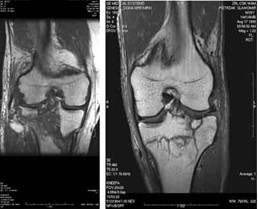
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
Technikę bramkowania oddechowego stosuje się w badaniu MR
W badaniu PET stosuje się tylko radioizotopy emitujące
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
Zamieszczony elektrokardiogram przedstawia
Czas połowicznego zaniku jest wykorzystywany
Do wykonania stomatologicznego zdjęcia rentgenowskiego techniką kąta prostego promień centralny należy ustawić prostopadle do
Przedstawiony obraz został zarejestrowany podczas wykonywania
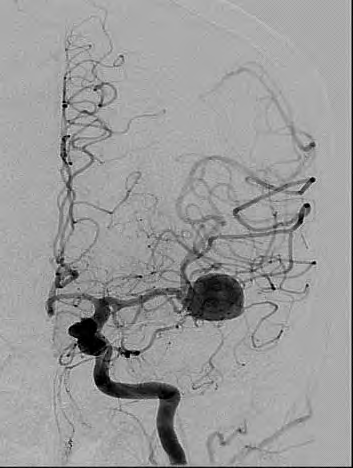
Którą patologię uwidoczniono w badaniu angiograficznym?
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Przyczyną zaniku kostnego jest
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
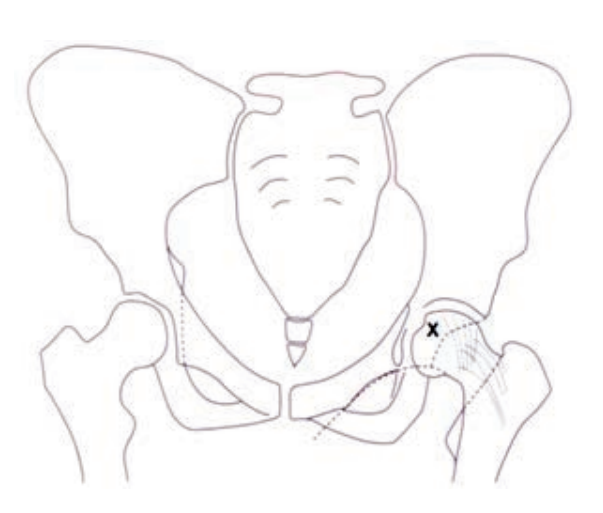
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
Wyniosłość międzykłykciowa znajduje się na nasadzie
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Fotostymulacja wykonywana jest podczas badania
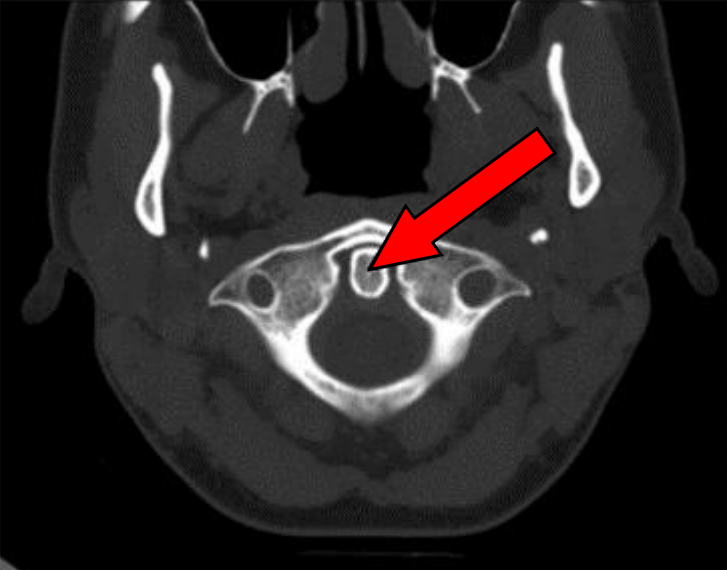
Na przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano
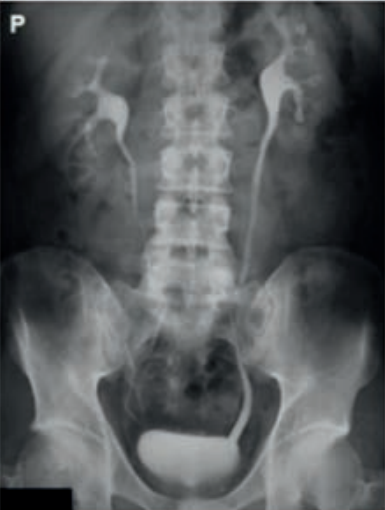
Na rentgenogramie uwidoczniono badanie
W leczeniu izotopowym tarczycy należy podać
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Na obrazie radiologicznym uwidoczniono złamanie kości