Pytanie 1
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
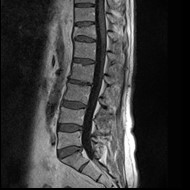
Na obrazie uwidoczniono złamanie kompresyjne kręgu
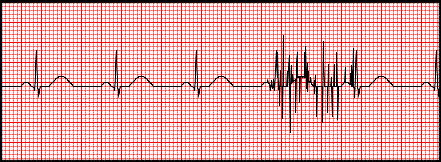
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
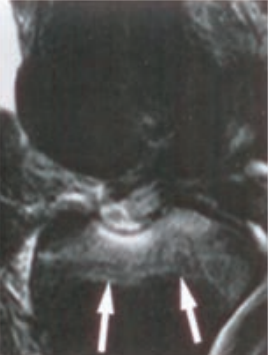
Fala głosowa rozchodzi się
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?
Obraz stawu kolanowego otrzymano metodą
Promieniowanie rentgenowskie jest
Do zdjęcia prawych otworów międzykręgowych kręgosłupa szyjnego pacjent stoi w skosie
Jaki jest cel stosowania bolusa w radioterapii?
W trakcie obrazowania metodą rezonansu magnetycznego wykorzystywane jest zjawisko wysyłania sygnału emitowanego przez
W zapisie EKG linia izoelektryczna obrazuje
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
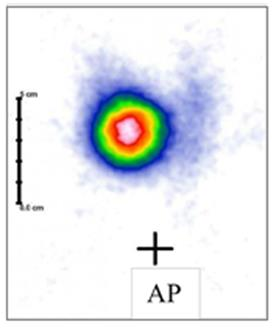
Na scyntygramie tarczycy uwidoczniono guzek
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
W przypadku migotania komór w zapisie EKG występuje
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
Na radiogramie uwidoczniono złamanie
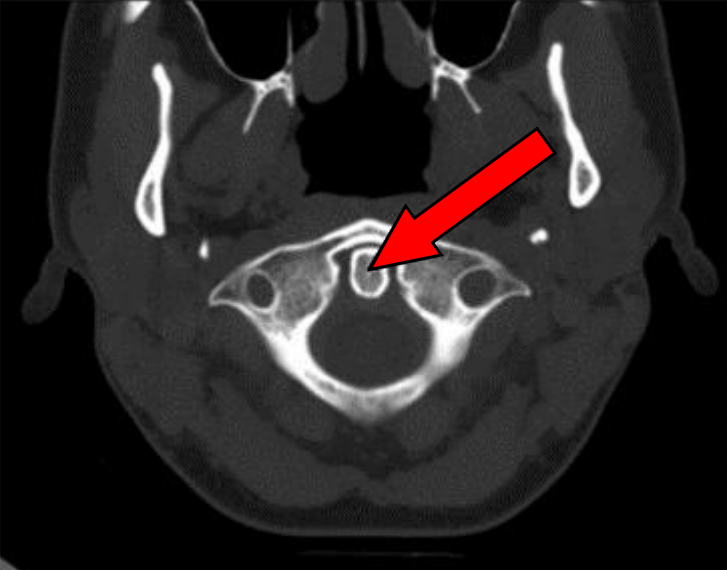
Na przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Zarejestrowany na obrazie TK artefakt jest spowodowany
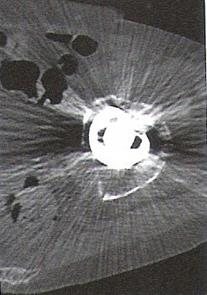
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Ligand stosuje się
Który radioizotop stosuje się do badania scyntygraficznego kości?
Chorobą układu oddechowego typu obturacyjnego jest
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
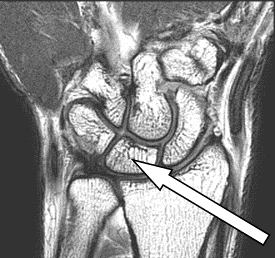
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
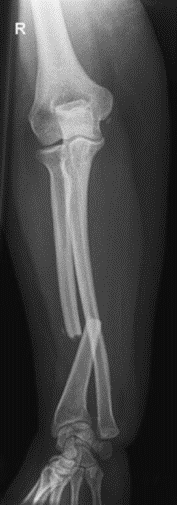
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
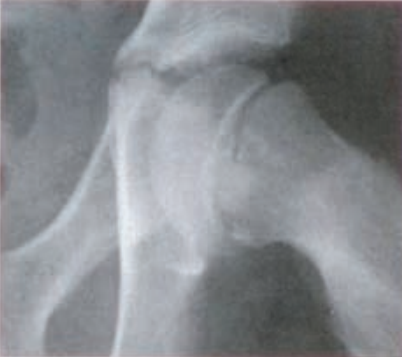
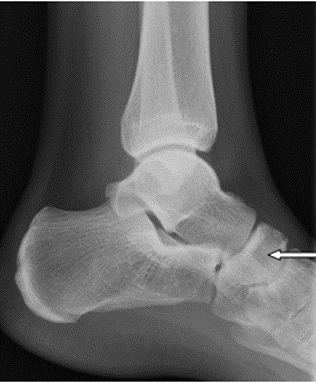
Na zamieszczonym radiogramie strzałką oznaczono kość
Technik elektroadiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
W badaniu PETCT radioizotop ulega
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
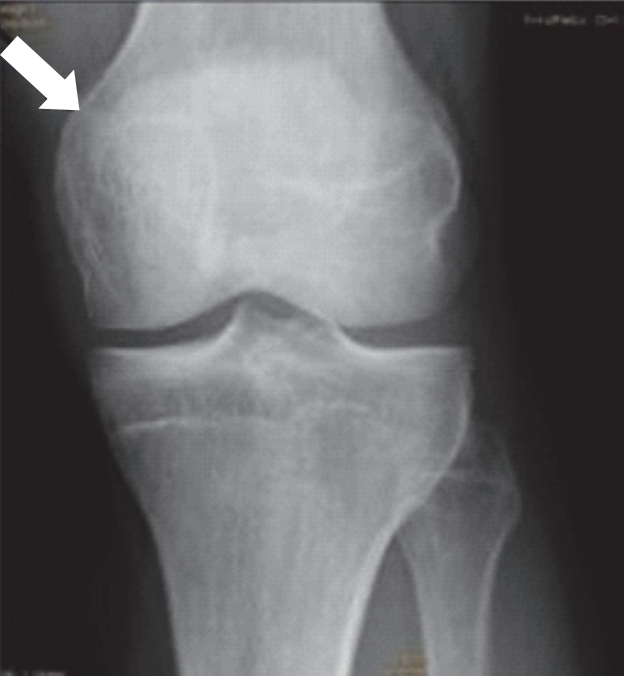
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
W medycynie nuklearnej wykorzystuje się:
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem