Pytanie 1
Pielografia zstępująca umożliwia diagnostykę
Wynik: 34/40 punktów (85,0%)
Wymagane minimum: 20 punktów (50%)
Pielografia zstępująca umożliwia diagnostykę
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W badaniu cystografii wstępującej środek kontrastowy należy podać
Limfografia to badanie kontrastowe
Głowica typu convex w USG służy do badania
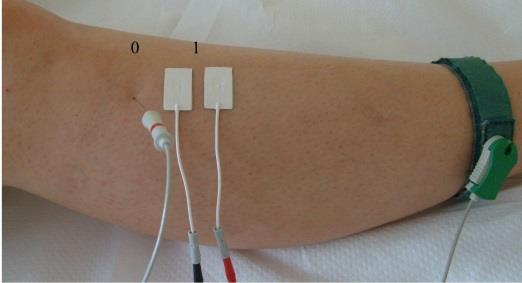
Na ilustracji przedstawiono przygotowanie pacjenta do badania
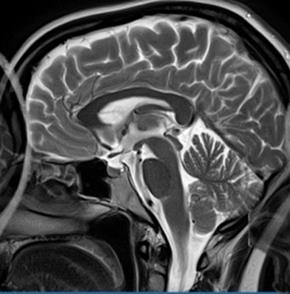
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
Wyniosłość międzykłykciowa znajduje się na nasadzie
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
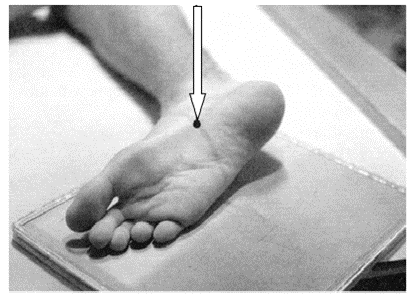
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
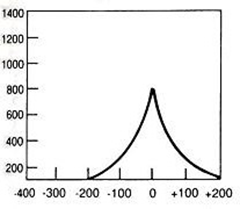
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
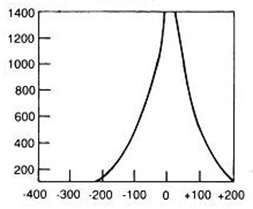
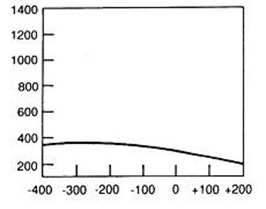
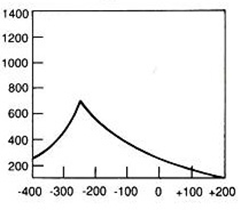
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
W jakich jednostkach mierzy się natężenie dźwięku?
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
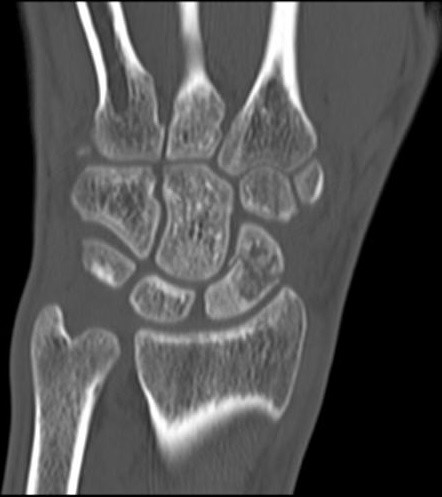
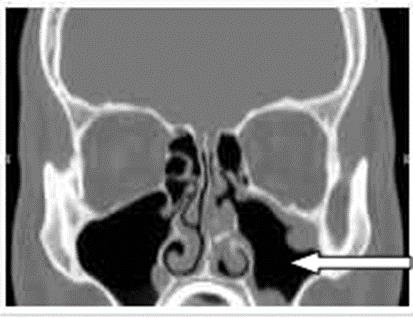
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
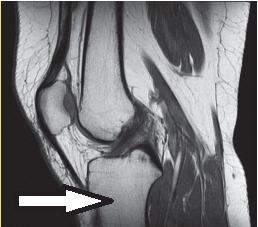
Którą kość oznaczono na obrazie rezonansu magnetycznego?
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
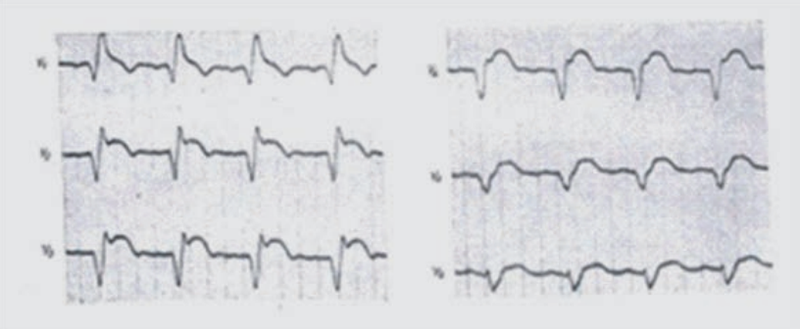
Na elektrokardiogramie zarejestrowano
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
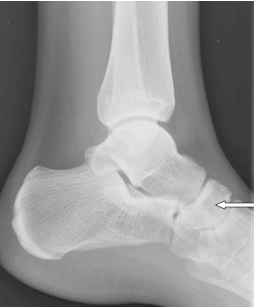
Na radiogramie strzałką oznaczono
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
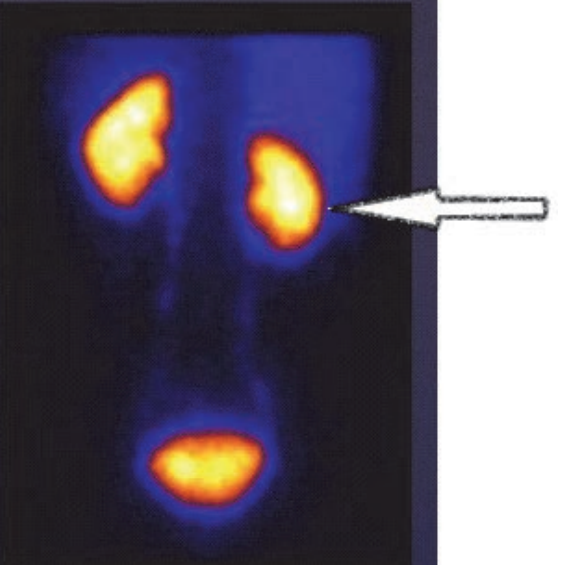
Na scyntygramie strzałką oznaczono
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
W zapisie EKG linia izoelektryczna obrazuje
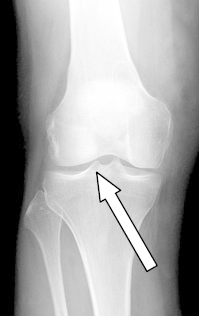
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
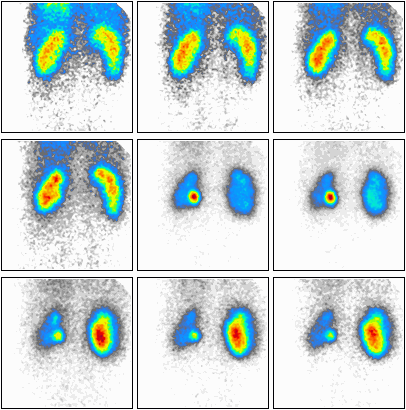
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz