Pytanie 1
Na rentgenogramie uwidoczniono badanie
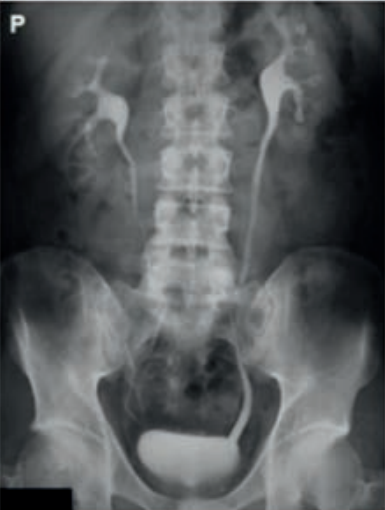
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Na rentgenogramie uwidoczniono badanie

W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
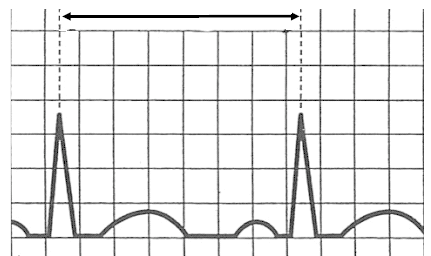
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
Na scyntygramie kości strzałkami oznaczono ogniska
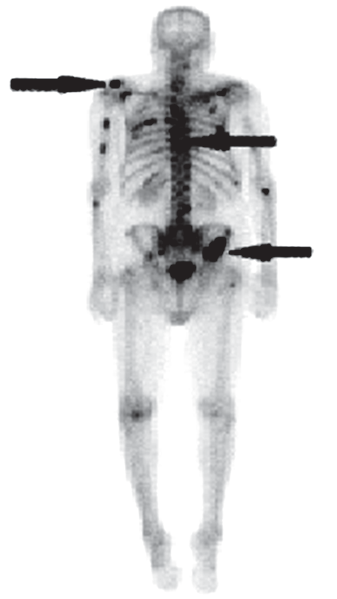
Jak konwencjonalnie frakcjonuje się dawkę w teleradioterapii?
Więzka promieniowania X to
Promieniowanie rentgenowskie jest
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Którą kość zaznaczono strzałką na radiogramie stopy?
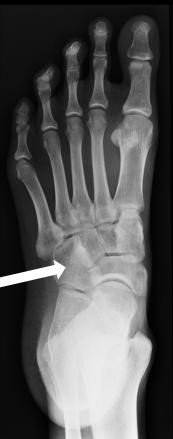
Na schemacie oznaczono
Na przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano
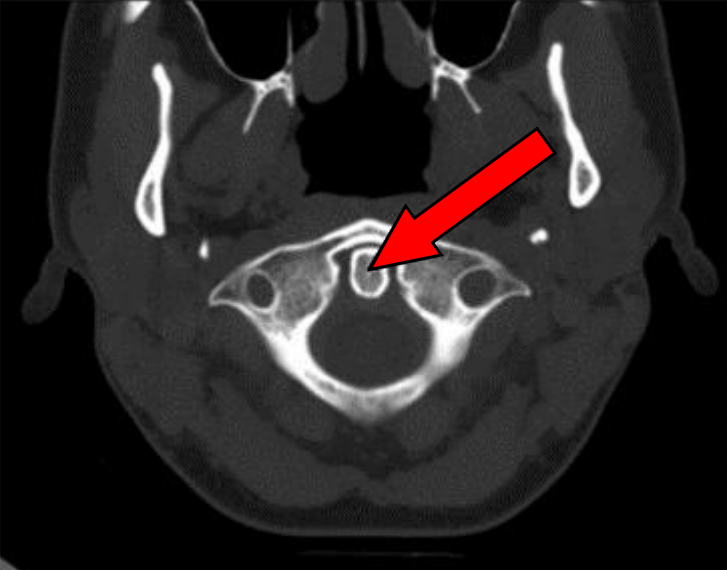
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Na radiogramie uwidoczniono złamanie
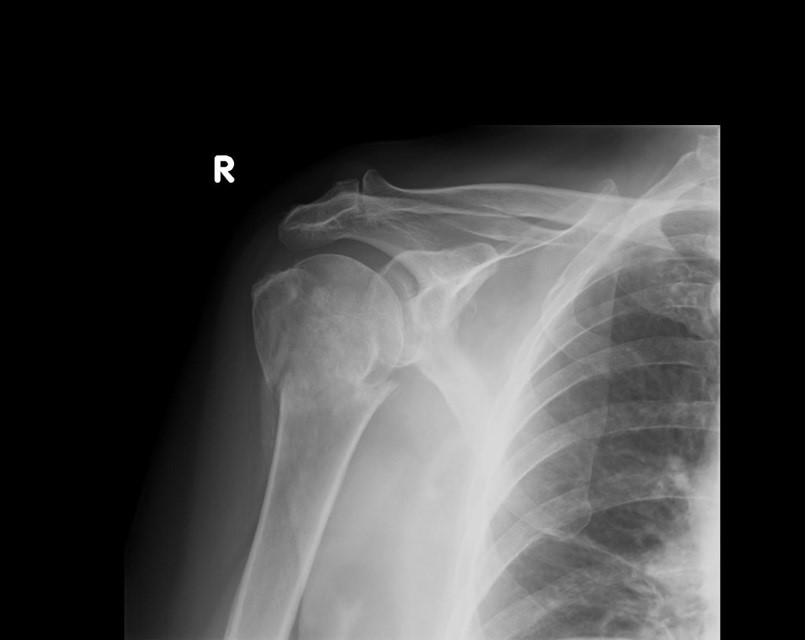
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
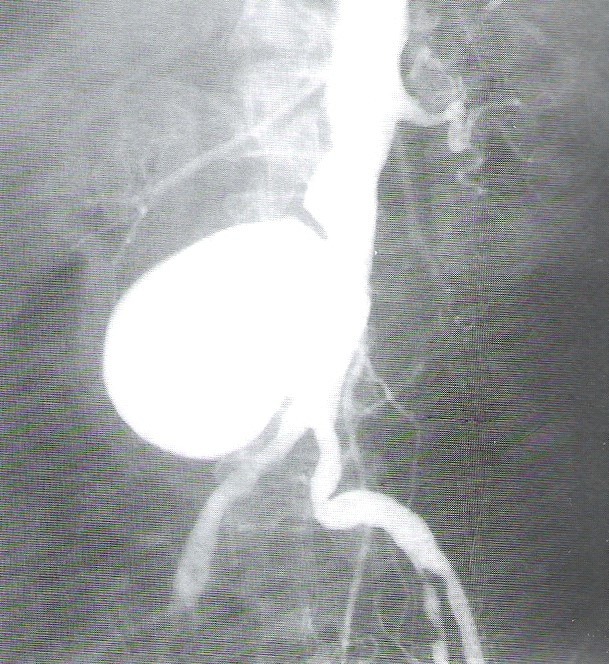
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
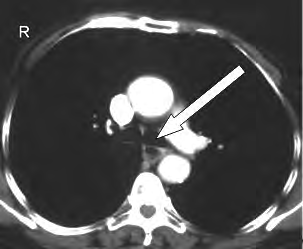
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Rak drobnokomórkowy i rak niedrobnokomórkowy to postacie organiczne nowotworów złośliwych
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
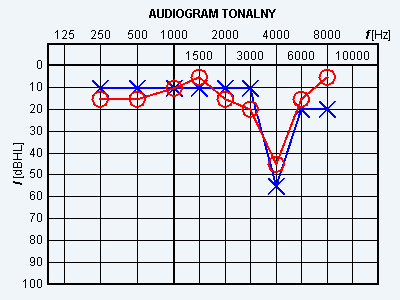
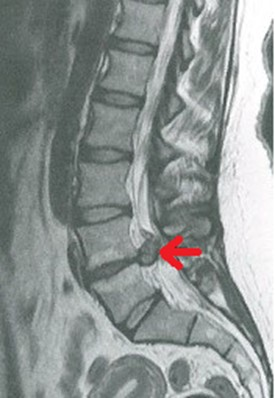
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
W brachyterapii MDR stosowane są dawki promieniowania
W badaniu cystografii wstępującej środek kontrastowy należy podać
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Na obrazie rentgenowskim strzałką zaznaczono
Technik elektroadiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
W audiometrii badanie polegające na maskowaniu (zagłuszaniu) tonów szumem białym to próba
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
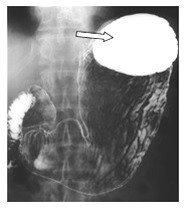
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest