Pytanie 1
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
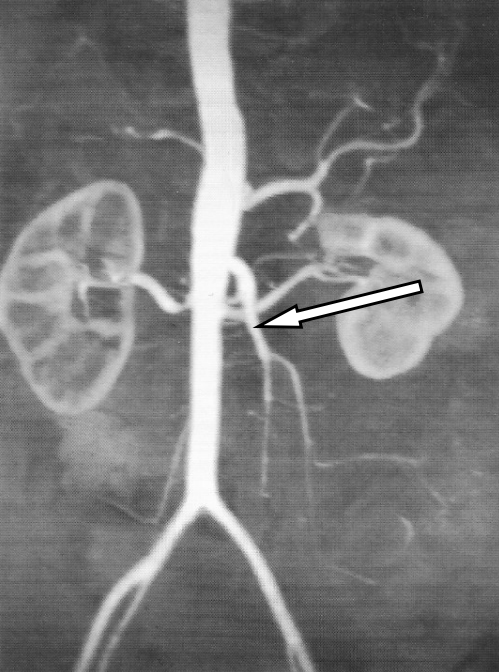
Którą tętnicę zaznaczono strzałką na obrazie MR?
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
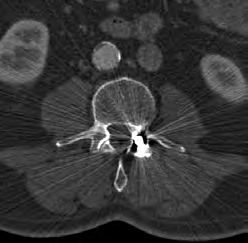
Który artefakt jest widoczny na skanie tomografii komputerowej?
Fistulografia to badanie kontrastowe
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
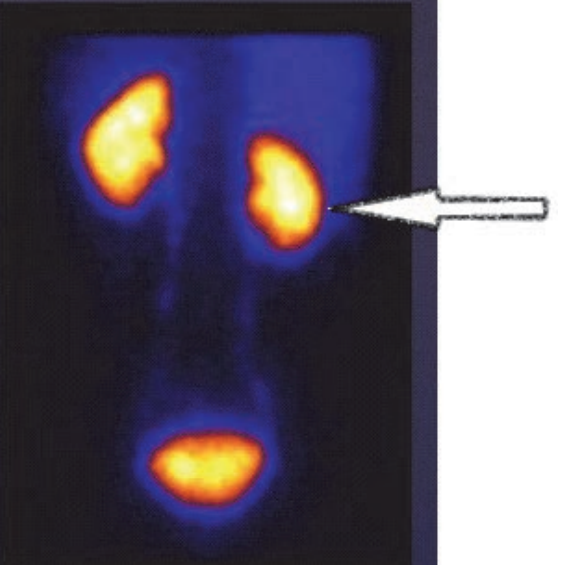
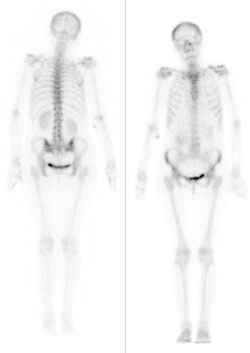
Na scyntygramie strzałką oznaczono
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
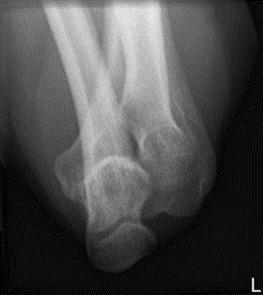
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
Pielografia to badanie układu
Rytm alfa i beta rejestruje się podczas badania
Które badanie, zgodnie z zakresem kompetencji, może samodzielnie wykonać technik elektroradiolog?
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
W obrazowaniu MR wykorzystuje się moment magnetyczny
Zgodnie ze standardami do wykonania zdjęcia bocznego czaszki, należy zastosować kasetę o wymiarze
Brachyterapia wewnątrzjamowa jest wykorzystywana podczas leczenia nowotworu
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Przedstawiony obraz został zarejestrowany podczas wykonania
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Promieniowanie rentgenowskie jest
Na obrazie uwidoczniono
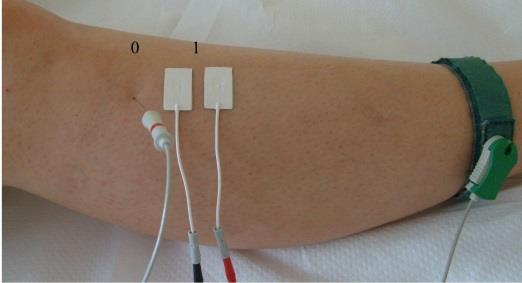
W badaniu EKG różnice potencjałów pomiędzy lewym podudziem a lewym przedramieniem rejestruje odprowadzenie
W audiometrii badanie polegające na maskowaniu (zagłuszaniu) tonów szumem białym to próba
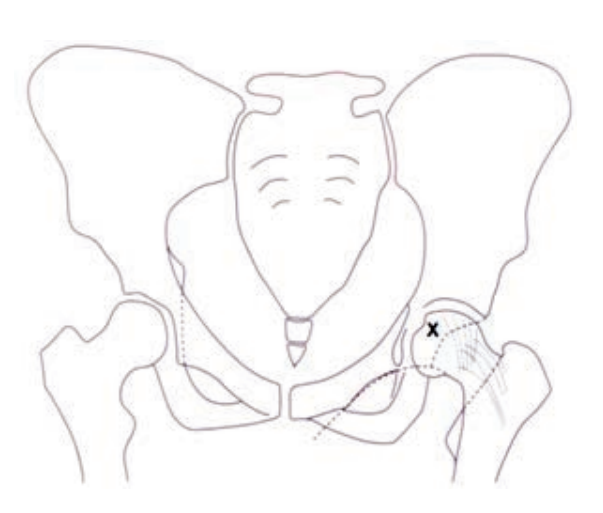
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
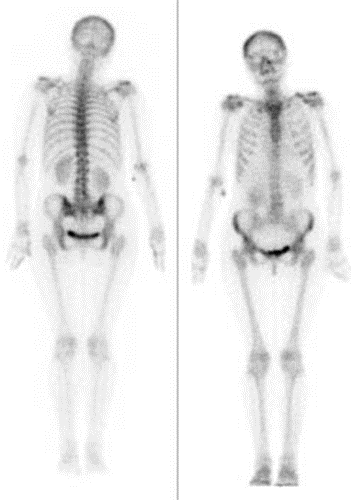
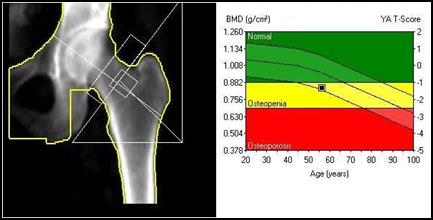
Zamieszczone na ilustracji obrazy dotyczą badania
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
Brachyterapia wewnątrzprzewodowa jest stosowana w leczeniu
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
Planowany obszar napromieniania PTV obejmuje
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
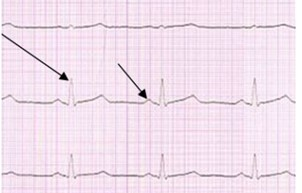
Na elektrokardiogramie strzałki wskazują załamki
Audiometria impedancyjna polega na pomiarze
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Brak odpowiedzi na to pytanie.
Czas połowicznego zaniku jest wykorzystywany
Brak odpowiedzi na to pytanie.