Pytanie 1
Na ilustracji przedstawiono zjawisko
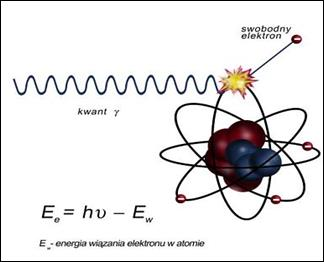
Wynik: 18/40 punktów (45,0%)
Wymagane minimum: 20 punktów (50%)
Na ilustracji przedstawiono zjawisko

Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
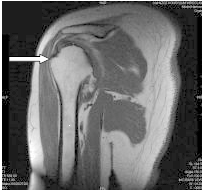
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Na ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
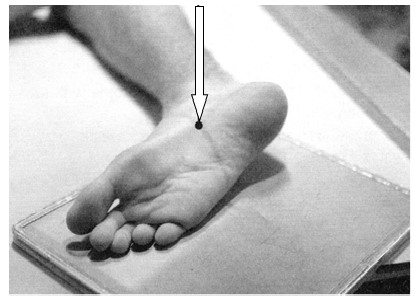
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Do zdjęcia rentgenowskiego żeber w projekcji skośnej tylnej pacjenta należy ustawić
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
Zarejestrowany na obrazie TK artefakt jest spowodowany
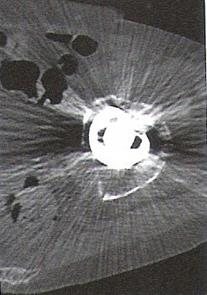
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Zdjęcie zatok przynosowych wykonuje się w pozycji
W obrazowaniu MR wykorzystuje się moment magnetyczny
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Celiakografia jest badaniem kontrastowym
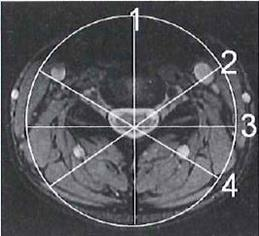
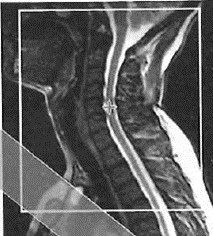
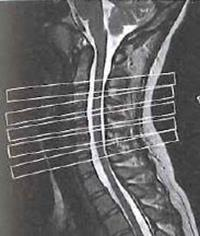
Na którym obrazie MR jest widoczne pasmo saturacji?

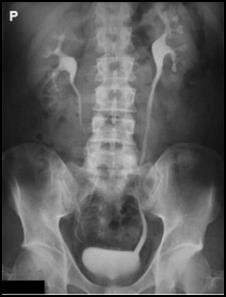
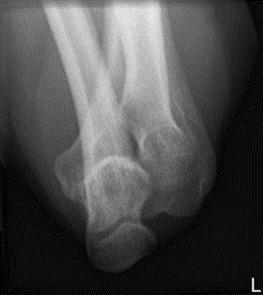
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
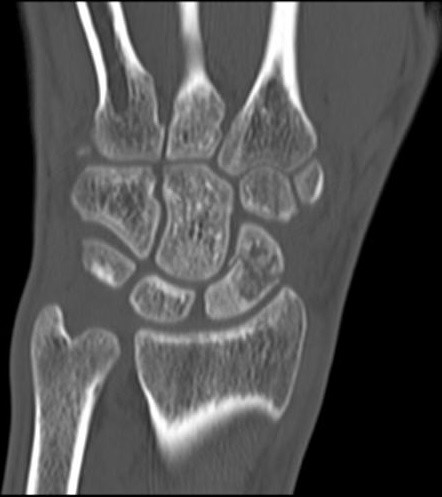
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
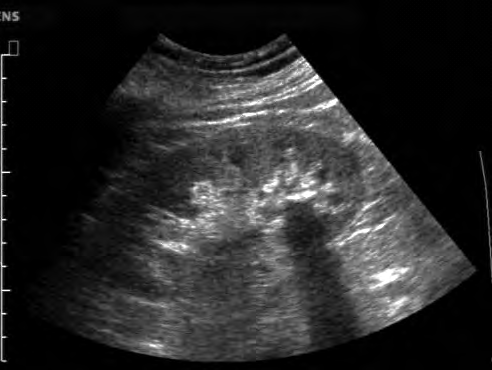
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Technik elektroradiolog do badania MR kręgosłupa lędźwiowego powinien ułożyć pacjenta:
Który detektor w radiografii wymaga laserowego czytnika obrazu?
W radiologii stomatologicznej ząb o numerze 23 to kieł
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
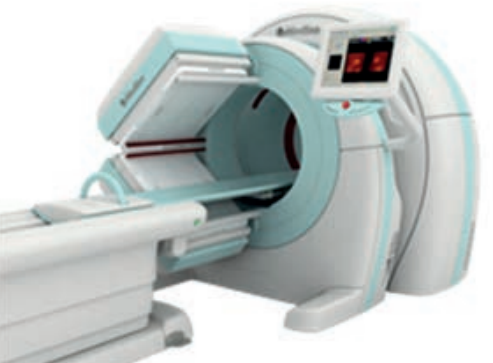
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
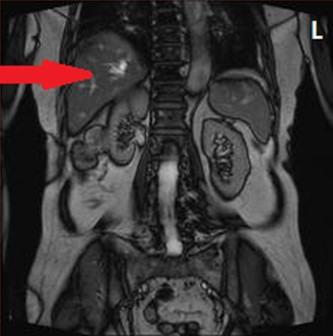
Na obrazie MR jamy brzusznej strzałką wskazano
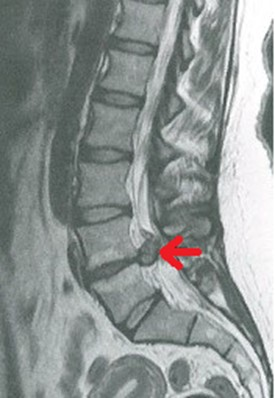
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
Powierzchnia gabinetu rentgenowskiego, w którym zainstalowany jest aparat rentgenowski wyposażony w oddzielną lampę, nie może być mniejsza niż
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
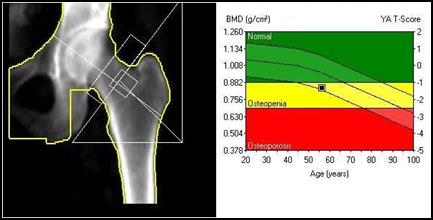
Zamieszczone na ilustracji obrazy dotyczą badania
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
Technikę bramkowania oddechowego stosuje się w badaniu MR
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla